
| A、铁和稀盐酸反应:Fe+2H+═Fe2++H2↑ |
| B、碳酸钙溶于醋酸溶液:CaCO3+2H+═Ca2++CO2↑+H2O |
| C、硫酸溶液中加入碳酸氢钠溶液:H++HCO3-═CO2↑+H2O |
| D、在氢氧化钾的稀溶液中通过量的二氧化碳气体:CO2+OH-═HCO3- |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
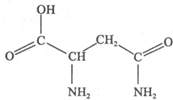 天冬酰胺(结构如图)在芦笋中含量丰富,具有提高身体免疫力的功效.
天冬酰胺(结构如图)在芦笋中含量丰富,具有提高身体免疫力的功效.| 化学式 | 键长/nm | 键角 | 沸点/℃ |
| H2S | 1.34 | 92.3° | -60.75 |
| H2Se | 1.47 | 91.0° | -41.50 |
| 编号 | I5/kJ?mol-1 | I6/kJ?mol-1 | I7/kJ?mol-1 | I8/kJ?mol-1 |
| A | 6990 | 9220 | 11500 | 18770 |
| B | 6702 | 8745 | 15455 | 17820 |
| C | 5257 | 6641 | 12125 | 13860 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 配制100mL 0.1mol?L-1的硫酸 |
B、 吸收氨气并防止倒吸 |
C、 制取少量乙烯气体 |
D、 验证溴乙烷发生消去反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1mol Na2O2与足量水完全反应时,转移电子数目为0.1NA |
| B、12g金刚石含有的共价键数为2NA |
| C、0.1mol的铜与足量的浓硫酸反应生成SO2的体积(标况)约为2.24L |
| D、标况下,22.4L CH3Cl和CH2Cl2的混合物所含氯原子数介于NA至2NA之间 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NO2-酸性氧化物 Na2O2-碱性氧化物 Al2O3-两性氧化物 |
| B、汽油-混合物 胆矾-纯净物 金刚石-单质 |
| C、纯碱-碱 硫化氢-酸 小苏打-酸式盐 |
| D、液氯-非电解质 硫酸钡-强电解质 醋酸-弱电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、一定浓度的醋酸钠溶液可使酚酞试液变红,其原因是溶液中存在如下平衡:CH3COO-+H2O?CH3COOH+OH-,使得溶液中的c(OH-)>c(H+) |
| B、某温度下,容积一定的密闭容器中进行可逆反应,X(g)+Y(g)?2Z(g)+W(s)△H>0平衡后,升高温度,c(Z)增大 |
| C、常温下,在醋酸溶液中加入少量的CH3COONa固体,会使其电离平衡正向移动 |
| D、在碳酸钙的沉淀溶解平衡体系中,加入稀盐酸,平衡向溶解的方向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、澄清透明的溶液中:H+、Fe2+、SO42-、NO3- |
| B、使甲基橙变红的溶液中:Ca2+、NH4+、CH3COO-、Cl- |
| C、0.1 mol?L-1的BaCl2溶液中:K+、Na+、OH-、NO3- |
| D、由水电离出的c(H+)=10-12 mol?L-1的溶液中:Mg2+、K+、Br-、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com