
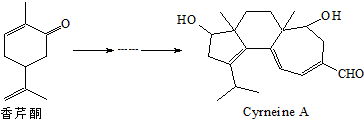
| A. | 香芹酮化学式为C9H12O | |
| B. | Cyrneine A可以发生加成反应、消去反应和氧化反应 | |
| C. | 香芹酮和Cyrneine A均能使酸性KMnO4溶液褪色 | |
| D. | 香芹酮和Cyrneine A可以通过氯化铁溶液鉴别 |
分析 由有机物结构简式确定有机物的分子式,香芹酮含有碳碳双键,Cyrneine A分子含有碳碳双键、醛基以及羟基,结合烯烃、醛以及醇的性质确定有机物的性质,以此解答该题.
解答 解:A.根据有机物的结构简式并结合键线式的结构特点可知,香芹酮的化学式为C10H14O,故A错误;
B.Cyrneine A分子含有碳碳双键、醛基以及羟基,且与羟基相连的碳原子的邻位碳原子上含有氢原子,所以A可以发生加成反应、氧化反应、消去反应,故B正确;
C.香芹酮和Cyrneine A分子中均含有碳碳双键,均能使酸性KMnO4溶液褪色,故C正确;
D.都不含有酚羟基,用过氯化铁溶液不能鉴别,故D错误.
故选BC.
点评 本题考查有机物的结构和性质,是高考中的常见题型和重要的考点之一,属于中等难度的试题,意在考查学生对官能团与物质性质的关系及常见的有机反应类型的判断能力.试题基础性强,侧重对学生能力的培养和解题方法的指导.该题的关键是准确判断出分子中含有的官能团,然后依据相应官能团的结构和性质,灵活运用即可.有利于培养学生的知识迁移能力和辑推理能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 升高温度能够增加活化分子的总数 | |
| B. | 增大反应物浓度能够增加活化分子的百分数 | |
| C. | 加入催化剂可以使本来不能发生的反应发生化学反应 | |
| D. | 压强影响所有化学反应的速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 实验序号 | 实验操作 | 现象 | 结论 |
| Ⅰ | 向氯水中加入淀粉KI溶液 | 溶液变蓝 | 氯水中含有氯气分子 |
| Ⅱ | 将氯水滴入AgNO3溶液 | 产生白色沉淀 | 氯气与水反应的产物中含有Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol冰醋酸和1mol乙醇经催化加热反应可生成H2O分子数为NA | |
| B. | 常温常压下,将15g NO和8g O2混合,所得混合气体分子总数小于0.5NA | |
| C. | 标准状况下,2.24 L的CCl4中含有的C-Cl键数为0.4NA | |
| D. | 6.8g熔融态KHSO4中含有0.1NA个阳离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
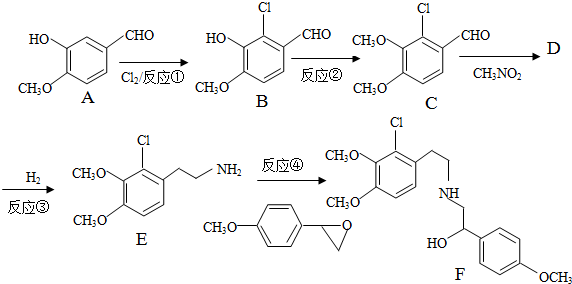
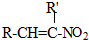 +H2O
+H2O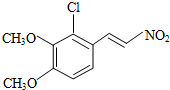 ,反应③中1摩尔D需要4摩尔H2才能转化为E
,反应③中1摩尔D需要4摩尔H2才能转化为E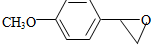 很多种同分异构体,请写出符合下列条件的一种同分异构体的结构简式
很多种同分异构体,请写出符合下列条件的一种同分异构体的结构简式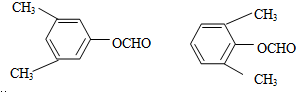 .
.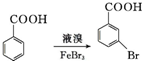 .写出以
.写出以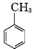 为原料制备
为原料制备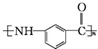 的合成路线流程图(无机试剂任选).(合成路线常用表示方法为:A$→_{反应试剂}^{反应试剂}$B …$→_{反应试剂}^{反应试剂}$目标产物)
的合成路线流程图(无机试剂任选).(合成路线常用表示方法为:A$→_{反应试剂}^{反应试剂}$B …$→_{反应试剂}^{反应试剂}$目标产物)查看答案和解析>>
科目:高中化学 来源: 题型:解答题
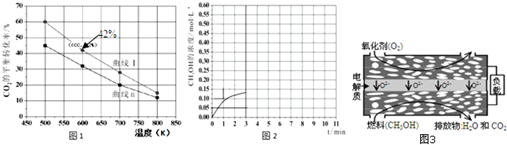
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入足量氢氧化钠溶液后产生的浑浊不溶解 | |
| B. | 用pH试纸检验呈弱酸性 | |
| C. | 滴入KSCN溶液后溶液变血红色 | |
| D. | 溶液显浅黄色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com