

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
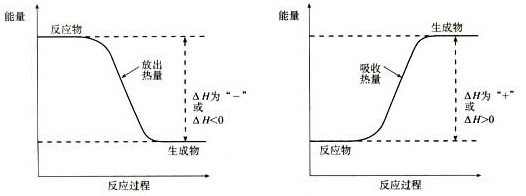
 H2SO4(ÅØ)+ NaOH(aq)=
H2SO4(ÅØ)+ NaOH(aq)= Na2SO4(aq)+ H2O(l)£»”÷H2 = m,ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
Na2SO4(aq)+ H2O(l)£»”÷H2 = m,ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ| A£®ÉĻŹöČČ»Æѧ·½³ĢŹ½ÖŠµÄ¼ĘĮæŹż±ķŹ¾·Ö×ÓøöŹż | B£®”÷H1>”÷H2 |
| C£®”÷H2 =" -" 57.3 kJ”¤mol-1 | D£®|”÷H1|>|”÷H2| |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®Ö²Īļ¹āŗĻ×÷ÓĆ£ŗ¹āÄÜ”śÉśĪļÖŹÄÜ |
| B£®µēµĘ·¢¹ā£ŗµēÄÜ”ś»ÆѧÄÜ |
| C£®Ä¾²ńÖó·¹£ŗÉśĪļÖŹÄÜ”śČČÄÜ |
| D£®Ģ«ŃōÄÜČČĖ®Ę÷£ŗ¹āÄÜ”śČČÄÜ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®øĆ¹ż³ĢĪŖĪļĄķ±ä»Æ | B£®½šøÕŹÆ±ČŹÆÄ«Ó²¶Č“ó |
| C£®ŹÆÄ«±Č½šøÕŹÆĪČ¶Ø | D£®ŹÆÄ«½šøÕŹÆ²»ÄÜ»„Ļą×Ŗ»Æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĪŹ“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®Ä³·“Ó¦µÄÉś³ÉĪļµÄ×ÜģŹ“óÓŚ·“Ó¦ĪļµÄ×ÜģŹŹ±£¬·“Ó¦ĪüČČ£¬¦¤H£¾0 |
| B£®»Æѧ·“Ó¦¹ż³ĢÖŠ£¬·¢ÉśĪļÖŹ±ä»ÆµÄĶ¬Ź±²»Ņ»¶Ø·¢ÉśÄÜĮæ±ä»Æ |
| C£®SO2ÄÜČÜÓŚĖ®£¬ĖłµĆČÜŅŗÄܵ¼µē£¬ĖłŅŌSO2ŹĒµē½āÖŹ |
| D£®¼ĘĖćij·“Ó¦µÄ·“Ó¦ČČæÉÓĆÉś³ÉĪļµÄ¼üÄÜ×ÜŗĶ¼õČ„·“Ó¦ĪļµÄ¼üÄÜ×ÜŗĶ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā

 N2£Øg£© + 2 CO2£Øg£© ”÷H = kJ/mol”£
N2£Øg£© + 2 CO2£Øg£© ”÷H = kJ/mol”£ 2NH3(g)£»”÷H<0£¬ĘäĘ½ŗā³£ŹżKÓėĪĀ¶ČTµÄ¹ŲĻµČēĻĀ±ķ£ŗ
2NH3(g)£»”÷H<0£¬ĘäĘ½ŗā³£ŹżKÓėĪĀ¶ČTµÄ¹ŲĻµČēĻĀ±ķ£ŗ| T/K | 298 | 398 | 498 |
| Ę½ŗā³£ŹżK | 4.1”Į106 | K1 | K2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®ŅĄ¾Ż¶”“ļ¶ūŠ§Ó¦æÉĒų·ÖČÜŅŗŗĶ½ŗĢå |
| B£®ĪŖ×¼Č·²ā¶ØŃĪĖįÓėNaOHČÜŅŗ·“Ó¦µÄÖŠŗĶČČ£¬ĖłÓĆĖįŗĶ¼īµÄĪļÖŹµÄĮæ±ŲŠėĻąµČ |
| C£®²ā¶ØĮņĖįĶ¾§ĢåÖŠ½į¾§Ė®ŗ¬ĮæŹ±£¬×ĘÉÕÖĮ¹ĢĢå·¢ŗŚ£¬²ā¶ØÖµ“óÓŚĄķĀŪÖµ |
| D£®ŃĪĪöæÉĢį“æµ°°×ÖŹ²¢±£³ÖĘäÉśĄķ»īŠŌ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
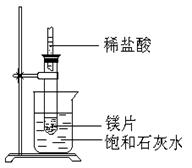
 ÖŠ“ķĪóµÄŹĒ
ÖŠ“ķĪóµÄŹĒ 21
21| A£®ÖŠŗĶ·“Ó¦ŹĒ·ÅČČ·“Ó¦ | B£®ÓĶÖ¬ŌŚČĖĢåÖŠŃõ»ÆŹĒ·ÅČČ·“Ó¦ |
| C£®Ć¾ÓėŃĪĖį·“Ó¦ŹĒĪüČČ·“Ó¦ | D£®Ēā·Ö×Ó£ØH£H£©±ä³É2øöHŠčĪüŹÕÄÜĮæ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com