
已知常温下在溶液中可发生如下两个离子反应:
Ge4++Fe2+===Fe3++Ge3+,Sn2++2Fe3+===2Fe2++Sn4+
由此可以确定Fe2+、Ge3+、Sn2+三种离子的还原性由强到弱的顺序是( )
A.Sn2+、Fe2+、Ge3+ B.Sn2+、Ge3+、Fe2+
C.Ge3+、Fe2+、Sn2+ D.Fe2+、Sn2+、Ge3+
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
区别CH4、CH2===CH2、CH≡CH的最简易方法是( )
A.分别通入溴水
B.分别通入酸性高锰酸钾溶液
C.分别在空气中点燃
D.分别通入盛有碱石灰的干燥管
查看答案和解析>>
科目:高中化学 来源: 题型:
某学校课外活动小组仅有一大一小两试管和氢氧化钠溶液。甲、乙两个同学找来铝制废牙膏皮,各自设计了一套装置如下图,制取并收集一试管氢气。
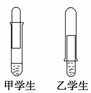
(1)哪个学生设计的装置比较合理?____(填“甲”或“乙”),另一设计装置不合理的原
因________________________________________________________________________
________________________________________________________________________。
(2)用比较合理的装置制取氢气,要使氢气充满收集氢气的试管,应该采取的措施是
________________________________________________________________________。
(3)还可以用哪些常见物品和试剂代替废牙膏皮和氢氧化钠溶液完成实验?
________________________________________________________________________
________________________________________________________________________。
(4)测定H2和空气混合气体的爆炸范围实验如下所述。取10支大试管,依次盛水90%(体积分数)、80%……再用排水集气法收集H2,而后分别把试管口移近酒精灯火焰,实验结果如下:
| H2体积分数/% | 90 | 80 | 70 | 60~20 | 10 | 5 |
| 空气体积分数/% | 10 | 20 | 30 | 40~80 | 90 | 95 |
| 点燃现象 | 安静 燃烧 | 安静 燃烧 | 弱爆炸 | 强爆炸 | 弱爆炸 | 不燃烧 不爆炸 |
由上述实验结果评价:用向下排空气法收集H2,保持试管倒置移近火焰,如果只发出轻微的“噗声”,表示收集的H2已纯净的说法的真正涵义:________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作中正确的是( )
①用剩的药品为避免浪费应放回原瓶 ②蒸发氯化钠溶液时要用玻璃棒不断搅动 ③称取易潮解的药品必须放在玻璃器皿中称量 ④用试纸检验气体性质时,手拿着试纸经水润洗后靠近气体观察试纸颜色变化
A.②③ B.②③④ C.②④ D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验中,溶液颜色有明显变化的是( )
A.少量明矾溶液加入到过量NaOH溶液中
B.往FeCl3溶液中滴入KI溶液,再滴入淀粉溶液
C.少量Na2O2固体加入到过量NaHCO3溶液中
D.在酸性高锰酸钾溶液中滴入少量Fe2(SO4)3稀溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学实验小组的同学为探究和比较SO2和氯水的漂白性,设计了如下的实验装置。
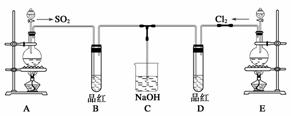
(1)实验室用装置A制备SO2。某同学在实验时发现打开A的分液漏斗活塞后,漏斗中液体未流下,你认为原因可能是________________________________________________
(2)实验室用装置E制备Cl2,其反应的化学方程式为:MnO2+4HCl(浓)MnCl2+Cl2+2H2O。若有6 mol 的HCl参加反应,则转移的电子总数为_______________________;
(3)①反应开始一段时间后,观察到B、D两个试管中的品红溶液出现的现象是:
B:____________________________________,D:______________________________。
②停止通气后,再给B、D两个试管分别加热;两个试管中的现象分别为:
B:____________________________________,D:________________________________。
(4)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强。他们将制得的SO2和Cl2按1∶1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样。请你分析该现象的原因(用化学方程式表示)_______________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
根据下列装置图回答问题(装置图用符号表示):
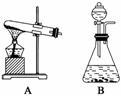
(1)双氧水(H2O2)是无色液体,可发生如下化学反应:2H2O2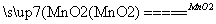 2H2O+O2↑。
2H2O+O2↑。
反应中MnO2的作用是________。在实验室利用此反应制取氧气时,应选用的气体发生装置是________,简述检查本装置气密性的方法: _______________________________
________________________________________________________________________。
(2)KClO3在MnO2作催化剂时,加热也可以制得氧气。应选用的气体发生装置是
________。
(3)为了验证MnO2在KClO3分解过程中起到了催化剂作用,我们要把反应后的产物分离,提取出MnO2并验证其的确是催化剂。分离出MnO2的操作有________、________、洗涤、烘干、称量。为证明MnO2是催化剂,还需要知道的一个数据是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值,下列叙述正确的是
A.1 mol Na2O和Na2O2混合物中含有的阴、阳离子总数是3 NA
B.标准状况下,22.4 L NH3中含有共价键的数目为NA
C.1 molCl2与足量Fe反应转移电子数一定为3NA
D.标准状况下,11.2 L SO3所含的分子数目为0.5 NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com