
下列叙述正确的是( )
A.溶度积大的化合物溶解度肯定大
B.向含有AgCl固体的溶液中加入适量的水使AgCl溶解又达到平衡时,AgCl的溶度积不变,其溶解度也不变
C.将难溶电解质放入纯水中,溶解达到平衡时,电解质离子的浓度的乘积就是该物质的溶度积
D.AgCl水溶液的导电性很弱,所以AgCl为弱电解质
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
糖类、油脂和蛋白质是维持人体生命活动所必需的三大营养物质。下列说法正确的是
A.利用淀粉可直接检验食盐中是否含有碘酸钾
B.淀粉和纤维素水解的最终产物都能发生银镜反应
C.植物油能使溴的四氯化碳溶液褪色
D.棉花、羊毛、蚕丝等天然纤维的成分都是纤维素
查看答案和解析>>
科目:高中化学 来源: 题型:
已知扎那米韦是流感病毒神经氨酸酶抑制剂,其对流感病毒的抑制是以慢结合的方式进行的,具有高度特异性,其分子结构如图所示。

下列说法正确的是( )
A.该物质的分子式为C12H19N4O7
B.1 mol该物质与NaOH溶液反应,可以消耗4 mol NaOH
C.在一定条件下,该物质可以发生消去、加成、取代等反应
D.该物质能使溴水或高锰酸钾溶液褪色,能与FeCl3溶液发生显色反应
查看答案和解析>>
科目:高中化学 来源: 题型:
双水杨酯可用于缓解包括头痛、牙痛、神经痛、关节痛及软组织炎症等各类疼痛,其结构如图所示。下列关于双水杨酯的性质描述正确的是( )
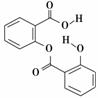
A.能与FeCl3溶液发生显色反应
B.能使酸性KMnO4溶液褪色
C.能发生加成、取代、消去反应
D.1 mol该物质最多可与2 mol NaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.向0.1 mol·L-1 Na2CO3溶液中滴加酚酞,溶液变红色
B.Al3+、NO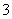 、Cl-、CO
、Cl-、CO 、Na+可以大量共存于pH=2的溶液中
、Na+可以大量共存于pH=2的溶液中
C.乙醇和乙酸都能溶于水,都是电解质
D.分别与等物质的量的HCl和H2SO4反应时,消耗的NaOH的物质的量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关说法正确的是
A.SiO2是酸性氧化物,所以SiO2能与NaOH溶液反应
B.SO2可以使溴水褪色,所以SO2具有漂白性
C.若某碱性溶液的焰色反应呈黄色,则该溶液的溶质一定为NaOH
D.NH3的水溶液可以导电,所以NH3是电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
氨基甲酸铵(H2NCOONH4)是一种白色固体,易水解、受热易分解,可用做肥料、灭火剂、洗涤剂等。某化学兴趣小组模拟制备氨基甲酸铵,反应的化学方程式如下:2NH3(g)+CO2(g) H2NCOONH4(s) △H<0
H2NCOONH4(s) △H<0
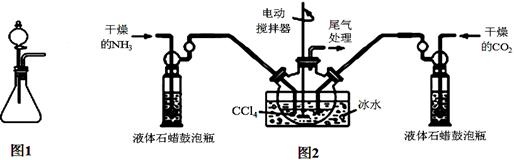
(注:四氯化碳与液体石蜡均为惰性介质)
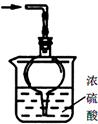
(1)如用图1装置制取氨气,分液漏斗中的试剂名称是 。
(2)制备氨基甲酸铵的装置如图2所示,把氨气和二氧化碳通入四氯化碳中,不断搅拌混合,生成的氨基甲酸铵小晶体悬浮在四氯化碳中。当悬浮物较多时,停止制备。
①发生器用冰水冷却的目的是 。
液体石蜡鼓泡瓶的作用是 。
 ②从反应后的混合物中分离出产品的实验方法是 (填操作名称)。为了得到纯净的产品,应采取的方法是 (填选项序号)。
②从反应后的混合物中分离出产品的实验方法是 (填操作名称)。为了得到纯净的产品,应采取的方法是 (填选项序号)。
a. 常压加热烘干 b. 高压加热烘干 c. 减压40 ℃以下烘干
③尾气处理装置如右图所示。球形干燥管的作用: ;
浓硫酸的作用: 。
(3)取因部分变质而混有NH4HCO3的氨基甲酸铵样品15.64g,用足量石灰水充分处理后,使样品中所有碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为20 g。则样品中氨基甲酸铵的物质的量分数为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
烟气(主要污染物SO2、NOx)经O3预处理后用CaSO3水悬浮液吸收,可减少烟气中SO2、NOx的含量。O3氧化烟气中SO2、NOx的主要反应的热化学方程式为:
NO(g)+O3(g)=NO2(g)+O2(g) △H=-200.9kJ·mol-1
NO(g)+1/2O2(g)=NO2(g) △H=-58.2kJ·mol-1
SO2(g)+O3(g)=SO3(g)+O2(g) △H=-241.6kJ·mol-1
(1)反应3NO(g)+O3(g)=3NO2(g)的△H=_______mol·L-1。
(2)室温下,固定进入反应器的NO、SO2的物质的量,改变加入O3的物质的量,反应一段时间后体系中n(NO)、n(NO2)和n(SO2)随反应前n(O3):n(NO)的变化见右图。
①当n(O3):n(NO)>1时,反应后NO2的物质的量减少,其原因是__________。
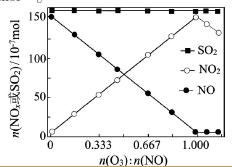 ②增加n(O3),O3氧化SO2的反应几乎不受影响,其可能原因是 _________。
②增加n(O3),O3氧化SO2的反应几乎不受影响,其可能原因是 _________。
(3)当用CaSO3水悬浮液吸收经O3预处理的烟气时,清液(pH约为 8)中SO32-将NO2转化为NO2-,其离子方程式为:___________。
(4)CaSO3水悬浮液中加入Na2SO4溶液,达到平衡后溶液中c(SO32-)=________[用c(SO42-)、Ksp(CaSO3)和Ksp(CaSO4)表示];CaSO3水悬浮液中加入Na2SO4溶液能提高NO2的吸收速率,其主要原因是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中含有HCO3﹣、SO32﹣、CO32﹣、CH3COO﹣4种阴离子.若向其中加入足量的Na2O2后,溶液中离子浓度基本保持不变的是()
| A. | CH3COO﹣ | B. | SO32﹣ | C. | CO32﹣ | D. | HCO3﹣ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com