
【题目】已知25℃时Ksp(BaSO4)=1.0×1010。该温度下,CaSO4悬浊液中c(Ca2+)与c(SO42)的关系如图所示,下列叙述正确的是( )
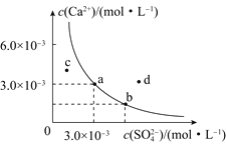
A.向a点的溶液中加入等物质的量固体Na2SO4或Ca(NO3)2,析出的沉淀量不同
B.a、b、c、d四点对应的体系中,d点体系最稳定
C.升高温度后,溶液可能会由a点转化为b点
D.反应Ba2+(aq) + CaSO4(s)![]() BaSO4(s) + Ca2+(aq)的平衡常数K=9×104
BaSO4(s) + Ca2+(aq)的平衡常数K=9×104
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】已知重铬酸钾(K2Cr2O7)具有强氧化性,其还原产物Cr3+在水溶液中呈绿色或蓝绿色。在K2Cr2O7溶液中存在下列平衡:Cr2O72(橙色) + H2O![]() 2CrO42(黄色) + 2H+。用K2Cr2O7溶液进行下列实验:结合实验,下列说法不正确的是( )
2CrO42(黄色) + 2H+。用K2Cr2O7溶液进行下列实验:结合实验,下列说法不正确的是( )
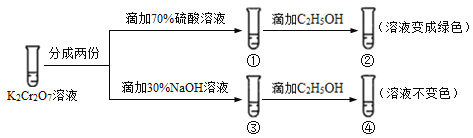
A.①中溶液橙色加深,③中溶液变黄
B.②中Cr2O72被C2H5OH还原
C.对比②和④可知K2Cr2O7酸性溶液氧化性强
D.若向④中加入70%H2SO4溶液至过量,溶液变为橙色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家开发的一种“磷酸钒锂/石墨离子电池”在4.6V电位区电池总反应为:Li3C6+V2(PO4)3![]() 6C+Li3V2(PO4)3。下列有关说法正确的是
6C+Li3V2(PO4)3。下列有关说法正确的是
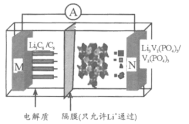
A.该电池比能量高,用Li3V2(PO4)3做负极材料
B.放电时,外电路中通过0.1 mol电子M极质量减少0.7 g
C.充电时,Li+向N极区迁移
D.充电时,N极反应为V2(PO4)3+3Li++3e-=Li3V2(PO4)3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH=-49.0kJ·mol-1。一定条件下,向体积为1L的恒容密闭容器中充入1molCO2和3mol H2,测得CO2和CH3OH(g)的浓度随时间变化曲线如图所示。下列叙述中正确的是( )
CH3OH(g)+H2O(g) ΔH=-49.0kJ·mol-1。一定条件下,向体积为1L的恒容密闭容器中充入1molCO2和3mol H2,测得CO2和CH3OH(g)的浓度随时间变化曲线如图所示。下列叙述中正确的是( )

A.3min时,用CO2的浓度表示的υ(正)等于用CH3OH的浓度表示的υ(逆)
B.从0-10min,用H2表示的平均反应速率v(H2)=0.75mol·L-1·min-1
C.13min时,向容器中充入2mol氦气,该反应的化学反应速率增加
D.从反应达到平衡状态时,CO2的平衡转化率为75%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向100 mL 0.01 molL﹣1 HA溶液中逐滴加入0.02 molL﹣1的MOH溶液,图中所示曲线表示混合溶液的pH变化情况,下列说法不正确的是

A. HA为一元强酸,MOH为一元弱碱
B. N点溶液中离子浓度大小关系为:c(M+)=c(A﹣)>c(H+)=c(OH﹣)
C. N点水的电离程度大于K点水的电离程度
D. N→K之间曲线上任意一点都有c(M+) >c(OH﹣)>c(A﹣)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某温度(t ℃)时,水的Kw=1×10-12,则该温度____(填“>”“<”或“=”)25 ℃,其理由是_________________________________________________________。
(2)该温度下,c(H+)=1×10-7 mol/L的溶液呈_____(填“酸性、碱性或中性”);若该溶液中只存在NaOH溶质,则由H2O电离出来的c(OH-)=________ mol/L。
(3)实验室用Zn和稀硫酸制取H2,反应时溶液中水的电离平衡______(填“向左” “向右”或“不”,下同 )移动。在新制氯水中加入少量的NaCl固体,水的电离平衡________移动。
(4)25 ℃时,pH=4的盐酸中水的电离程度________(填“大于”“小于”或“等于”)pH=10的Ba(OH)2溶液中水的电离程度。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学电源在日常生活和高科技领域中都有广泛应用。下列说法不正确的是
A.  Zn2+向Cu电极方向移动,Cu电极附近溶液中H+浓度增加
Zn2+向Cu电极方向移动,Cu电极附近溶液中H+浓度增加
B. 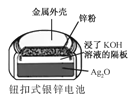 正极的电极反应式为Ag2O+2e+H2O2Ag+2OH
正极的电极反应式为Ag2O+2e+H2O2Ag+2OH
C.  锌筒作负极,发生氧化反应,锌筒会变薄
锌筒作负极,发生氧化反应,锌筒会变薄
D.  使用一段时间后,电解质溶液的酸性减弱,导电能力下降
使用一段时间后,电解质溶液的酸性减弱,导电能力下降
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上合成氨N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.4 kJ·mol-1一般采用700 K左右的温度,其原因是( )
2NH3(g) ΔH=-92.4 kJ·mol-1一般采用700 K左右的温度,其原因是( )
①提高H2的转化率 ②适当提高氨的合成速率 ③提高氨的产率 ④催化剂在700 K时活性最大
A.只有①B.②④C.②③④D.①②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表列出了A-F6种元素在周期表中短周期的位置。
C | D | ||||||
A | B | E | F |
请回答下列问题:
(1)C元素在周期表中的位置___;C元素的一种氧化物是温室气体,该氧化物的电子式为:___。
(2)A和B的最高价氧化物对应的水化物碱性较强的是___;(填化学式)
(3)D与同族下一周期元素的气态氢化物的沸点较高的是___(填化学式),原因是___。
(4)元素E与元素F相比,非金属性较强的是___(用元素符号填写),下列表述中能证明这一事实的是___(可多选)。
①F的氢化物比E的氢化物稳定
②常温下F的单质和E的单质状态不同
③一定条件下F和E的单质都能与氢氧化钠溶液反应
④F的氧化物的水化物的酸性比E的氧化物的水化物的酸性强
⑤F可以把E从其氢化物水溶液中置换出来
(5)元素E的一种氧化物通入氯化钡溶液无沉淀,通入硝酸钡溶液却会产生白色沉淀,写出少量该氧化物通入硝酸钡溶液的离子方程式___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com