
分析 稀硝酸质量增加的部分为氨气和部分二氧化氮,设出氨气和二氧化氮的物质的量,根据质量关系列出方程式①;最终气体为氮气和NO,利用体积关系列出方程式②,然后联立①②即可得出氨气和二氧化氮的物质的量,再根据V=nVm计算出氨气和二氧化氮的体积,最后得出氮气的体积.
解答 解:稀硝酸吸收氨气和NO2,同时放出NO气体,
设NH3为xmol,NO2为y mol,则生成$\frac{y}{3}$molNO,
则溶液增加的质量为:①17x+46y-30×$\frac{y}{3}$=12.5g,
根据氮气的体积可知:②10-22.4(x+y)=3.28-22.4×$\frac{y}{3}$,
联立①②解得:x=0.1 mol、y=0.3 mol,
所以混合体中NO2体积为:22.4L/mol×0.3mol=6.72L,NH3体积为:22.4L/mol×0.1mol=2.24L,N2体积为:10L-6.72L-2.24L=1.04L,
答:混合气体中NO2为6.72L、NH3为2.24L、N2为1.04L.
点评 本题考查了混合物反应的计算,题目难度中等,明确发生反应原理为解答关键,注意掌握质量守恒定律在化学计算中的应用,试题充分考查学生的分析能力及化学计算能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,11.2 L二氧化硫中所含的氧原子数等于NA | |
| B. | 标准状况下,80 g SO3中含3NA个氧原子,体积约为22.4 L | |
| C. | 标准状况下,足量Zn与一定量的浓硫酸反应,产生22.4 L气体时,转移的电子数一定为2NA | |
| D. | 对于气态物质,体积的大小主要是由分子间距离决定的 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题

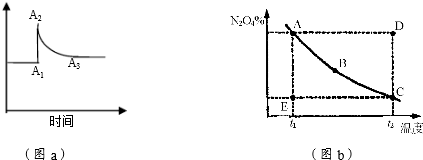
| A. | 图①是pH=13的NaOH溶液中加水稀释 | |
| B. | 图②是用适量的KClO3和MnO2混合物加热制O2 | |
| C. | 图③是向一定量的稀盐酸和氯化钙的混合溶液中不断滴入碳酸钠溶液至过量 | |
| D. | 图④向一定质量的稀盐酸中加入铁粉至过量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | X | Y | Z | W | R |
| 相 关 信 息 | 能形成+7价的化合物 | 日常生活中常见的金属,熔化时并不滴落,好像有一层膜兜着 | 通常状况下能形成短周期中最稳定的双原子分子,它是空气的主要成分之一 | 焰色反应为黄色 | 位于第ⅣA族,是形成化合物种类最多的元素 |


查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷 | B. | 乙烷 | C. | 丙烷 | D. | 丁烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com