
2013年2月朝鲜进行了第三次核试验,引起国际社会的极大关注。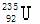 是一种重要的核燃料,这里的“235”是指该原子的 ( )
是一种重要的核燃料,这里的“235”是指该原子的 ( )
A.质量数 B.质子数 C.中子数 D.电子数
科目:高中化学 来源: 题型:
卤素单质及其化合物在生产和生活中有广泛应用。
Ⅰ、氟化钠主要用作农作物杀菌剂、杀虫剂、木材防腐剂。实验室以氟硅酸(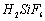 )等物质为原料、通过下图所示的流程制取较纯净的氟化钠,并得到副产品氯化铵:
)等物质为原料、通过下图所示的流程制取较纯净的氟化钠,并得到副产品氯化铵:
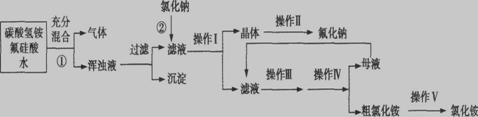
已知:20℃时氯化铵的溶解度为37.2 g,氟化钠的溶解度为4 g,Na2SiF6微溶于水。
请回答下列有关问题:
(1)完成并配平上述流程中①、②的化学反应方程式:

② 。
(2)操作Ⅲ分为两步,其顺序是 (填写所选序号)。
a、过滤 b、加热浓缩 c、冷却结晶 d、洗涤
操作Ⅱ是洗涤、干燥,其目的是 ,在操作Ⅰ~V中与之相同的操作步
骤是 。
(3)流程①中NH4HCO3必须过量,其原因是 。
Ⅱ、紫菜与海带类似,是一种富含生物碘的海洋植物,可用于食用补碘。以下为某兴趣小组模拟从紫菜中提取碘的过程:
 已知:商品紫菜轻薄松脆,比海带更易被焙烧成灰(此时碘转化为碘化物无机盐)。
已知:商品紫菜轻薄松脆,比海带更易被焙烧成灰(此时碘转化为碘化物无机盐)。
(4)将焙烧所得的紫菜灰与足量的双氧水和稀硫酸作用,写出反应的离子方程式:
。
(5)操作①中涉及两步操作,名称是 ,所用的主要玻璃仪器为 ,所用试剂A最好选用表格中的 (填试剂名称)。
| 乙醇 | 四氯化碳 | 裂化汽油 | 碘(晶体) | |
| 密度/g、cm-3 | 0.7893 | 1.595 | 0.71~0.76 | 4.94 |
| 沸点/℃ | 78.5 | 76.8 | 25~232 | 184.35 |
(6)将下列装置图中缺少的必要仪器补画出来,以最终将单质碘与试剂A分离:

查看答案和解析>>
科目:高中化学 来源: 题型:
在密闭容器中发生反应:aA(g)cC(g)+dD(g),达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡浓度的1.8倍。下列叙述正确的是( )
A.A的转化率变大 B.平衡向正反应方向移动
C.D的体积分数变大 D.a<c+d
查看答案和解析>>
科目:高中化学 来源: 题型:
化工生产中常用MnS作沉淀剂除去工业废水中的Cu2+:
Cu2+(aq)+MnS(s)  CuS(s)+Mn2+(aq),下列说法错误的是( )
CuS(s)+Mn2+(aq),下列说法错误的是( )
A.MnS的Ksp比CuS的Ksp大
B.该反应达到平衡时:c(Mn2+)/c(Cu2+) =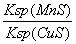
C.往平衡体系中加入少量CuSO4固体后,c(Mn2+)变大
D.MnS(s)的浊液中加入少量可溶性MnSO4固体后, c(S2-)变大
查看答案和解析>>
科目:高中化学 来源: 题型:
已知,在450℃并有催化剂存在下进行如下反应:
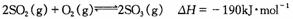
(1)硫酸工业中,该反应需要通入过量空气的目的是 ;该反应不在更高温度下进行的原因是 。
(2)在容积固定的密闭容器中,下列情况已达到平衡状态的是 。
A.v(O2)正=2v(SO3)逆 B.容器中气体的压强不随时间而变化
C.容器中气体的密度不随时间而变化 D.容器中气体的原子总数不随时间而变化
(3)当向上述平衡体系中通入18O2气体,再次达到平衡时,18O存在于 中。
A. SO2、O2 B.SO2、SO3 C.SO3 D.SO2、SO3、O2
(4)在一个固定容积为2L的密闭容器中充入0.20 mol SO2和0.10mol O2,在450℃并有催化剂条件下,2分钟后达到平衡,测得容器中含SO30.16mol,则
v(O2)= mol( L·min-1);放出的热量为 kJ;该温度下的平衡常数为 ;若继续通入0.20mol SO2和0.10mol O2,则再次平衡时,二氧化硫的转化率 (选填“变大”或“变小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
配制一定物质的量浓度的NaOH溶液时,造成所配溶液浓度偏低的原因是( )
A.定容时俯视液面 B.转移溶液前溶液未冷却至室温
C.容量瓶未干燥 D.未洗涤烧杯和玻璃棒
查看答案和解析>>
科目:高中化学 来源: 题型:
已知某300ml MgCl2 与AlCl3的混合液,若往其中滴加NaOH溶液,要使沉淀达到最大值,需消耗0.5mol/L的NaOH溶液600ml;则混合液中c(Cl-)是( )
A.0.6 mol/L B.0.8 mol/L C.1.0 mol/L D.1.2 mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com