
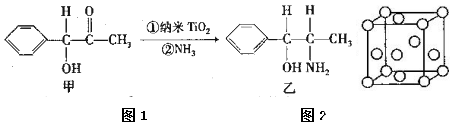
���� ��1��������22��Ԫ�أ�Ti2+������20�����ӣ�
��BH4-��Bԭ�Ӽ۲���Ӷ�=4+$\frac{1}{2}$��3+1-4��1��=4����ϼ۲���ӶԻ�������ȷ���ռ乹�ͣ�
���ѵ�3d�������δ�ɶԵ�����Ϊ2����λ�ڵ������ڣ���ͬһ�����������Ni��3d�������8�����Ӽ���2��δ�ɶԣ�Ge��4p�������2�����Ӽ���2��δ�ɶԣ�Se��4p�������4�����Ӽ���2��δ�ɶԣ�
��2���ٸ���̼ԭ����ɵĿռ乹�ͺͳɼ�������ȷ�����ӻ���ʽ���ж���sp3�ӻ���ԭ�ӣ��ٸ��ݵ�һ�����ܵĵݱ�����ж����һ�����ܵĴ�С��
�ڵȵ�������ԭ�Ӹ�����ȼ۵�������ȣ�
��3����ÿ���ѵľ����к�����ԭ����Ϊ8��$\frac{1}{8}$+$6��\frac{1}{2}$=4���辧��������Ϊa������$��=\frac{m}{V}$����þ�����������ټ���þ����ı߳���
��� �⣺��1��������22��Ԫ�أ�Ti2+������20�����ӣ����ݹ���ԭ��֪���̬��������Ų�ʽΪ��1s22s22p63s23p63d2��
�ʴ�Ϊ��1s22s22p63s23p63d2��
��BH4-��Bԭ�Ӽ۲���Ӷ�=4+$\frac{1}{2}$��3+1-4��1��=4����û�йµ��Ӷԣ���������������ṹ��
�ʴ�Ϊ���������壻
���ѵ�3d�������δ�ɶԵ�����Ϊ2����λ�ڵ������ڣ���ͬһ�����������Ni��3d�������8�����Ӽ���2��δ�ɶԣ�Ge��4p�������2�����Ӽ���2��δ�ɶԣ�Se��4p�������4�����Ӽ���2��δ�ɶԣ�����δ�ɶԵ�����������ͬ��Ԫ����Ni��Ge��Se����3�֣�
�ʴ�Ϊ��3��
��2���ٻ�������б���C���ʻ�C��sp2�ӻ�����7��C����sp3�ӻ���ʽ��ԭ����O��N��C������Nԭ��2p������������һ�����ܸ���O��
�ʴ�Ϊ��7��C��O��N��
��CNO-�к���3��ԭ�ӣ�16���۵��ӣ�������ȵ������з���Ϊ��CO2����N2O��CS2��BeCl2�ȣ�������Ϊ��SCN-��N3-���ȣ�
�ʴ�Ϊ��CO2����N2O��CS2��BeCl2�ȣ���SCN-��N3-����
��3����ÿ���ѵľ����к�����ԭ����Ϊ8��$\frac{1}{8}$+$6��\frac{1}{2}$=4���辧��������Ϊa������$��=\frac{m}{V}$�У�$��=\frac{\frac{4��48}{{N}_{A}}}{{a}^{3}}$������a=$\root{3}{\frac{4��48}{��{N}_{A}}}$cm=$\root{3}{\frac{192}{{N}_{A}��}}$cm��
�ʴ�Ϊ��$\root{3}{\frac{192}{{N}_{A}��}}$��
���� �����ۺϿ������ʽṹ�����ʣ�Ϊ�߿��������ͺ�Ƶ���㣬�漰��������Ų����ȵ����塢�ӻ���ʽ���жϡ��ռ乹�͵��жϡ������ļ����֪ʶ�㣬���ؿ���ѧ���ķ����������������ѵ��Ǿ����ļ��㣬������ù�ʽ�ǽⱾ��ؼ����Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ʵ����������� | ʵ����� | |
| A | ����ij��Һ���Ƿ���SO42-ʱ������Һ�еμ����� ���ữ��BaCl2��Һ���а�ɫ�������� | ����Һ��һ������SO42- |
| B | �������������Ĺܵ��Ƿ���й©ʱ����һ��������պȡŨ��ˮ��Ȼ���ܵ� | �а�ɫ��������ʱ˵���ܵ�����й© |
| C | ����FeCl3��Һ���Ƿ���Fe2+ʱ������Һ�еμ� ����KMnO4��Һ����Һ��Ϊ��ɫ | ����Һ��һ������Fe2+ |
| D | ��2mL0.1mol•L-1 ��������Һ�м��뼸��0.1mol•L-1NaCl��Һ�����ְ�ɫ�������ټ��뼸��0.1mol•L-1Na2S��Һ���к�ɫ�������� | ������˵����ͬ�¶���Ksp��Ag2S����Ksp��AgCl�� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | 1 mol��˾ƥ����������5 molH2 | |
| B�� | ˮ�������������ԭ�ӿ��ܹ��� | |
| C�� | ˮ������Է���ȡ�����ӳɡ��������Ӿ۷�Ӧ | |
| D�� | 1 mol��˾ƥ����������2 molNaOH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1L0.1mol•L-1�ľƾ���Һ�к���ԭ����Ϊ0.6NA | |
| B�� | ���³�ѹ�£�1L1L0.1mol•L-1�Ĵ������Һ�к���ԭ����ĿΪ0.1NA | |
| C�� | 1mol�л���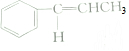 �к���5NA��̼̼˫�� �к���5NA��̼̼˫�� | |
| D�� | 1mol����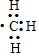 �������ĵ�����Ϊ7NA �������ĵ�����Ϊ7NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
| ��� | �� | �� | �� | �� |
| װ�� | 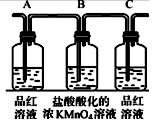 |  |  | 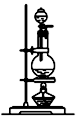 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
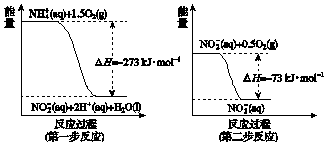
 ��NaOH��Ba��OH��2��NaAlO2��1mol�Ļ����Һ�У�����ͨ��CO2���壬��������������ͨ��CO2����ͼ���ϵ��ͼ��ʾ������˵��������ǣ�������
��NaOH��Ba��OH��2��NaAlO2��1mol�Ļ����Һ�У�����ͨ��CO2���壬��������������ͨ��CO2����ͼ���ϵ��ͼ��ʾ������˵��������ǣ�������| A�� | a���Ӧ����Һ�У�Na+��Fe3+��SO42-��HCO3-�ܴ������� | |
| B�� | c��d�����Ӧ����Һ�У�������������� | |
| C�� | d���Ӧ����Һ�У�c��Na+����c��HCO3-����c��OH-����c��H+�� | |
| D�� | d����e��Աȣ�e����Һ�ĵ�������ǿ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
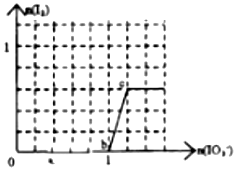 ��֪����ԭ��HSO3-��I-��������IO3-��I2���ں�3mol NaHSO3����Һ����μ���KIO3��Һ������KIO3������I2�����ʵ����Ĺ�ϵ������ͼ��ʾ������˵������ȷ���ǣ�������
��֪����ԭ��HSO3-��I-��������IO3-��I2���ں�3mol NaHSO3����Һ����μ���KIO3��Һ������KIO3������I2�����ʵ����Ĺ�ϵ������ͼ��ʾ������˵������ȷ���ǣ�������| A�� | 0��a�䷢����Ӧ��3HSO3-+IO3-�T3SO42-+I-+3H+ | |
| B�� | a��b�乲����NaHSO3�����ʵ���Ϊ1.8mol | |
| C�� | b��c�䷴Ӧ��I2������������ | |
| D�� | ����Һ��I-��I2�����ʵ���֮��Ϊ5��3ʱ�������KIO3Ϊ1.1mol |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com