
| A. | b为铅蓄电池的正极 | |
| B. | 电解过程中,阳极区溶液中c(H+)逐渐减小 | |
| C. | 阴极反应式:2CO2+12H++12e-═C2H4+4H2O | |
| D. | 每生成1mol乙烯,理论上铅蓄电池中消耗12mol硫酸 |
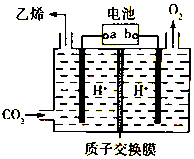
分析 A.根据图知,右侧电极上OH-放电生成O2,则右侧电极为阳极,左侧电极为阴极,连接电解池阴极的电极为原电池负极、连接电解池阳极的电极为原电池正极;
B.电解过程中阳极反应式为2H2O-4e-=O2↑+4H+,阳极附近有H+生成;
C.阴极上二氧化碳得电子和氢离子反应生成乙烯和水;
D.阴极反应式为2CO2+12H++12e-═C2H4+4H2O,铅蓄电池反应式为Pb+PbO2+2H2SO4 ═2PbSO4+2H2O,串联电路中转移电子相等,据此计算消耗硫酸物质的量.
解答 解:A.根据图知,右侧电极上OH-放电生成O2,则右侧电极为阳极,左侧电极为阴极,连接电解池阴极的电极为原电池负极、连接电解池阳极的电极为原电池正极,所以a为负极、b为正极,故A正确;
B.电解过程中阳极反应式为2H2O-4e-=O2↑+4H+,阳极附近有H+生成,所以电解过程中,阳极区溶液中c(H+)逐渐增大,故B错误;
C.阴极上二氧化碳得电子和氢离子反应生成乙烯和水,电极反应式为2CO2+12H++12e-═C2H4+4H2O,故C正确;
D.阴极反应式为2CO2+12H++12e-═C2H4+4H2O,铅蓄电池反应式为Pb+PbO2+2H2SO4 ═2PbSO4+2H2O,串联电路中转移电子相等,生成1mol乙烯转移12mol电子,转移2mol电子消耗2mol硫酸,所以当转移12mol电子时消耗12mol硫酸,故D正确;
故选B.
点评 本题考查原电池和电解池原理,为高频考点,明确得失电子与电解池阴阳极的关系是解本题关键,知道各个电极上电极反应式如何书写,题目难度不大.


 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:选择题
| A. | 锌是负极,发生还原反应 | |
| B. | O2在正极发生氧化反应 | |
| C. | 工作一段时间后,电解质溶液的碱性会减弱 | |
| D. | 该电池能将化学能全部转化为电能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁粉的能量高于FeS | |
| B. | 铁粉和硫粉的反应常温下不能自发进行 | |
| C. | 该反应是放热反应 | |
| D. | 该反应不会产生污染物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将10%的葡萄糖溶液加入新制氢氧化铜悬浊液中,加热可得到砖红色沉淀 | |
| B. | 苯加入到溴水中,苯和溴发生取代反应而使溴水褪色 | |
| C. | 在洁净的试管中加入1~2 mL AgNO3溶液,再滴加稀氨水,直到AgOH完全沉淀,即制得银氨溶液 | |
| D. | 在空气中灼烧铜丝,待铜丝冷却后伸入乙醇中,反复多次,可以制得乙醛 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
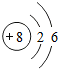 ,b的最简单氢化物的电子式为
,b的最简单氢化物的电子式为 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HBr、CO2、NH3 | B. | Na2O、Na2O2、Na2S | C. | NaCl、HCl、H2O | D. | NaOH、CaCl2 CaO |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com