
| A. | X的结构简式为HCOOCH2CH3 | B. | Y的分子中不含-CH3(甲基) | ||
| C. | Z不具有氧化性 | D. | Z分子中含有甲基且具有还原性 |
分析 C3H6O2水解后得到一元羧酸Y和一元醇Z,结合X分子式可知Y为饱和一元羧酸、Z为饱和一元醇,Y、Z的相对分子质量相等,则Y分子比Z分子少一个碳原子,故Y为HCOOH,Z为CH3CH2OH,X为HCOOCH2CH3.
解答 解:C3H6O2水解后得到一元羧酸Y和一元醇Z,结合X分子式可知Y为饱和一元羧酸、Z为饱和一元醇,Y、Z的相对分子质量相等,则Y分子比Z分子少一个碳原子,故Y为HCOOH,Z为CH3CH2OH,X为HCOOCH2CH3.
A.由上述分析可知,X的结构简式为HCOOCH2CH3,故A正确;
B.Y为HCOOH,分子中没有甲基,故B正确;
C.Z为CH3CH2OH,与钠反应时表现氧化性,故C错误;
D.Z为CH3CH2OH,含有甲基,醇羟基能被氧化,具有还原性,故D正确.
故选:C.
点评 本题考查有机物推断、有机物的结构与性质,C选项以氧化性考查醇与金属的反应,贴近教材又比较新颖.


科目:高中化学 来源: 题型:选择题
| A. | 氯气溶于水:Cl2+H2O═2H++Cl-+ClO- | |
| B. | 硝酸亚铁溶液中滴加少量稀硫酸:Fe2++NO3-+4H+═Fe3++NO↑+2H2O | |
| C. | 把反应Cu+2FeCl3═2FeCl2+CuCl2设计成原电池,其正极反应为Fe3++e-═Fe2+ | |
| D. | 向硫酸氢钠溶液中加入氢氧化钡溶液至中性,则离子方程式为H++SO42-+Ba2++OH-═BaSO4↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
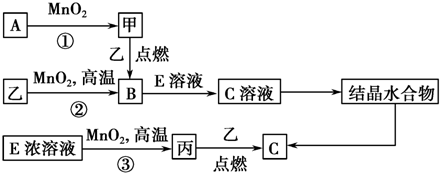
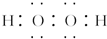 .若反应①需在加热条件下进行,则反应①的化学方程式为2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑.
.若反应①需在加热条件下进行,则反应①的化学方程式为2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将水库的钢闸门与电源负极相连或将锌块焊接于闸门上以防止其生锈 | |
| B. | 用于文物年代鉴定的放射性14C和作为原子量标准的12C,化学性质不同 | |
| C. | 苯酚、甲醛分别可用于环境消毒和鱼肉等食品的防腐保鲜 | |
| D. | NO2和SO2都是酸性氧化物,都是大气污染物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由上述热化学方程式可知d>c | |
| B. | H2的燃烧热为d kJ/mol | |
| C. | CH3OH(g)═CO(g)+2H2(g)△H=(b+2c-a)kJ/mol | |
| D. | 当CO和H2的物质的量之比为1:2时,其完全燃烧生成CO2和H2O(l)时,放出Q kJ热量,则混合气中CO的物质的量为$\frac{Q}{b+2c}$mol |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A | B | C | D | |
| 装置 | 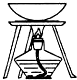 |  |  | 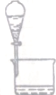 |
| 实验 | 从KI和I2的固体混合物中回收I2 | 分离混合体系中的Fe(OH)3沉淀和胶体 | 蒸干NH4Cl饱和溶液制备NH4Cl晶体 | 分离苯酚和水的混合物 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
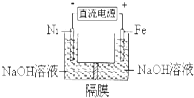
| A. | 铁是阳极,电极反应为Fe-6e-+4H2O═FeO42-+8H+ | |
| B. | 若隔膜为阴离子交换膜,则OH-自左向右移动 | |
| C. | 电解时电子的流动方向为:负极→Ni电极→溶液→Fe电极→正极 | |
| D. | 每制得1mol Na2FeO4,理论上可以产生67.2L气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com