
 短周期元素X、Y、Z.W的原子序数依次增大.在如图所示物质转化关系中,b是Y元素的单质,其余为由上述的两种或三种元素组成的化合物.常温时,0.1mol•L-1的a溶液的pH为1,d为红棕色气体,e为无色气体.下列说法正确的是( )
短周期元素X、Y、Z.W的原子序数依次增大.在如图所示物质转化关系中,b是Y元素的单质,其余为由上述的两种或三种元素组成的化合物.常温时,0.1mol•L-1的a溶液的pH为1,d为红棕色气体,e为无色气体.下列说法正确的是( )| A. | 元素的非金属性:Y>Z>X | |
| B. | 反应①中消耗lmola时转移电子数与反应②中生成1mol a时转移电子数相等 | |
| C. | 原子半径的大小:y<Z<W | |
| D. | Y的氢化物常温常压下为气态 |
分析 0.1mol•L-1的a溶液的pH为1,则a为一元强酸,d为红棕色气体,应为NO2,则a为HNO3,e为无色气体,可知b为浓硝酸反应生成两种气体,则b应为碳,Y为C元素,e为CO2,生成c为H2O,由转化关系可知f为NO,可知X为H元素,Y为C元素,Z为N元素,W为O元素,以此解答该题.
解答 解:由以上分析可知X为H元素,Y为C元素,Z为N元素,W为O元素,为HNO3,b为C,c为H2O,d为NO2,e为CO2,f为NO,
A.Y为C元素,Z为N元素,非金属性N>C,故A错误;
B.反应①为C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O,反应中N元素化合价由+5价降低为+4价,消耗lmolHNO3时转移电子1mol,反应②为3NO2+H2O═2HNO3+NO,反应中N元素化合价由+4价升高为+5价,则生成1mol硝酸转移1mol电子,故B正确;
C.同周期元素从左到右原子半径逐渐减小,故C错误;
D.Y为C元素,对应的氢化物为烃,种类繁多,不一定为气体,当碳原子大于4时,常温下为液体或固体,故D错误.
故选B.
点评 本题考查无机物的推断,为高频考点,把握物质的性质、发生的反应、元素周期律等为解答的关键,侧重分析与推断能力的考查,注意a与d 为推断的突破口,题目难度不大


 金钥匙试卷系列答案
金钥匙试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,35.5g的氯气与足量的氢氧化钙溶液完全反应,转移的电子数为0.5NA | |
| B. | 60g甲酸甲酯和葡萄糖的混合物含有的碳原子数目为2NA | |
| C. | 同温下,pH=1体积为1L的硫酸溶液所含氢离子数与pH=13体积为1L的氢氧化钠所含氢氧根离子数均为0.1NA | |
| D. | 已知合成氨反应N2(g)+3H2(g)?2NH3(g)△H=-92.4KJ/mol,当该反应生成NA个NH3分子时,反应放出的热量为46.2KJ |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

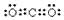
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用惰性电极电解饱和食盐水,若电路中通过NA个电子,则阴极一定产生11.2LCl2 (标况) | |
| B. | lmolCH3COOC2H5在稀硫酸溶液中受热水解可得到乙醇分子数为NA | |
| C. | 含NA个Na+的Na2O2溶解于水配成2L溶液,所得溶液中Na+的物质的量浓度为0.5mol/L | |
| D. | 足量的MnO2固体与1L12mol/L的浓盐酸加热时反应,生成Cl2的分子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 短周期元素W、X、Y、Z、Q的原子序数依次增大,已知A、B、C、D是它们两种或三种元素间形成的化合物,且A、B、C均含有Z元素.A的焰色反应呈黄色,水溶液呈弱碱性;B是两性氢氧化物;D是由W与Q形成的化合物,0.1mol•L-1D溶液的pH为1.在一定条件下它们之间的相互转化关系如图所示.下列说法正确的是( )
短周期元素W、X、Y、Z、Q的原子序数依次增大,已知A、B、C、D是它们两种或三种元素间形成的化合物,且A、B、C均含有Z元素.A的焰色反应呈黄色,水溶液呈弱碱性;B是两性氢氧化物;D是由W与Q形成的化合物,0.1mol•L-1D溶液的pH为1.在一定条件下它们之间的相互转化关系如图所示.下列说法正确的是( )| A. | X、Y、Z元素的离子半径大小是X>Y>Z | |
| B. | X元素的氢化物沸点比同主族元素的氢化物低 | |
| C. | Q形成的单质在化学反应中只体现氧化性 | |
| D. | Q的氧化物对应水化物的酸性在同主族元素中是最强的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 能发生银镜发应 | |
| B. | 分子式为C10H10NO2 | |
| C. | 1mol 该物质最多可与5mol H2反应 | |
| D. | 吲哚-3-乙酸可发生加成反应和取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.2molH2O和D2O形成的混合物中,含有中子的数目为2NA | |
| B. | 含有0.1molNH4+的氨水中,含有OH-的数目为0.1NA | |
| C. | 400mL1mol•L-1稀硝酸与Fe完全反应(还原产物只有NO),转移电子的数目为0.3NA | |
| D. | 30g乙酸和乙酸乙酯的混合物完全燃烧,消耗O2的分子数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向某溶液中加入2滴KSCN溶液,溶液不显红色,再向溶液中加入几滴新制的氯水,溶液变为红色,该溶液中一定含有Fe2+ | |
| B. | 为检验红砖中铁的价态,向红砖粉末中加入盐酸,充分反应后取上层清液于试管中,滴加KSCN溶液2~3滴,溶液变为红色,说明红砖中只有三氧化二铁 | |
| C. | 制备氢氧化亚铁时,向硫酸亚铁溶液中滴加氢氧化钠溶液,边加边搅拌,即可制得白色的氢氧化亚铁 | |
| D. | 将(NH4)2Fe(SO4)2•6H2O试样溶于稀硝酸中,滴加KSCN溶液,出现血红色,说明检验前该试样已变质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 阴阳离子间通过静电吸引形成的化学键叫做离子键 | |
| B. | HF,HCl,HBr,HI的热稳定性依次增强 | |
| C. | 元素非金属越强,其对应含氧酸的酸性就越强 | |
| D. | 元素周期律是元素原子核外电子排布周期性变化的结果 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com