
����(1100�棩�����ܱ������з�����Ӧ��Na2SO4(s��+4H2(g��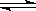 Na2S(s��+4H2O(g��������˵����ȷ����( ��
Na2S(s��+4H2O(g��������˵����ȷ����( ��
A���÷�Ӧ��ƽ�ⳣ������ʽK=c(H2O��/c(H2��
B����������������ܶȻ�ѹǿ���ֲ��䣬��˵���÷�Ӧ�Ѵﵽƽ��״̬
C����Na2SO4�������ı���ʼ����H2��Ũ�ȣ���ƽ��ʱH2��ת���ʲ���
D������ʼʱͶ��2.84gNa2SO4��һ����H2����Ӧ��ƽ��ʱ�����ڹ��干��2.264g����Na2SO4��ת����Ϊ50%
 ���Ž�������С״Ԫϵ�д�
���Ž�������С״Ԫϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ɫ��Һ��Cu2+��H+��Cl-��HSO${\;}_{3}^{-}$ | |
| B�� | �μ�ʯ����Һ�Ժ�ɫ����Һ��Na+��NH${\;}_{4}^{+}$��Fe2+��NO${\;}_{3}^{-}$ | |
| C�� | Na2CO3��Һ��K+��Fe3+��SO${\;}_{4}^{2-}$��NO${\;}_{3}^{-}$ | |
| D�� | pH=12����Һ��Na+��K+��SiO${\;}_{3}^{2-}$��NO${\;}_{3}^{-}$ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | c=$\frac{1000W}{aV}$mol/L | B�� | c��Cl-��=$\frac{10dW}{a}$mol/L | C�� | ��%=$\frac{100W}{dV}$% | D�� | S=$\frac{100W}{dV-W}$ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ������������������ѧУ�߶��ο�һ��ѧ���������棩 ���ͣ������
��һ���¶��£���һ�̶��ݻ����ܱ������м��� 1mol A�� 2mol B������������Ӧ��A(g��+2B(g�� 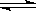 3C(g��+2D(s�� ��H>0���ﵽƽ��ʱ����
3C(g��+2D(s�� ��H>0���ﵽƽ��ʱ���� ��1.8 mol C��
��1.8 mol C��
��1������ͬ�����£�����������и�Ϊ����0.3mol A��0.6 mol B��Ҫʹƽ����������C���ʵ����������ԭƽ�����ͬ����D����ʱ����Ӧ���� mol������C��
��2����ά��������������¶Ȳ��䣬��Ӧ���淴Ӧ����ʼ������ͬ�������Ϊ��ʼ���ʣ��ﵽƽ��ʱC��Ϊ1.8 mol ����D����ʼ���ʵ���n(D��Ӧ����������ǣ�n(D��___________��
���ı��¶Ȼ�ѹǿʱ���п��ܸı����ʵľۼ�״̬����ƽ�����Ӱ�졣�ش�3����4��
��3��������ƽ����ϵ�¶ȣ����ٴδﵽƽ��������ƽ�������»�������ƽ����Է�������δ�����ı䣬�Խ����γ����ֽ���Ŀ���ԭ���ǣ�_________________��
��4������������Ϊ�ݻ��ɱ����������һ���¶Ⱥͳ�ѹ�£���������ƽ��֮��A�����ʵ���Ũ��Ϊa mol/L���ֳ�������ѹǿ������
�ٵ�ѹǿΪԭ��1.5��ʱ��A��ƽ��ʱ���ʵ���Ũ��Ϊm mol/L�����m=1.5a��
�ڵ�ѹǿΪԭ��10��ʱ��A��ƽ��ʱ���ʵ���Ũ��Ϊn mol/L�����n >10 a��
�۵�ѹǿΪԭ��100��ʱ��A��ƽ��ʱ���ʵ���Ũ��Ϊp mol/L�����p<100a��
�Խ����γ����ֽ���Ŀ��ܵ�ԭ��
��1.5��ʱ�� ��
��10��ʱ�� ��
��100��ʱ��  ��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ������������������ѧУ�߶��ο�һ��ѧ���������棩 ���ͣ�ѡ����
����ʱ������������ȷ����
A��ϡ��pH=3�Ĵ��ᣬ��Һ���������ӵ�Ũ�Ⱦ�����
B��һ��Ũ�ȵ�CH3COOH��NaOH��ϣ���Һ�����ԣ�����Һ��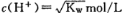
C��pH��Ϊ11��NaOH��NH3��H2O��Һ�У�ˮ�ĵ���̶Ȳ���ͬ
D���ֱ��к�pH���������ͬ������ʹ��ᣬ���������������Ƶ����ʵ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ������������������ѧУ�߶��ο�һ��ѧ���������棩 ���ͣ�ѡ����
��0.1mol•L��1��KI��Һ��0.05mol•L��1 Fe2(SO4��3��Һ�������Ϻ�ȡ���Һ�ֱ��������ʵ�飬��˵����Һ�д��ڻ�ѧƽ�⡰2Fe3++2I�� 2Fe2++I2������( ��
2Fe2++I2������( ��
ʵ���� | ʵ����� | ʵ������ |
�� | ����KSCN��Һ | ��Һ���ɫ |
�� | ����AgNO3��Һ | �л�ɫ�������� |
�� | ����K3[Fe(CN��6]��Һ | ����ɫ��������(����֤��Fe2+���ڣ� |
�� | ���������Һ | ��Һ����ɫ |
A���ٺ͢� B���ں͢� C���ں͢� D���ٺ͢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
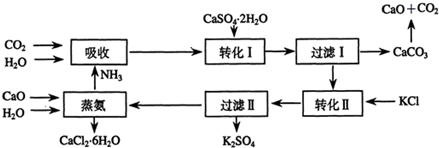
| �������� | ���鷽�� |
| K+ | ȡ������Һ���Թ��У�ͨ����ɫ��Ӧ���������ɫ������ɫ�ܲ����� |
| NH4+ | ȡ������Һ���Թ��У��������м���NaOH�ȣ��д̼�����ζ�������������ʹʪ���ɫʯ����ֽ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ͬŨ��������Һ�У��٣�NH4��2SO4 ��NH4HCO3 ��NH4Cl��NH3•H2O��c��NH4+���ɴ�С��˳���ǣ��٣��ۣ��ڣ��� | |
| B�� | ����ʱ���������������Ͱ�ˮ��Ϻ�pH=7����c ��NH4+����c ��Cl-�� | |
| C�� | 0.2 mol•L-1Na2CO3��Һ�У�c ��OH-��=c ��HCO3-��+c ��H+��+c ��H2CO3�� | |
| D�� | 0.01 mol•L-1��NH4Cl��Һ��0.05mol•L-1��NaOH��Һ�������ϣ�c ��Cl-����c ��NH4+����c ��Na+����c ��OH-����c ��H+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���б����ˮ | B�� | ʳ��ˮ | C�� | �ྻ�Ŀ��� | D�� | ������ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com