
| A£® | ³żČ„NaHCO3ČÜŅŗÖŠÉŁĮæµÄNa2CO3£ŗĶØČė¹żĮæµÄCO2 | |
| B£® | ³żČ„MgCl2ČÜŅŗÖŠÉŁĮæµÄAlCl3£ŗ¼ÓČė¹żĮæĒāŃõ»ÆÄĘČÜŅŗ£¬¹żĀĖ£¬ÓĆÕōĮóĖ®Ļ“µÓ³ĮµķŗóÓĆĻ”ŃĪĖįČܽā³Įµķ | |
| C£® | ³żČ„K2CO3¹ĢĢåÖŠÉŁĮæNaHCO3£ŗÖĆÓŚŪįŪöÖŠ¼ÓČČ | |
| D£® | ÓĆŃĪĖį³żČ„AgClÖŠÉŁĮæµÄAg2CO3 |
·ÖĪö A”¢Ģ¼ĖįÄĘŗĶ¶žŃõ»ÆĢ¼”¢Ė®·“Ӧɜ³ÉĢ¼ĖįÄĘ£»
B”¢¼ÓČė¹żĮæĒāŃõ»ÆÄĘČÜŅŗ£¬Al3+Éś³ÉĘ«ĀĮĖįøł£¬¹żĀĖµĆµ½ĒāŃõ»ÆĆ¾³Įµķ£¬¼ÓŃĪĖįČܳĮµķ½ā£¬µĆµ½ĀČ»ÆĆ¾£»
C”¢¼ÓČČNaHCO3Éś³ÉNa2CO3£»
D”¢ŃĪĖįŗĶĢ¼ĖįŅų·“Ӧɜ³ÉĀČ»ÆŅų”¢¶žŃõ»ÆĢ¼ŗĶĖ®£®
½ā“š ½ā£ŗA”¢Ģ¼ĖįÄĘŗĶ¶žŃõ»ÆĢ¼”¢Ė®·“Ӧɜ³ÉĢ¼ĖįÄĘ£¬°ŃŌÓÖŹ×Ŗ»ÆĪŖNaHCO3ČÜŅŗµÄČÜÖŹ£¬¹ŹAÕżČ·£»
B”¢¼ÓČė¹żĮæĒāŃõ»ÆÄĘČÜŅŗ£¬Al3+Éś³ÉĘ«ĀĮĖįøł£¬¹żĀĖµĆµ½ĒāŃõ»ÆĆ¾³Įµķ£¬¼ÓŃĪĖįČܽā³Įµķ£¬µĆµ½ĀČ»ÆĆ¾£¬¹ŹBÕżČ·£»
C”¢¼ÓČČNaHCO3Éś³ÉNa2CO3£¬ČŌČ»ŹĒK2CO3¹ĢĢåµÄŌÓÖŹ£¬¹ŹC“ķĪó£»
D”¢ŃĪĖįŗĶĢ¼ĖįŅų·“Ӧɜ³ÉĀČ»ÆŅų”¢¶žŃõ»ÆĢ¼ŗĶĖ®£¬³żČ„ĮĖĢ¼ĖįŅų£¬¹ŹDÕżČ·£»
¹ŹŃ”C£®
µćĘĄ ±¾Ģāæ¼²éĮĖ³żŌÓ²Ł×÷µÄ»ł±¾ŌŌņ£¬ŅŌ¼°ÄʵÄÖŲŅŖ»ÆŗĻĪļµÄ»ÆѧŠŌÖŹ£¬ÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
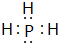 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ŌŖĖŲ | ””””””””””²æ·Ö½į¹¹ÖŖŹ¶ | ””””””””””””””””””””””””””²æ·ÖŠŌÖŹ |
| X | XŌ×ÓŗĖĶāµē×ÓÕ¼ÓŠ9øöŌ×Ó¹ģµĄ | XµÄŅ»ÖÖŃõ»ÆĪļŹĒŠĪ³ÉĖįÓźµÄÖ÷ŅŖĪļÖŹ |
| Y | YŌ×ӵēĪĶā²ćµē×ÓŹżµČÓŚ×īĶā²ćµē×ÓŹżµÄŅ»°ė | YÄÜŠĪ³É¶ąÖÖĘųĢ¬Ēā»ÆĪļ |
| Z | ZŌ×ÓµÄ×īĶā²ćµē×ÓŹż¶ąÓŚ4 | ZŌŖĖŲµÄ×īøßÕż»ÆŗĻ¼ŪÓė×īµĶøŗ»ÆŗĻ¼Ū“śŹżŗĶµČÓŚ6 |
| W | WŌ×ÓµÄ×īĶā²ćµē×ÓŹżµČÓŚ2n-3£ØnĪŖŌ×ÓŗĖĶāµē×Ó²ćŹż£© | »Æѧ·“Ó¦ÖŠWŌ×ÓŅ׏§Č„×īĶā²ćµē×ÓŠĪ³ÉWn+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŌŚ1 mol•L-1µÄKClO3ČÜŅŗÖŠ£¬K+µÄøöŹżĪŖNA | |
| B£® | ŌŚ±ź×¼×“æöĻĀ£¬22.4 L CH3CH2OHµÄ·Ö×ÓŹżĪŖNA | |
| C£® | 32 gŃõĘųŗĶ³ōŃõµÄ»ģŗĶĘųĢåÖŠŗ¬ÓŠµÄŃõŌ×ÓŹżĪŖ2NA | |
| D£® | 22.4 L HClĘųĢåÖŠŗ¬ÓŠµÄ·Ö×ÓŹżĪŖNA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 0.25mol | B£® | 2.5mol | C£® | 0.15mol | D£® | 1.5mol |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | HClŗĶNaOH·“Ó¦µÄÖŠŗĶČČ”÷H=-57.3 kJ/mol£¬ŌņH2SO4ŗĶCa£ØOH£©2·“Ó¦µÄÖŠŗĶČČ”÷H=2”Į£Ø-57.3£©kJ/mol | |
| B£® | CO£Øg£©µÄČ¼ÉÕČČŹĒ283.0 kJ/mol£¬Ōņ2CO2£Øg£©=2CO£Øg£©+O2£Øg£©·“Ó¦µÄ”÷H=+566.0 kJ/mol | |
| C£® | ŠčŅŖ¼ÓČČ²ÅÄÜ·¢ÉśµÄ·“Ó¦Ņ»¶ØŹĒĪüČČ·“Ó¦ | |
| D£® | Ba£ØOH£©2•8H2OÓėNH4Cl·“Ó¦µÄģŹ±äŠ”ÓŚ0£¬ĖłŅŌŌŚ³£ĪĀĻĀÄÜ×Ō·¢½ųŠŠ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
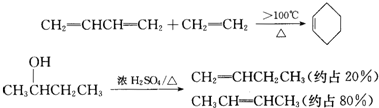

 £»C
£»C £»D
£»D £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | HClĘųĢåČÜÓŚĖ® | B£® | µā¾§ĢåŹÜČČ×Ŗ±ä³ÉµāÕōĘų | ||
| C£® | NaClČÜÓŚĖ® | D£® | ¼ÓČČHIĘųĢåŹ¹Ö®·Ö½ā |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

 £¬BNÖŠBŌŖĖŲµÄ»ÆŗĻ¼ŪĪŖ+3£»
£¬BNÖŠBŌŖĖŲµÄ»ÆŗĻ¼ŪĪŖ+3£» £¬Ę䶞ĀČ“śĪļÓŠ4ÖÖ£®
£¬Ę䶞ĀČ“śĪļÓŠ4ÖÖ£®²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com