
| 元素代号 | X | Y | Z | M | R | Q | |
| 原子半径(×10-10 m) | 1.86 | 0.99 | 1.43 | 1.60 | 0.75 | 0.74 | |
| 主要化 合价 | 最高正价 | +1 | +7 | +3 | +2 | +5 | -- |
| 最低负价 | -- | -1 | -- | -- | -3 | -2 | |
| A. | Y的非金属性大于S,其含氧酸酸性一定强于H2SO4 | |
| B. | 元素X和Q形成的化合物中不可能含有共价键 | |
| C. | X、Z、M的单质分别与水反应,M最剧烈 | |
| D. | X、Z、R的最高价氧化物的水化物之间可两两相互反应 |
分析 X、Y、Z和M均为第三周期元素.由化合价关系可知X为Na元素,Y为Cl元素,Z为Al元素,M为Mg元素,Q只有-2价,应为O元素,R有+5价,且原子半径与O相近,应为N元素,结合对应单质、化合物的性质以及元素周期率解答该题.
解答 解:X、Y、Z和M均为第三周期元素.由化合价关系可知X为Na元素,Y为Cl元素,Z为Al元素,M为Mg元素,Q只有-2价,应为O元素,R有+5价,且原子半径与O相近,应为N元素,
A.Y的非金属性大于S,如不是最高价含氧酸,则酸性不一定比硫酸强,如HClO为弱酸,故A错误;
B.如O和Na形成Na2O2,则含有共价键,故B错误;
C.Na的金属性最强,与水反应最剧烈,故C错误;
D.Z为Al,对应的氢氧化铝为两性氢氧化物,含有强碱、强酸反应,故D正确.
故选D.
点评 本题考查元素位置结构和性质的关系及应用,从原子半径的变化和元素的最高正价和最低负价入手寻求突破,正确把握元素化合价、原子半径与元素性质的关系是解答该题的关键,题目难度中等.


 同步奥数系列答案
同步奥数系列答案科目:高中化学 来源: 题型:选择题
| A. | ⅡA族元素 | |
| B. | 可能是金属元素,也可能是非金属元素 | |
| C. | 金属元素 | |
| D. | ⅡA族或ⅡB族元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
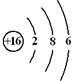 ,电子式表示化合物 C2D 的形成过程
,电子式表示化合物 C2D 的形成过程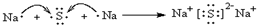 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①中有机物均可以发生还原反应 | |
| B. | ②中有机物可用饱和Na2CO3溶液鉴别 | |
| C. | ③中有机物均可以发生水解反应 | |
| D. | ③中有机物均属于高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba2+、K+、Cl-、SO32- | B. | Na+、SiO32-、AlO2-、SO42- | ||
| C. | Na+、K+、HCO3-、S2- | D. | K+、NH4+、Fe3+、I- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
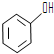 和
和 ,应选用a(填字母).
,应选用a(填字母).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2的结构式为O=C=O | B. | 乙烯的结构简式是C2H4 | ||
| C. | NaCl的电子式是Na:Cl: | D. | S原子的结构示意图: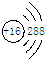 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com