
| 选项 | 甲 | 乙 |
| A | 电解质 | BaSO4、NaHSO4、SO3 |
| B | 弱电解质的电离 | 均分步电离 |
| C | 化学平衡影响因素 | 温度、压强、浓度、催化剂等 |
| D | 化学电源 | 一次电池、二次电池、燃料电池等 |
| A. | A | B. | B | C. | C | D. | D |
科目:高中化学 来源: 题型:解答题
 用下列仪器、药品验证由铜和适量浓硝酸反应产生的气体中含NO(仪器可选择使用,N2和O2的用量可自由控制).
用下列仪器、药品验证由铜和适量浓硝酸反应产生的气体中含NO(仪器可选择使用,N2和O2的用量可自由控制).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
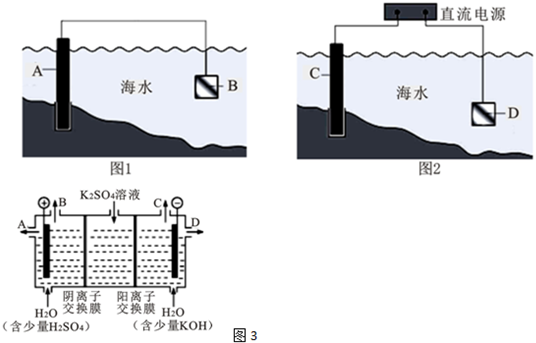
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
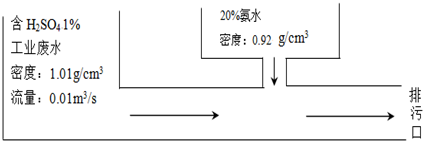
| A. | 1.98×10-3m3/s | B. | 5.49×10-4m3/s | C. | 1.90×10-4 m3/s | D. | 9.52×10-5 m3/s |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 7.8 g苯含有碳碳双键的数目为0.3NA | |
| B. | 标准状况下,足量的Fe与2.24 L Cl2反应转移电子的数目为0.3NA | |
| C. | 273K、101kPa下,28 g乙烯与丙烯混合物中含有C-H键的数目为5NA | |
| D. | 100 mL1mol•L-1的NaF中:N(F-)+N(HF)=0.1 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K2SO4固体 | B. | H2O | C. | 少量CuSO4溶液 | D. | 4 mol/L H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu2+、H+、Cl- | B. | CO32-、OH-、Cl- | C. | K+、H+、Cl- | D. | K+、CO32-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 酚酞呈无色的溶液中:K+、Al3+、Cl-、HCO3- | |
| B. | 使pH试纸变深蓝色的溶液中:ClO-、Na+、AlO2-、SO42- | |
| C. | 甲基橙呈红色的溶液中:NH4+、I-、Fe2+、SO42- | |
| D. | 加入铝粉产生氢气的溶液:Na+、SO42-、Mg2+、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 与新制氢氧化铜反应 | |
| B. | 使溴的四氯化碳溶液褪色 | |
| C. | 与乙醇在浓硫酸催化下发生酯化反应 | |
| D. | 与银氨溶液反应析出银 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com