
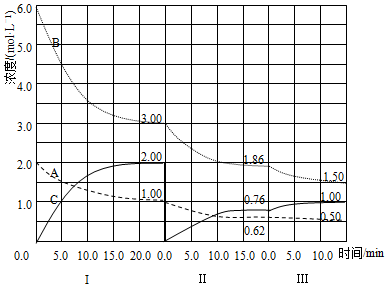
���� ��1����ͼ��֪�ڢ�Σ�ƽ��ʱ��c��A��=2mol/L-1mol/L=1mol/L����c��B��=6mol/L-3mol/L=3mol/L����c��C��=2mol/L������Ũ�ȱ仯��֮�ȵ��ڻ�ѧ������֮�ȼ��㣻
��2���ڢ��C�Ǵ�0��ʼ�ģ�˲��A��BŨ�Ȳ��䣬��˿���ȷ����һ��ƽ������ϵ���Ƴ���C��������������Ũ�ȣ�ƽ�������ƶ���
��3���ڢ�εĿ�ʼ��ڢ�ε�ƽ������ʵ�������ȣ�����A��B�������٣�C�������ӿ��ж�ƽ���������ƶ��ģ�����ƽ�ʼʱŨ��ȷ����ƽ���ƶ�����������Ũ�ȵı仯����ģ�������Ŀ��������������������䣬��ı�ѹǿҲ�����ܣ����һ��Ϊ�¶ȵ�Ӱ�죬�˷�Ӧ����Ϊ���ȷ�Ӧ�������Ʋ�Ϊ�����¶ȣ�������A�������������ε������ȷ���ı������һ��Ϊ�����¶ȣ�������������ԭ����ƽ����ƶ�ֻ�ܼ����ı䣬���ܵ����ı䣬��˴ﵽƽ����¶�һ���ȵڢ��ƽ��ʱ���¶ȵͣ�
��4��������ƽ��ʱ��A��ƽ�����ʵ���Ϊ0.50mol/L��B��ƽ�����ʵ���Ϊ1.50mol��C�����ʵ���Ϊ1.00mol/L������ƽ�ⳣ���ļ��㹫ʽ����ƽ�ⳣ������ʽ��
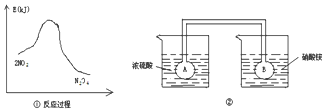
��5����ͼ�ٿ�֪����������ת��Ϊ�����������ķ�ӦΪ���ȷ�Ӧ��ͼ���У�Ũ�����ܽ���ˮ�¶����ߣ���������ܽ���ˮ��Һ�¶Ƚ��ͣ����Ҳ��ձ����¶ȵ�����࣬�����¶�ʹ2NO2������ɫ��?N2O4����ɫ����H��0�����淴Ӧ�����ƶ���
��� �⣺��1����ͼ��֪�ڢ�Σ�ƽ��ʱ��c��A��=2mol/L-1mol/L=1mol/L����c��B��=6mol/L-3mol/L=3mol/L����c��C��=2mol/L��Ũ�ȱ仯��֮�ȵ��ڻ�ѧ������֮�ȣ���a��b��c=1mol/L��3mol/L��2mol/L=1��3��2��
�ʴ�Ϊ��1��3��2��
��2���ڢ��C�Ǵ�0��ʼ�ģ�˲��A��BŨ�Ȳ��䣬��˿���ȷ����һ��ƽ������ϵ���Ƴ���C��������������Ũ�ȣ�ƽ�������ƶ���
�ʴ�Ϊ��ƽ�������ƶ����ӷ�Ӧ��ϵ���Ƴ�����C��
��3���ڢ�εĿ�ʼ��ڢ�ε�ƽ������ʵ�������ȣ�����A��B�������٣�C�������ӿ��ж�ƽ���������ƶ��ģ�����ƽ�ʼʱŨ��ȷ����ƽ���ƶ�����������Ũ�ȵı仯����ģ�������Ŀ��������������������䣬��ı�ѹǿҲ�����ܣ����һ��Ϊ�¶ȵ�Ӱ�죬�˷�Ӧ����Ϊ���ȷ�Ӧ�������Ʋ�Ϊ�����¶ȣ�������A�������������ε������ȷ���ı������һ��Ϊ�����¶ȣ�������������ԭ����ƽ����ƶ�ֻ�ܼ����ı䣬���ܵ����ı䣬��˴ﵽƽ����¶�һ���ȵڢ��ƽ��ʱ���¶ȵͣ�
�ʴ�Ϊ�������˷�ӦΪ���ȷ�Ӧ�������¶ȣ�ƽ��������Ӧ�����ƶ���
��4�����淴ӦA+3B?2C�����δﵽƽ��ʱA��ƽ��Ũ��Ϊ0.25mol/L��B��ƽ��Ũ��Ϊ0.75mol/L��C��ƽ��Ũ��Ϊ0.50mol/L����ʱK=$\frac{{0.5mol/L}^{2}}{0.25mol/L����0.75mol��^{3}}$���ʴ�Ϊ��$\frac{{0.5mol/L}^{2}}{0.25mol/L����0.75mol��^{3}}$��
��5����ͼ�ٿ�֪��2mol������������������1mol�������������������ʶ�������ת��Ϊ�����������ķ�ӦΪ���ȷ�Ӧ����ͼ���У���Ũ�����ܽ���ˮ��Һ�¶����ߣ�������ܽ���ˮ��Һ�¶Ƚ��ͣ�����ձ����¶ȸ����Ҳ࣬�����¶�ʹ2NO2������ɫ��?N2O4����ɫ����H��0�����淴Ӧ�����ƶ�����������NO2�ƶ�����Bƿ��ɫ��dz��
�ʴ�Ϊ��dz��2NO?N2O4��H��0��Aƿ���ȣ�ƽ��������ɫ���Bƿ�����¶ȣ�ƽ��������ɫ��dz��
���� ���⿼�黯ѧ��Ӧ�����뻯ѧƽ��ͼ��ѧƽ���йؼ��㡢��ѧ��Ӧ���ʡ���ѧƽ��Ӱ�����ؼ���ѧ��Ӧ�������仯�ȣ�ע���������������Ϣ���ݣ������Ѷ��еȣ�


 Ӧ����㲦ϵ�д�
Ӧ����㲦ϵ�д� ״Ԫ����ϵ�д�
״Ԫ����ϵ�д� ͬ������ϵ�д�
ͬ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 �Ӻ�������ȡ���ʵ⼰��Ļ�������ת����ϵ��ͼ��ʾ��
�Ӻ�������ȡ���ʵ⼰��Ļ�������ת����ϵ��ͼ��ʾ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
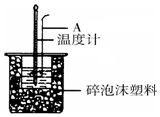 50mL 0.50mol/L�����50mL 0.55mol/L NaOH��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ��㷴Ӧ�ȣ�
50mL 0.50mol/L�����50mL 0.55mol/L NaOH��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ��㷴Ӧ�ȣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������Ӧ�У�ˮ�Ȳ���������Ҳ���ǻ�ԭ�� | |
| B�� | ����������Ӧ�У��������ﶼ��H3PO4 | |
| C�� | ��Ӧ��2���У�1mol CuSO4������1/5molP | |
| D�� | ����������Ӧ�У���������ֻ������ͭ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��ѧʽ | CH3COOH | H2C2O4 | H2S |
| ����ƽ�ⳣ�� | 1.8��10-5 | Ka1=5.4��10-2 Ka2=5.4��10-5 | Ka1=1.3��10-7 Ka2=7.1��10-15 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  | B�� |  | ||
| C�� |  | D�� |  |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Ӧ����������ԭ������ͭ����ԭ | |
| B�� | NH4CuSO3����Ԫ�ر����� | |
| C�� | 2mol NH4CuSO3��ȫ��Ӧת��6.02��1023������ | |
| D�� | �̼�����ζ�������ǰ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ᡢ��Ȼ�������ᡢ���ᡢ�ɱ� | |
| B�� | ��ˮ�����������Ȼ��ء�̼�ᡢ�Ҵ� | |
| C�� | ���Ȼ�̼�����ᡢ���ᱵ��������̼������ | |
| D�� | �ơ������������ơ����ᡢ�������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com