
| A. | 4g D2和足量O2反应可生成D2O 2NA个 | |
| B. | 98g H3PO4和H2SO4的混合物中含氢原子2.5NA个 | |
| C. | 6.02×1023个葡萄糖分子约含羟基6NA个 | |
| D. | 1molNa完全燃烧可转移电子NA个 |
分析 A、求出4g D2的物质的量,然后根据1mol D2~1molD2O来分析;
B、H3PO4和H2SO4的摩尔质量均为98g/mol,但含有的H原子个数不同;
C、葡萄糖中含有5个-OH;
D、钠燃烧后变为+1价.
解答 解:A、4g D2的物质的量为1mol,而1mol D2~1molD2O,故生成重水1mol,个数为NA个,故A错误;
B、H3PO4和H2SO4的摩尔质量均为98g/mol,故98g混合物的物质的量为1mol,但由于磷酸和硫酸含有的H原子个数不同,且两者在混合物中的比例不明确,故混合物中含有的H原子个数无法计算,故B错误;
C、葡萄糖中含有5个-OH,故6.02×1023个葡萄糖分子约含羟基5NA个,故C错误;
D、钠燃烧后变为+1价,故1mol钠燃烧后失去NA个电子,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
;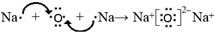 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
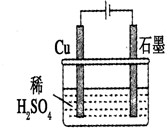
| A. | 石墨是电解池的负极,Cu是电解池的正极 | |
| B. | 电解过程中,铜电极上自身没什么变化 | |
| C. | 电解一定时间后,石墨电极上会有铜析出 | |
| D. | 整个电解过程中,溶液的pH不会变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 混合粉末中物质的量之间一定满足:n(Cu)+n(Fe)=n(Fe2O3) | |
| B. | 混合粉末中物质的量之间一定满足:n(Fe)>n(Cu)>n(Fe2O3) | |
| C. | 混合粉末中物质的量之间一定满足:n(Cu)+n(Fe)═n(Fe2O3)+$\frac{bL}{22.4L•mo{l}^{-1}}$ | |
| D. | 若a=72.50,b=1.12,则20.40g混合粉末中:n(Fe)=n(Cu)=0.05mol、n(Fe2O3)=0.09mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
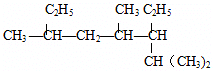 名称:2,4,6-三甲基-3-乙基辛烷
名称:2,4,6-三甲基-3-乙基辛烷 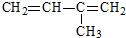 名称:2-甲基-1,3-丁二烯
名称:2-甲基-1,3-丁二烯
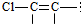 结构的有4种
结构的有4种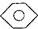 和
和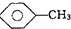 :KMnO4(H+)溶液.
:KMnO4(H+)溶液.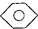 ,
,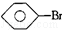 和C6H12(已烯):溴水.
和C6H12(已烯):溴水.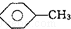 ,CCl4和乙醇:水.
,CCl4和乙醇:水.查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com