
| A£® | 2Na2O2+2H2OØT4NaOH+O2”ü | B£® | 4Fe£ØOH£©2+O2+2H2OØT4Fe£ØOH£©3 | ||
| C£® | Cl2+H2OØTHCl+HClO | D£® | 2Al+2NaOH+2H2OØT2NaAlO2+3H2”ü |
·ÖĪö ·“Ó¦Br2+SO2+2H2O=H2SO4+2HBrÖŠ£¬Ė®¼Č²»ŹĒŃõ»Æ¼ĮŅ²²»ŹĒ»¹Ō¼Į£¬¾Ż“Ė·ÖĪö£®
½ā“š ½ā£ŗA”¢Ė®¼Č²»ŹĒŃõ»Æ¼ĮŅ²²»ŹĒ»¹Ō¼ĮÓėBr2+SO2+2H2O=H2SO4+2HBrÖŠĖ®µÄ×÷ÓĆĻąĶ¬£¬¹ŹA“ķĪó£»
B”¢Ė®¼Č²»ŹĒŃõ»Æ¼ĮŅ²²»ŹĒ»¹Ō¼Į£¬ÓėBr2+SO2+2H2O=H2SO4+2HBrÖŠĖ®µÄ×÷ÓĆĻąĶ¬£¬¹ŹB“ķĪó£»
C”¢Ė®¼Č²»ŹĒŃõ»Æ¼ĮŅ²²»ŹĒ»¹Ō¼Į£¬ÓėBr2+SO2+2H2O=H2SO4+2HBrÖŠĖ®µÄ×÷ÓĆĻąĶ¬£¬¹ŹC“ķĪó£»
D”¢Ė®ŹĒŃõ»Æ¼Į£¬ÓėBr2+SO2+2H2O=H2SO4+2HBrÖŠĖ®µÄ×÷ÓĆ²»ĻąĶ¬£¬¹ŹDÕżČ·£®
¹ŹŃ”D£®
µćĘĄ ±¾Ģāæ¼²éѧɜŃõ»Æ»¹Ō·“Ó¦ÖŠµÄ»ł±¾øÅÄīÖŖŹ¶£¬æÉŅŌøł¾ŻĖłŃ§ÖŖŹ¶½ųŠŠ»Ų“š£¬ÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³£ĪĀĻĀ£¬“×ĖįÄĘÓė“×ĖįµÄ»ģŗĻČÜŅŗpH=7£¬c£ØNa+£©=c£ØCH3COO-£© | |
| B£® | 0.1 mol/L Na2CO3ČÜŅŗÖŠ£ŗc£ØOH-£©=c£ØHCO3-£©+c£ØH+£©+2c£ØH2CO3£© | |
| C£® | ³£ĪĀĻĀ£¬½«pH=1µÄ“×ĖįČÜŅŗĻ”ŹĶ100±¶ŗó£¬Ė®µēĄėµÄc£ØH+£©=10-11mol/L | |
| D£® | 0.1mol/L NaHCO3ČÜŅŗÖŠ£ŗc£ØNa+£©+c£ØH+£©=c£ØHCO3-£©+c£ØOH-£©+2c£ØCO32-£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ·ÅµēŹ±£¬øŗ¼«·“Ó¦Ź½ĪŖLi-e-ØTLi+ | |
| B£® | ³äµēŹ±£¬Ńō¼«·“Ó¦Ź½ĪŖS2O42--2e-ØT2SO2 | |
| C£® | ·ÅµēŹ±Li+Ļņøŗ¼«ŅĘ¶Æ | |
| D£® | øƵē³ŲµÄČÜŅŗ²»Ź¹ÓĆĖ®ČÜŅŗ£¬ŌŅņŹĒLiŅ×ÓėĖ®·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
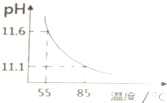
| A£® | c£ØH+£©Ōö“ó£¬c£ØOH-£©¼õŠ” | B£® | $\frac{c£ØC{{O}_{3}}^{2-}£©}{c£ØHC{{O}_{3}}^{-}£©}$±ČÖµ²»¶ĻŌö“ó | ||
| C£® | c£ØCO32-£©+c£ØHCO3-£©+c£ØH2CO3£©=0.10 | D£® | c£ØOH-£©-c£ØHCO3-£©-c£ØH2CO3£©=10-11.1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŹŅĪĀĻĀ£¬ĻņNH4HSO4ČÜŅŗÖŠµĪ¼ÓNaOHČÜŅŗÖĮÖŠŠŌ£ŗc£ØNa+£©£¾c£ØSO42-£©£¾c£ØNH4+£©£¾c£ØOH-£©=c£ØH+£© | |
| B£® | 0.1mol•L-1NaHCO3ČÜŅŗ£ŗc£ØNa+£©£¾c£ØOH-£©£¾c£ØHCO3-£©£¾c£ØH+£© | |
| C£® | NaHSO3ČÜŅŗ£ŗc£ØOH-£©+c£ØSO32-£©=c£ØHSO3-£©+2c£ØH2SO3£©+c£ØH+£© | |
| D£® | 25”ꏱ£¬ÅØ¶Č¾łĪŖ0.1mol•L-1µÄCH3COOH”¢CH3COONa»ģŗĻČÜŅŗ£¬pH=4.75£ŗc£ØCH3COO-£©+c£ØOH-£©£¼c£ØCH3COOH£©+c£ØH+£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ńõ»ÆĪļ | B£® | ÓŠ»śĪļ | C£® | ½šŹō»ņŗĻ½š | D£® | Ėį”¢¼ī”¢ŃĪ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com