
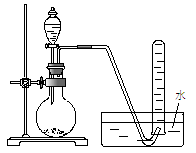
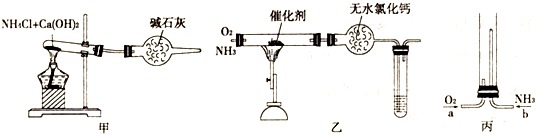
| A.用H2O2溶液和MnO2反应制取O2 |
| B.用浓盐酸和MnO2反应制取C12 |
| C.用稀硫酸与石灰石反应制取CO2 |
| D.用NH4C1和Ca(OH)2反应制取NH3 |
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案科目:高中化学 来源:不详 题型:问答题
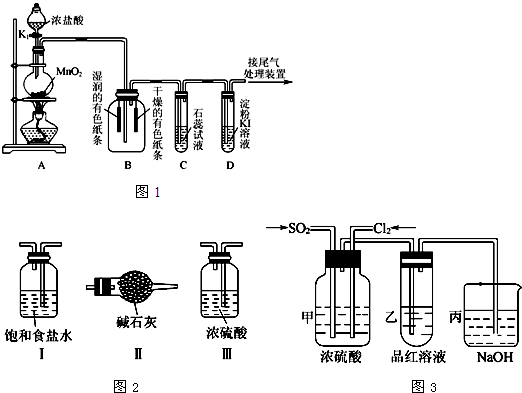
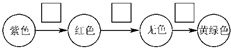 ,请在方框内写出导致该阶段颜色变化的粒子符号.
,请在方框内写出导致该阶段颜色变化的粒子符号.查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
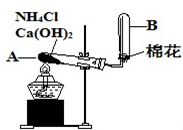
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
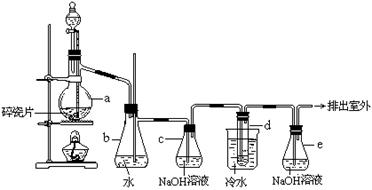
| A.用蒸馏方法提纯水 | B.乙醛的银镜反应 |
| C.实验室制乙烯 | D.实验室制取硝基苯 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
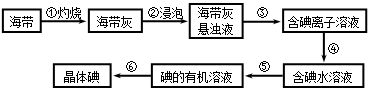
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
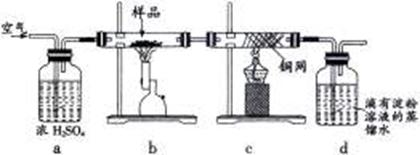
| A.除去空气中的二氧化碳 | B.除去空气中的水蒸气 |
| C.有利于气体混合 | D.有利于观察、控制空气流速 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
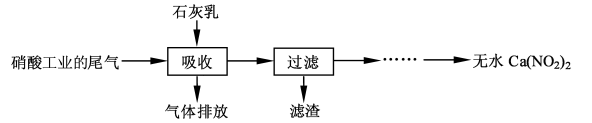
 N2O3(g),其平衡常数表达式为K = 。
N2O3(g),其平衡常数表达式为K = 。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com