
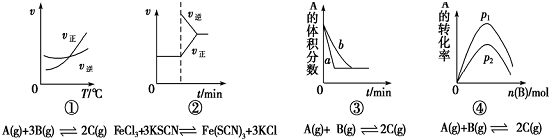
| A. | 图①是其他条件一定时反应速率随温度变化的图象,图象表明,较低温度下升温平衡逆向移动,较高温度下升温平衡正向移 | |
| B. | 图②是在平衡体系的溶液中加入少量KCl晶体后化学反应速率随时间的变化 | |
| C. | 图③可能是催化剂对化学平衡的影响,也可能是其它因素对化学平衡的影响 | |
| D. | 图④是一定条件下,向含有一定量A的容器中逐渐加入B时的图象,压强p1>p2 |
分析 A.图象表明,较低温度下是平衡的建立,较高温度下是平衡的移动;
B.氯化钾不影响平衡移动;
C.催化剂能同等程度的改变正逆反应速率,导致平衡不移动,两边的计量数相等;
D.A的转化率随着B的增加而增大.
解答 解:A.图象表明,较低温度下是平衡的建立,较高温度下是平衡的移动,升高温度平衡正向移动,故A错误;
B.该反应实质为Fe3++3SCN-?Fe(SCN)3,钾离子和氯离子不参加反应,则KCl浓度增大不影响化学平衡移动,故B错误;
C.使用催化剂,反应速率加快,缩短反应时间,所以先达到平衡状态,两边的计量数相等,也可能是改变压强,故C正确;
D.该反应前后气体的物质的量不变,改变压强不影响平衡状态,即不影响A的转化率,由于不断加入B,A的转化率增大,故D错误;
故选C.
点评 本题考查了图象分析,会根据图象中曲线变化趋势、拐点、交点来确定平衡移动方向,注意结合方程式特点分析,注意A中正逆反应速率相等后才是改变条件后反应速率变化,为易错点.


 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案科目:高中化学 来源: 题型:选择题
| A. | HCl气体能使湿润的蓝色石蕊试纸变红 | |
| B. | 通常状况下,NO2是无色的气体 | |
| C. | 铝单质可与氢氧化钠溶液反应生成氢气 | |
| D. | 铁单质与浓硝酸加热时能发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在元素周期表中,Y所在族的元素都是活泼金属元素 | |
| B. | 37Z原子核电子数为20 | |
| C. | X与Y能形成YX型化合物 | |
| D. | 在常温下,Z的单质与氢气一定能大量共存 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 无色溶液:Cu2+、H+、Cl-、SiO32- | |
| B. | NaAlO2溶液:NH4+、H+、Cl-、CO32- | |
| C. | NaHCO3溶液:K+、Al3+、SO42-、NO3- | |
| D. | 能使pH试纸呈红色的溶液:Na+、K+、Fe3+、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
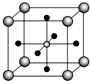 金属钛性能优越,被誉为继Fe、Al后应用广泛的“第三金属”.
金属钛性能优越,被誉为继Fe、Al后应用广泛的“第三金属”.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1,3-二甲基丁烷 | B. | 2,3-二甲基-2-乙基己烷 | ||
| C. | 2,3-二甲基-4-乙基戊烷 | D. | 2,3,5-三甲基己烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
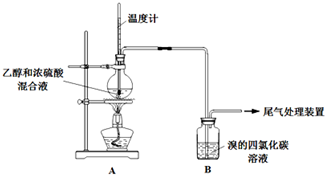
| 操 作 | 现 象 |
| 点燃酒精灯,加热至170℃ | Ⅰ:A中烧瓶内液体渐渐变黑 Ⅱ:B内气泡连续冒出,溶液逐渐褪色 |
| … | |
| 实验完毕,清洗烧瓶 | Ⅲ:A中烧瓶内附着少量黑色颗粒状物,有刺激性气味逸出 |

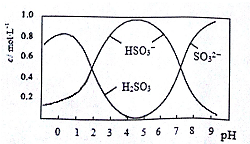
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定温度下,稀释0.1mol/L的CH3COOH溶液,KW不变,Ka将增大 | |
| B. | 对FeCl3溶液进行稀释时,Fe3+水解程度将增大,故溶液的酸性将增强 | |
| C. | 可根据Ksp的数值大小直接比较难溶物在水中的溶解度大小 | |
| D. | 25℃时,Ksp(AgCl)>Ksp(AgI),向AgCl悬浊液中加入KI固体,有黄色沉淀生成 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com