
| A、工业上一般以铁矿石、焦炭、石灰石和空气等原料在高炉中冶炼生铁 |
| B、炼钢主要目的是在高温下用还原剂将过多的碳和其他杂质还原成气体或炉渣除去 |
| C、炼钢中添加硅、锰、铝等作为脱氧剂,调整钢水的成分,制成多种性能优良的钢材 |
| D、电解铝时阴极材料需要定期更换. |


 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:
| A、酿酒过程中,葡萄糖可通过水解反应生成酒精 |
| B、利用催化转化装置可以将汽车尾气中的NO和CO转化为无害气体 |
| C、酸性高锰酸钾溶液中加入植物油充分振荡后,溶液紫色不会褪去 |
| D、制作航天服的聚酯纤维和用于光缆通信的光导纤维都是新型无机非金属材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CO2(H2S):通过CuSO4溶液 |
| B、CH3COOH(H2O):加新制生石灰,蒸馏 |
| C、苯(甲苯):加酸性高锰酸钾溶液、再加NaOH溶液,分液 |
| D、MgCl2溶液(Fe3+):加MgO,过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、电解精炼铜时,若阳极质量减少6.4g,则电路中转移电子数为0.2NA |
| B、标准状况下,44.8L NO与22.4L O2混合后气体中分子总数等于2NA |
| C、1mol Fe在氧气中充分燃烧失去3NA个电子 |
| D、NO2和H2O反应每生成2mol HNO3时转移的电子数目为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应A2(g)+3B2(g)═2AB3(g)在一定温度下能自发进行,则该反应的△H<0 |
| B、将NH3 通入热的CuSO4 溶液中能使Cu2+还原成Cu |
| C、钙和镁的氯化物溶液蒸发结晶出来的固体都是水合物,经焙烧得相应无水盐 |
| D、用酸溶解金属铝时,溶解的速率与铝的纯度有关,纯度越高速率越大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
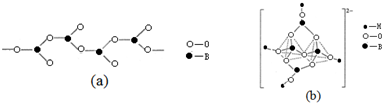
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH4与SiH4的稳定性:CH4>SiH4 |
| B、HClO与H2SO4的酸性:HClO>H2SO4 |
| C、1mol HCl(g)的能量比1mol H2(g)和1mol Cl2(g)的能量和高 |
| D、Cl与S的原子半径:Cl>S |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com