
| A. | 0.336L | B. | 0.448L | C. | 0.896 L | D. | 1.344L |
分析 铜与硝酸反应的实质为3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,只要Cu与氢离子足量,NO3-可以被完全还原,n(Cu)=$\frac{1.92g}{64g/mol}$=0.03mol,硝酸根离子的物质的量为:0.4mol/L×0.1L=0.04mol,氢离子的物质的量为:0.4mol/L×0.1L+0.1mol/L×0.1L×2=0.06mol,根据离子方程式进行过量计算,根据不足量的物质计算n(NO),再根据V=nVm计算NO体积.
解答 解:n(Cu)=$\frac{1.92g}{64g/mol}$=0.03mol,硝酸根离子的物质的量为:0.4mol/L×0.1L=0.04mol,氢离子的物质的量为:0.4mol/L×0.1L+0.1mol/L×0.1L×2=0.06mol,
依据方程式:
3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O
0.03mol 0.04mol 0.06mol
可知氢离子不足,应依据氢离子的物质的量计算产生一氧化氮的物质的量,
3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O
8 2
0.06mol n
n(NO)=$\frac{1}{4}$×0.06mol=0.015mol,
即所得NO体积在标准状况下为0.015mol×22.4L/mol=0.336L,
故选:A.
点评 本题考查了有关离子方程式计算,明确硝酸的性质及发生反应实质,把握离子方程式及过量计算为解答的关键,题目难度不大.


 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源: 题型:选择题
| A. | 生活中,用冰箱保存食物 | |
| B. | H2O2分解时,用MnO2 作催化剂 | |
| C. | 工业合成氨时,采用高温高压的措施 | |
| D. | 提高反应物的浓度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 是两种单质的混合物 | B. | 是共价化合物 | ||
| C. | 该新物质硬度很大 | D. | 含有离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 已知:pAg=-lg{c(Ag+)},Ksp(AgCl)=1×10-12.如图该温度下是向10mL AgNO3溶液中逐渐加入0.1mol•L-1的NaCl溶液时,溶液的pAg随着加入NaCl溶液的体积(单位mL)变化的图象(实线).根据图象所得下列结论不正确的是[提示:Ksp(AgCl)>Ksp(AgI)]( )
已知:pAg=-lg{c(Ag+)},Ksp(AgCl)=1×10-12.如图该温度下是向10mL AgNO3溶液中逐渐加入0.1mol•L-1的NaCl溶液时,溶液的pAg随着加入NaCl溶液的体积(单位mL)变化的图象(实线).根据图象所得下列结论不正确的是[提示:Ksp(AgCl)>Ksp(AgI)]( )| A. | 原AgNO3溶液的物质的量浓度为1mol•L-1 | |
| B. | 图中x点的坐标为(100,6) | |
| C. | 若升高温度,图象会发生变化 | |
| D. | 把0.1mol•L-1的NaCl换成0.1mol•L-1 NaI则图象在终点后变为虚线部分 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
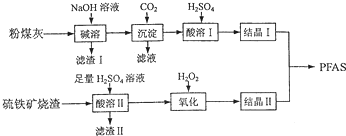
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
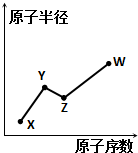 X、Y、Z、W是四种常见的短周期主族元素,其原子半径随原子序数的变化如图所示.已知Y、Z两种元素的单质是空气的主要成分,W原子的最外层电子数与Ne原子的最外层电子数相差1.下列说法正确的是( )
X、Y、Z、W是四种常见的短周期主族元素,其原子半径随原子序数的变化如图所示.已知Y、Z两种元素的单质是空气的主要成分,W原子的最外层电子数与Ne原子的最外层电子数相差1.下列说法正确的是( )| A. | Y、Z、W处于同一周期 | |
| B. | Y、W的最简单氢化物的水溶液能相互反应 | |
| C. | X、W可形成离子化合物XW | |
| D. | X、Z、W形成的化合物均为强酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子里含有-C≡C-的不饱和链烃 | |
| B. | 既能使溴水褪色,又能使酸性KMnO4溶液褪色,但原理不同 | |
| C. | 分子里所有的碳原子都在一条直线上 | |
| D. | 碳原子数相同的炔烃和二烯烃是同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 2-丙醇的催化氧化:2CH3CH(OH)CH3+O2$→_{△}^{Cu}$2CH3CH2CHO+2H2O | |
| B. | 用新制的Cu(OH)2悬浊液检验乙醛:CH3CHO+2Cu(OH)2$\stackrel{△}{→}$CH3COOH+Cu2O↓+2H2O | |
| C. | 实验室制取酚醛树脂: | |
| D. | 甲醛溶液与足量的银氨溶液共热:HCHO+2[Ag(NH3)2]OH$\stackrel{△}{→}$HCOONH4+2Ag↓+3NH3+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com