
R 、W 、X 、Y 、Z 为原子序数依次递增的同一短周期元素,下列说法一定正确的是(m, n 均为整数)( )
A.若R(OH)n为强碱,则W(OH)m也为强碱
B.若HnXOm为强酸,则Y 是活泼非金属元素
C.若Y 的最低负化合价为一2,则Z的最高正化合价为+7
D.若X 的最高正化合价为十5 ,则五种元素一定都是非金属元素
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案科目:高中化学 来源:2015-2016学年甘肃省高一下第二次月考化学试卷(解析版) 题型:填空题
中和热的测定是高中重要的定量实验。取0.55mol/L的NaOH溶液50mL与0.25mol/L的硫酸50mL置于图所示的装置中进行中和热的测定实验,回答下列问题:
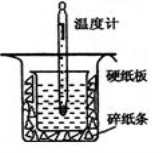
(1)从上图实验装置看,其中尚缺少的一种玻璃用品是_________,除此之外,装置中的一个明显错误是 。
(2)若改用60mL 0.25mol·L-1 H2SO4和50mL 0.55mol·L-1NaOH溶液进行反应与上述实验相比,所放出的热量________ ___(填“相等”、“不相等”),若实验操作均正确,则所求中和热________ ___(填“相等”“不相等”)。
(3)实验数据如下表:
①请填写下表中的空白:
温度 实验次数 | 起始温度t1℃ | 终止温度t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 29.5 |
|
2 | 27.0 | 27.4 | 27.2 | 32.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.2 | |
4 | 26.4 | 26.2 | 26.3 | 29.8 | |
②近似认为0.55 mol/L NaOH溶液和0.25 mol/L硫酸溶液的密度都是1 g/cm3,中和后生成溶液的比热容c=4.18 J/(g·℃)。则中和热ΔH=______ ____ ( 取小数点后一位)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建清流一中高二实验班下第三段测化学试卷(解析版) 题型:选择题
下列离子方程式中正确的是( )
A.乙醇和金属钠反应:CH3CH2OH+Na →CH3CH2O-+ Na++H2↑
B.氯乙烷在NaOH醇溶液中加热:CH3CH2Cl + OH-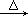 CH3CH2OH+Cl-
CH3CH2OH+Cl-
C.苯酚与NaOH溶液中和反应:H+ + OH- = H2O
D.苯酚钠溶液中通入少量CO2: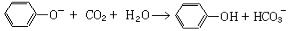
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高一下学期期中考试化学试卷(解析版) 题型:填空题
图1是部分短周期元素的常见化合价与原子序数的关系图:
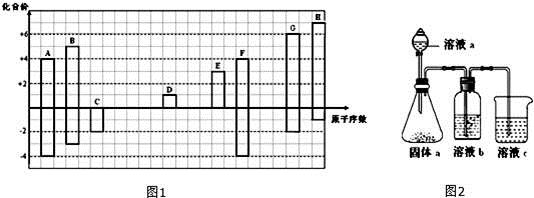
(1)元素F在周期表中的位置__________.
(2)DH其所含化学键类型为__________.
(3)C、D、G对应的简单离子半径大小顺序是__________.(用离子符号回答)
(4)某同学设计实验装置如图2,证明A、B、F的非金属性强弱关系:
①溶液a和溶液b分别为__________,__________.
②溶液c中的离子反应方程式为_____ _____.
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高一下学期期中考试化学试卷(解析版) 题型:选择题
X 、Y 为两种主族元素,其原子的最外层电子数分别为1 和6 ,则X 、Y 两种元素形成的化合物( )
A. 一定是离子化合物
B. 一定是共价化合物
C. 一定形成从X2Y型化合物
D. 以上说法均不妥当
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省抚州市高一下5月月考化学试卷(解析版) 题型:选择题
为体现“绿色奥运”“科技奥运”,2008年北京奥运会出现中国自己生产的燃料电池汽车,作为马拉松领跑车和电视拍摄车,预计该车装着“绿色心脏”——质子交换膜燃料电池,其工作原理如图所示,下列叙述正确的是( )
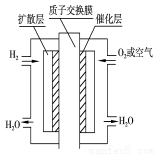
A.通入氧气的电极发生氧化反应
B.通入氢气的电极为正极
C.总反应式为O2+2H2 2H2O
2H2O
D.正极的电极反应式为O2+4H+-4e-=2H2O
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高一下学期第二次月考化学试卷(解析版) 题型:填空题
在一定温度下,体积为2L的密闭容器中,NO2和N2O4之间发生反应:2NO2(g)(红棕色) N2O4g)(无色),如图所示:
N2O4g)(无色),如图所示:
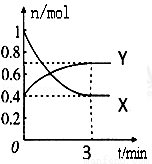
(1)曲线 (填“X”或“Y”)表示NO2的物质的量随时间的变化曲线.
(2)若降低温度,则v(正) ,v(逆) .(填“加快”或“减慢”或“不变”).
(3)若上述反应在甲、乙两个相同容器内同时进行,分别测得甲中v(NO2)=0.3mol/(L•s),乙中v(N2O4)=6mol/(L•min),则 中反应更快.
(4)在0到3min中内N2O4的反应速率为 .
(5)下列叙述能说明该反应已达到化学平衡状态的是(填标号) ;
A.v(NO2)=2v(N2O4)
B.容器内压强不再发生变化
C.X的体积分数不再发生变化
D.容器内气体原子总数不再发生变化
E.相同时间内消耗n mol的Y的同时生成2n mol的X
F.相同时间内消耗n mol的Y的同时消耗2n mol的X.
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江省高二6月月考化学试卷(解析版) 题型:选择题
向分别盛有100 mL水、100 mL 0.1 mol·L-1盐酸、100 mL 0.01 mol·L-1硫酸铜溶液的X、Y、Z三个烧杯中各投入0.05 mol Na。下列有关说法正确的是( )
A.三个烧杯中均会发生的离子反应为2Na+2H2O=2Na++2OH-+H2↑
B.三个烧杯中钠均在液面上剧烈反应,且X烧杯中反应最剧烈
C.三个烧杯反应后,生成的溶质的物质的量浓度相同
D.三个烧杯反应后,生成的气体的质量一定相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com