
固定和利用CO2,能有效地利用资源,并减少空气中的温室气体。工业上正在研究利用CO2来生产甲醇燃料的方法,该方法的化学方程式是:
CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)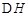 =-49.0kJ·mol
=-49.0kJ·mol
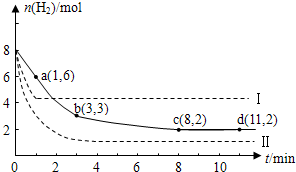
某科学实验小组将6mol CO2和8mol H2充入一容积为2L的密闭容器中(温度保持不变),测得H2的物质的量随时间变化如下图中实线所示(图中字母后的数字表示对应的坐标)。回答下列问题:
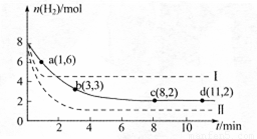
(1)该反应在0~8min内CO2的平均反应速率是 mol·L-1·min-1
(2)此温度下该反应的平衡常数K的数值为 。
(3)仅改变某一条件再进行实验,测得H2的物质的量随时间变化如图中虚线所示。
与实线相比,曲线Ⅰ改变的条件可能是 ,曲线Ⅱ改变的条件可能是 。若实线对应条件下平衡常数为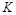 ,曲线Ⅰ对应条件下平衡常数为
,曲线Ⅰ对应条件下平衡常数为 ,曲线Ⅱ对应条件下平衡常数为
,曲线Ⅱ对应条件下平衡常数为 ,则
,则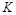 、
、 和
和 的大小关系是
。
的大小关系是
。
(10分)
(1)0.125(2分)
(2)0.5mol-2·L-2 (2分,单位不写扣分)
(3)升高温度(2分);增大压强(2分);K1<K2=K(2分);
【解析】
试题分析:
(1)该反应在0~8min内H2的平均反应速率是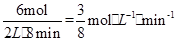 ,根据速率之比等于计量数之比CO2的平均反应速率是0.125
mol·L-1·min-1
,根据速率之比等于计量数之比CO2的平均反应速率是0.125
mol·L-1·min-1
(2)平衡常数K=;
(3)曲线Ⅰ,结合反应CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)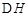 =-49.0kJ·mol,改变的条件升高温度使到达平衡所需时间缩短但氢气的转化率下降;曲线Ⅱ改变的条件增大压强使到达平衡所需时间缩短,由于平衡正向移动,与原平衡相比n(H2)减少;K只与温度有关,
=-49.0kJ·mol,改变的条件升高温度使到达平衡所需时间缩短但氢气的转化率下降;曲线Ⅱ改变的条件增大压强使到达平衡所需时间缩短,由于平衡正向移动,与原平衡相比n(H2)减少;K只与温度有关,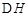 <0的反应。温度越高,K越小,所以K1<K2=K。
<0的反应。温度越高,K越小,所以K1<K2=K。
考点:考查化学反应速率、化学平衡及其影响因素,平衡常数等相关知识。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
 (2014?滨州一模)固定和利用CO2,能有效地利用资源,并减少空气中的温室气体.工业上正在研究利用CO2来生产甲醇燃料的方法,该方法的化学方程式是:
(2014?滨州一模)固定和利用CO2,能有效地利用资源,并减少空气中的温室气体.工业上正在研究利用CO2来生产甲醇燃料的方法,该方法的化学方程式是:查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
 (2011?闵行区二模)固定和利用CO2,能有效地利用资源,并减少空气中的温室气体.工业上正在研究利用CO2来生产甲醇燃料的方法,该方法的化学方程式是:
(2011?闵行区二模)固定和利用CO2,能有效地利用资源,并减少空气中的温室气体.工业上正在研究利用CO2来生产甲醇燃料的方法,该方法的化学方程式是:| [CH3OH]?[H2O] |
| [CO2]?[H2]3 |
| [CH3OH]?[H2O] |
| [CO2]?[H2]3 |
查看答案和解析>>
科目:高中化学 来源:2011届辽宁省沈阳二中高三第五次模拟考试(理综)化学部分 题型:填空题
固定和利用CO2,能有效地利用资源,并减少空气中的温室气体。工业上正在研究利用CO2来生产甲醇燃料的方法,该方法的化学方程式是:
CO2(g) + 3H2(g) CH3OH(g) + H2O(g) △H=" -49.0" kJ·mol-1
CH3OH(g) + H2O(g) △H=" -49.0" kJ·mol-1
某科学实验将6 mol CO2和8 mol H2充入一容积为2 L的密闭容器中(温度保持不变),测得H2的物质的量随时间变化如右图中实线所示(图中字母后的数字表示对应的坐标):
回答下列问题:
(1)该反应在 条件下能自发进行(填编号)。
A、高温 B、低温 C、任何温度
(2)该反应在0~8 min内CO2的平均反应速率是 mol/(L?min)。
(3)该反应的平衡常数K= 。
(4)仅改变某一条件再进行实验,测得H2的物质的量随时间变化如图中虚线所示。与实线相比,曲线Ⅰ改变的条件可能是 ,曲线Ⅱ改变的条件可能是 。
若实线对应条件下平衡常数为K,曲线Ⅰ对应条件下平衡常数为K1,曲线Ⅱ对应条
件下平衡常数为K2,则K、K1和K2的大小关系是 。
(5)根据化学反应速率与化学平衡理论,联系化工生产实际,你认为下列说法不正确的是
。
A.化学反应速率理论可指导怎样在一定时间内快出产品
B.有效碰撞理论可指导怎样提高原料的转化率
C.勒夏特列原理可指导怎样使用有限原料多出产品
D.催化剂的使用是提高产率的有效方法
E.正确利用化学反应速率和化学反应限度都可以提高化工生产的综合经济效益
查看答案和解析>>
科目:高中化学 来源:2010-2011学年辽宁省高三第五次模拟考试(理综)化学部分 题型:填空题
固定和利用CO2,能有效地利用资源,并减少空气中的温室气体。工业上正在研究利用CO2来生产甲醇燃料的方法,该方法的化学方程式是:
CO2(g) + 3H2(g) CH3OH(g) + H2O(g)
△H= -49.0 kJ·mol-1
CH3OH(g) + H2O(g)
△H= -49.0 kJ·mol-1
某科学实验将6 mol CO2和8 mol H2充入一容积为2 L的密闭容器中(温度保持不变),测得H2的物质的量随时间变化如右图中实线所示(图中字母后的数字表示对应的坐标):

回答下列问题:
(1)该反应在 条件下能自发进行(填编号)。
A、高温 B、低温 C、任何温度
(2)该反应在0~8 min内CO2的平均反应速率是 mol/(L•min)。
(3)该反应的平衡常数K= 。
(4)仅改变某一条件再进行实验,测得H2的物质的量随时间变化如图中虚线所示。与实线相比,曲线Ⅰ改变的条件可能是 ,曲线Ⅱ改变的条件可能是 。
若实线对应条件下平衡常数为K,曲线Ⅰ对应条件下平衡常数为K1,曲线Ⅱ对应条
件下平衡常数为K2,则K、K1和K2的大小关系是 。
(5)根据化学反应速率与化学平衡理论,联系化工生产实际,你认为下列说法不正确的是
。
A.化学反应速率理论可指导怎样在一定时间内快出产品
B.有效碰撞理论可指导怎样提高原料的转化率
C.勒夏特列原理可指导怎样使用有限原料多出产品
D.催化剂的使用是提高产率的有效方法
E.正确利用化学反应速率和化学反应限度都可以提高化工生产的综合经济效益
查看答案和解析>>
科目:高中化学 来源:2013届山东省潍坊市高二寒假作业化学(二)试卷 题型:填空题
固定和利用CO2,能有效地利用资源,并减少空气中的温室气体。工业上正在研究利用CO2来生产甲醇燃料的方法,该方法的化学方程式是:CO2(g) + 3H2(g) 
 CH3OH(g)
+H2O(g)
CH3OH(g)
+H2O(g)
△H=-49.0 kJ·mol-1。某科学实验将6 mol CO2和8 mol H2充入一容积为2 L的密闭容器中(温度保持不变),测得H2的物质的量随时间变化如下图中实线所示(图中字母后的数字表示对应的坐标)
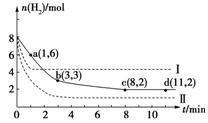
回答下列问题:
(1)该反应在0~8 min内CO2的平均反应速率是 mol/(L•min)。
(2)该反应的平衡常数K= 。
(3)仅改变某一条件再进行实验,测得H2的物质的量随时间变化如图中虚线所示。与实线相比曲线Ⅰ改变的条件可能是 ,曲线Ⅱ改变的条件可能是 。若实线对应条件下平衡常数为K,曲线Ⅰ对应条件下平衡常数为K1,曲线Ⅱ对应条件下平衡常数为K2,则K、K1和K2的大小关系是
(4)根据化学反应速率与化学平衡理论,联系化工生产实际,你认为下列说法不正确的
A.化学反应速率理论可指导怎样在一定时间内快出产品
B.有效碰撞理论可指导怎样提高原料的转化率
C.勒夏特列原理可指导怎样使用有限原料多出产品
D.催化剂的使用是提高产率的有效方法
E.正确利用化学反应速率和化学反应限度都可以提高化工生产的综合经济效益
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com