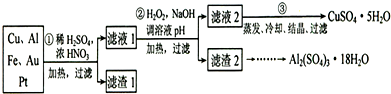
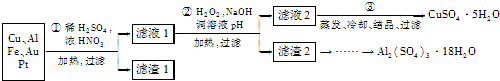
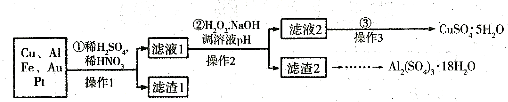
信息时代产生的大量电子垃圾对环境构成了极大的威胁.某“变废为宝”学生探究小组将一批废弃的线路板简单处理后,得到含70%Cu、25%Al、4%Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的路线:
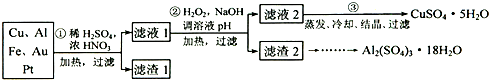
请回答下列问题:
(1)第①步Cu与酸反应的离子方程式为
Cu+4H
++2NO
3-Cu
2++2NO
2↑+2H
2O
或3Cu+8H
++2NO
3-3Cu
2++2NO↑+4H
2O
Cu+4H
++2NO
3-Cu
2++2NO
2↑+2H
2O
或3Cu+8H
++2NO
3-3Cu
2++2NO↑+4H
2O
;得到滤渣1的主要成分为(填化学式)
Au、Pt
Au、Pt
.
(2)第②步加H
2O
2的作用是
将Fe2+氧化为Fe3+
将Fe2+氧化为Fe3+
,使用H
2O
2的优点是
不引入杂质,对环境无污染
不引入杂质,对环境无污染
;调溶液pH的目的是使
Fe3+、Al3+
Fe3+、Al3+
生成沉淀.
(3)用第③步所得CuSO
4?5H
2O制备无水CuSO
4的方法是
加热脱水
加热脱水
.
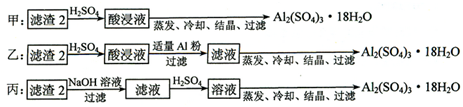
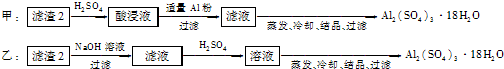
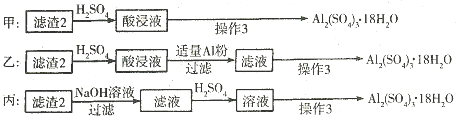
(4)由滤渣2制取Al
2(SO
4)
3?18H
2O,探究小组设计了三种方案:
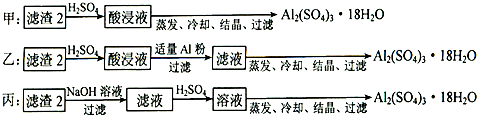
上述三种方案中,
甲
甲
方案不可行,原因是
所得产品中含有较多Fe2(SO4)3杂质
所得产品中含有较多Fe2(SO4)3杂质
:从原子利用率角度考虑,
乙
乙
方案更合理.





 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案