
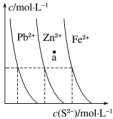
 ČēĶ¼ĪŖijĪĀ¶ČĻĀ£¬PbS£Øs£©”¢ZnS£Øs£©”¢FeS£Øs£©·Ö±šŌŚČÜŅŗÖŠ“ļµ½³ĮµķČܽāĘ½ŗāŗó£¬ČÜŅŗµÄS2-ÅØ¶Č”¢½šŹōŃōĄė×ÓÅØ¶Č±ä»ÆĒéæö£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
ČēĶ¼ĪŖijĪĀ¶ČĻĀ£¬PbS£Øs£©”¢ZnS£Øs£©”¢FeS£Øs£©·Ö±šŌŚČÜŅŗÖŠ“ļµ½³ĮµķČܽāĘ½ŗāŗó£¬ČÜŅŗµÄS2-ÅØ¶Č”¢½šŹōŃōĄė×ÓÅØ¶Č±ä»ÆĒéæö£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©| A£® | ČżÖÖÄŃČÜĪļµÄČܶȻżKsp£ØFeS£©µÄ×īŠ” | |
| B£® | Čē¹ūĻņČżÖÖ³ĮµķÖŠ¼ÓŃĪĖį£¬×īĻČČܽāµÄŹĒPbS | |
| C£® | ĻņŠĀÉś³ÉµÄZnS×ĒŅŗÖŠµĪČė×ćĮæŗ¬ĻąĶ¬ÅØ¶ČµÄPb2+”¢Fe2+µÄČÜŅŗ£¬Õńµ“ŗó£¬ZnS³Įµķ»į×Ŗ»ÆĪŖPbS³Įµķ | |
| D£® | ¶ŌÓŚČżÖÖÄŃČÜĪļĄ“½²£¬aµć¶ŌÓ¦µÄ¶¼ŹĒ²»±„ŗĶČÜŅŗ |
·ÖĪö A£®½šŹōŃōĄė×ÓÅضČĻąĶ¬Ź±£¬S2-ÅضČŌ½Š”£¬KspŌ½Š”£»
B£®KspŌ½“óµÄ¼ÓŃĪĖįĻČČܽā£»
C£®·¢Éś³ĮµķµÄ×Ŗ»Æ£¬ĻņČܶȻżøüŠ”µÄ·½ĻņŅĘ¶Æ£»
D£®ÓÉĶ¼æÉÖŖ£¬Ö»ÓŠc£ØFe2+£©”Įc£ØS2-£©£¼Ksp£ØFeS£©£®
½ā“š ½ā£ŗA£®½šŹōŃōĄė×ÓÅضČĻąĶ¬Ź±£¬S2-ÅضČŌ½Š”£¬KspŌ½Š”£¬ŌņKsp£ØPbS£©£¼Ksp£ØZnS£©£¼Ksp£ØFeS£©£¬Ksp£ØFeS£©×ī“󣬹ŹA“ķĪó£»
B£®KspŌ½“óµÄ¼ÓŃĪĖįĻČČܽā£¬ŌņĻņČżÖÖ³ĮµķÖŠ¼ÓŃĪĖį£¬×īĻČČܽāµÄŹĒFeS£¬¹ŹB“ķĪó£»
C£®·¢Éś³ĮµķµÄ×Ŗ»Æ£¬ĻņČܶȻżøüŠ”µÄ·½ĻņŅĘ¶Æ£¬ŌņĻņŠĀÉś³ÉµÄZnS×ĒŅŗÖŠµĪČė×ćĮæŗ¬ĻąĶ¬ÅØ¶ČµÄPb2+”¢Fe2+µÄČÜŅŗ£¬Õńµ“ŗó£¬ZnS³Įµķ»į×Ŗ»ÆĪŖPbS³Įµķ£¬¹ŹCÕżČ·£»
D£®ÓÉĶ¼æÉÖŖ£¬Ö»ÓŠc£ØFe2+£©”Įc£ØS2-£©£¼Ksp£ØFeS£©£¬ĪŖ²»±„ŗĶČÜŅŗ£¬¶ų¶ŌPbS£Øs£©”¢ZnS£Øs£©Ą“ĖµĪŖ±„ŗĶČÜŅŗ£¬¹ŹD“ķĪó£»
¹ŹŃ”C£®
µćĘĄ ±¾Ģāæ¼²éÄŃČܵē½āÖŹµÄČܽāĘ½ŗā£¬ĪŖøßĘµæ¼µć£¬°ŃĪÕKspµÄ±Č½Ļ”¢Ķ¼Ļó·ÖĪöĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲ·ÖĪöÓėÓ¦ÓĆÄÜĮ¦µÄ漲飬עŅā³ĮµķµÄ×Ŗ»Æ¼°Čܽā£¬ĢāÄæÄŃ¶Č²»“ó£®


 ¼ĘĖćøߏÖĻµĮŠ“š°ø
¼ĘĖćøߏÖĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¼ĘĖćĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
| ĪļÖŹ | CH3OH | CH3OCH3 | H2O |
| c/mol•L-1 | 0.44 | 0.60 | 0.60 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ČōĪĀ¶Č²»±ä½«ČŻĘ÷µÄČŻ»żŌö“ó1±¶£¬“ļµ½ŠĀĘ½ŗāŹ±AµÄÅØ¶Č±äĪŖŌĄ“µÄ0.45 ±¶£¬Ōņm+n£¾p+q | |
| B£® | ČōĘ½ŗāŹ±£¬A”¢BµÄ×Ŗ»ÆĀŹĻąµČ£¬ĖµĆ÷·“Ó¦æŖŹ¼Ź±£¬A”¢BµÄĪļÖŹµÄĮæÖ®±ČĪŖm£ŗn | |
| C£® | ČōÉżøßĘ½ŗāĢåĻµµÄĪĀ¶Č£¬“ļµ½ŠĀĘ½ŗāŹ±A µÄÅØ¶Č±äĪŖŌĄ“µÄ0.55 ±¶£¬ĖµĆ÷øĆ·“Ó¦”÷H£¼0 | |
| D£® | ČōĘ½ŗāŗóĶ¬Ź±Ōö“óA”¢BµÄÅØ¶Č£¬ŌņA”¢BµÄ×Ŗ»ÆĀŹŅ»¶Ø¶¼¼õŠ” |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
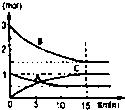 ŌŚÄ³ČŻ»ż²»±äµÄĆܱÕČŻĘ÷ÖŠ£¬ÓŠæÉÄę·“Ó¦£ŗmA£Øg£©+nB£Øg£©?pC£Øg£©+qD£ØS£©”÷H£¼0ČēĶ¼Ä³·“Ó¦¹ż³ĢÖŠø÷ĪļÖŹĪļÖŹµÄĮæn£Ømol£©Ėꏱ¼ätµÄ±ä»ÆĒśĻßĶ¼£®
ŌŚÄ³ČŻ»ż²»±äµÄĆܱÕČŻĘ÷ÖŠ£¬ÓŠæÉÄę·“Ó¦£ŗmA£Øg£©+nB£Øg£©?pC£Øg£©+qD£ØS£©”÷H£¼0ČēĶ¼Ä³·“Ó¦¹ż³ĢÖŠø÷ĪļÖŹĪļÖŹµÄĮæn£Ømol£©Ėꏱ¼ätµÄ±ä»ÆĒśĻßĶ¼£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
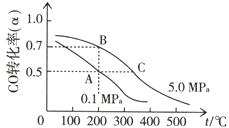 ”°½ą¾»Ćŗ¼¼Źõ”±ŃŠ¾æŌŚŹĄ½ēÉĻĻąµ±Ęձ飬æĘŃŠČĖŌ±ĶعżĻņµŲĻĀĆŗ²ćĘų»ÆĀÆÖŠ½»Ģę¹ÄČėæÕĘųŗĶĖ®ÕōĘųµÄ·½·Ø£¬Į¬Šų²ś³öĮĖČČÖµøß“ļ122500”«16000kJ•m-3µÄĆŗĢæĘų£¬ĘäÖ÷ŅŖ³É·ÖŹĒCOŗĶH2£®COŗĶH2æÉ×÷ĪŖÄÜŌ“ŗĶ»Æ¹¤ŌĮĻ£¬Ó¦ÓĆŹ®·Ö¹ć·ŗ£®
”°½ą¾»Ćŗ¼¼Źõ”±ŃŠ¾æŌŚŹĄ½ēÉĻĻąµ±Ęձ飬æĘŃŠČĖŌ±ĶعżĻņµŲĻĀĆŗ²ćĘų»ÆĀÆÖŠ½»Ģę¹ÄČėæÕĘųŗĶĖ®ÕōĘųµÄ·½·Ø£¬Į¬Šų²ś³öĮĖČČÖµøß“ļ122500”«16000kJ•m-3µÄĆŗĢæĘų£¬ĘäÖ÷ŅŖ³É·ÖŹĒCOŗĶH2£®COŗĶH2æÉ×÷ĪŖÄÜŌ“ŗĶ»Æ¹¤ŌĮĻ£¬Ó¦ÓĆŹ®·Ö¹ć·ŗ£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ģįøß·ēÄÜ”¢Ģ«ŃōÄܵČæÉŌŁÉśĒå½ąÄÜŌ“µÄŹ¹ÓƱȥż | |
| B£® | ĶĘ¹ćCO2ŌŁĄūÓĆ¼¼Źõ£¬½«ĘäŗĻ³ÉÓŠ¼ŪÖµµÄ»Æѧʷ | |
| C£® | ĄūÓĆ¹¤Ņµ·ĻĖ®¹ąøČÅ©×÷Īļ£¬ĢįøßĖ®×ŹŌ“µÄĄūÓĆĀŹ | |
| D£® | ŃŠ·¢ĆŗĢæµÄ½ą¾»”¢øߊ§ĄūÓĆ¼¼Źõ£¬±£»¤ÉśĢ¬»·¾³ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CO2ĶØČėCaCl2ČÜŅŗÖŠ | B£® | NO2ĶØČėFeSO4ČÜŅŗÖŠ | ||
| C£® | NH3ĶØČėA1C13ČÜŅŗÖŠ | D£® | SO2ĶØČėBa£ØNO3£©2ČÜŅŗÖŠ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com