
| A、1mol氧含有6.02×1023个微粒 |
| B、阿伏加德罗常数数值约等于6.02×1023 |
| C、钠的摩尔质量等于它的相对原子质量 |
| D、1mol任何气体所含的气体分子数目,不一定都相等 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、石英(SiO2)是制造玻璃的重要原料之一 |
| B、石英砂可以用于制取高纯度的硅,硅是将太阳能转化为电能的常用材料 |
| C、Na2SiO3是制备硅胶和木材防火剂的原料 |
| D、晶体硅是制造光导纤维的材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:
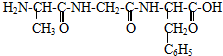
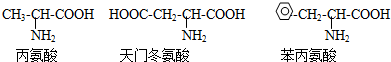
| A、D-12 | ||
| B、D-13 | ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、②③ | C、③④ | D、④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下,1L pH=1的硫酸溶液中含有的H+为0.1NA |
| B、常温下,14g C2H4和C3H6的混合气体中含有2NA个氢原子 |
| C、2.3g Na和足量的O2完全反应,在常温和燃烧时,转移电子数均为0.1NA |
| D、1mol甲醇中含有C-H键的数目为4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素编号 | 元素性质或原子结构 |
| A | 该元素有一种核素质量数为1 |
| B | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| C | 形成的简单离子是第三周期元素形成简单离子半径中最小的 |
查看答案和解析>>
科目:高中化学 来源: 题型:
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | |||
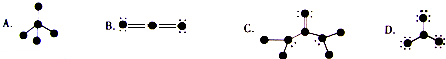
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com