
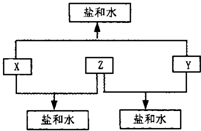
 已知:已知A、B、C、D四种短周期元素原子序数依次增大,A与D的原子序数之和等于B与C的原子序数之和,由D元素组成的单质在通常状况下呈黄绿色,B、C、D三种元素位于同一周期,A、B、C三种元素的最高价氧化物对应的水化物分别为X、Y、Z,且存在如下转化关系,试推断回答下列问题.
已知:已知A、B、C、D四种短周期元素原子序数依次增大,A与D的原子序数之和等于B与C的原子序数之和,由D元素组成的单质在通常状况下呈黄绿色,B、C、D三种元素位于同一周期,A、B、C三种元素的最高价氧化物对应的水化物分别为X、Y、Z,且存在如下转化关系,试推断回答下列问题.

| ||
| ||
 ,故答案为:
,故答案为: ;
;
| ||
| ||


 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案科目:高中化学 来源: 题型:


| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)画出B的原子结构示意图______________;写出C和D形成的淡黄色固体化合物的电子式______________。
(2)元素原子的物质的量之比为A∶B∶C=4∶2∶3的晶体名称为______________,其水溶液显______________性,其反应的离子方程式为_______________________________。
(3)请写出与A2C和BA3分子中电子数相同,且仍由A、B、C元素中任意两元素组成的粒子符号(举两例)______________。
(4)写出由B、C元素组成且元素原子质量比为B∶C=7∶12的化合物的化学式_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知A、B、C是中学化学的常见物质,它们在一定条件下有如下转化关系:
(1)若A能使湿润的红色石蕊试纸变蓝,C为红棕色气体。则实验室常用的制取A的化学方程式为 ,A转化为B的化学方程式为 。
(2)若组成D单质的元素在地壳中含量最高,A元素焰色反应为黄色,则C的电子式为 。
(3)若D是金属,C溶液在贮存时应加入少量D,其理由是(只用离子方程式说明)________________,A与D反应的化学方程式是 。
(4)若D是一种常见的温室气体;A是一种强电解质且在水溶液中电离出的阴、阳离子均含有10个电子。则B转化为C的离子方程式为 。
(5)若D为一种强碱,B具有两性,则C溶液中除氢氧根外还存在的阴离子的化学式为 。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年北京市四中高一下学期期中考试化学试卷(带解析) 题型:填空题
已知A、B、C是中学化学的常见物质,它们在一定条件下有如下转化关系: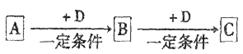
(1)若A能使湿润的红色石蕊试纸变蓝,C为红棕色气体。则实验室常用的制取A的化学方程式为 ,A转化为B的化学方程式为 。
(2)若组成D单质的元素在地壳中含量最高,A元素焰色反应为黄色,则C的电子式为 。
(3)若D是金属,C溶液在贮存时应加入少量D,其理由是(只用离子方程式说明)________________,A与D反应的化学方程式是 。
(4)若D是一种常见的温室气体;A是一种强电解质且在水溶液中电离出的阴、阳离子均含有10个电子。则B转化为C的离子方程式为 。
(5)若D为一种强碱,B具有两性,则C溶液中除氢氧根外还存在的阴离子的化学式为 。
查看答案和解析>>
科目:高中化学 来源:2014届北京市高一下学期期中考试化学试卷(解析版) 题型:填空题
已知A、B、C是中学化学的常见物质,它们在一定条件下有如下转化关系:
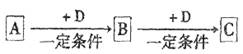
(1)若A能使湿润的红色石蕊试纸变蓝,C为红棕色气体。则实验室常用的制取A的化学方程式为 ,A转化为B的化学方程式为 。
(2)若组成D单质的元素在地壳中含量最高,A元素焰色反应为黄色,则C的电子式为 。
(3)若D是金属,C溶液在贮存时应加入少量D,其理由是(只用离子方程式说明)________________,A与D反应的化学方程式是 。
(4)若D是一种常见的温室气体;A是一种强电解质且在水溶液中电离出的阴、阳离子均含有10个电子。则B转化为C的离子方程式为 。
(5)若D为一种强碱,B具有两性,则C溶液中除氢氧根外还存在的阴离子的化学式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com