
| A. | 放电时负极上I-被氧化 | |
| B. | 充电时Li+从阳极区移向阴极区 | |
| C. | 充电时阴极反应为:LiOH+e-═Li+OH- | |
| D. | 放电时正极反应为:O2+2H2O+4Li++4e-═4LiOH |
分析 A.放电时,负极上发生失电子的氧化反应,元素的化合价升高;
B.充电时,电解质里的阳离子移向阴极,阴离子移向阳极;
C.充电时阴极发生得电子的还原反应;
D.放电时,正极上发生得电子的还原反应,据此书写电极反应式.
解答 解:A.放电时,负极上发生失电子的氧化反应,元素的化合价升高,根据总反应,I- 被氧化,故A正确;
B.充电时,电解质里的阳离子移向阴极,故B正确;
C.充电时阴极发生得电子的还原反应,应该是碘单质得电子的还原反应,故C错误;
D.放电时,正极上发生得电子的还原反应,正极反应为O2+2H2O+4Li++4e-═4LiOH,故D正确;
故选C.
点评 本题以新型电池为载体考查原电池和电解池原理,明确原电池和电解池电极上得失电子即可解答,注意电极方程式的书写是关键.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 纯碱溶液中逐滴加少量盐酸:CO32-+H+═HCO3- | |
| B. | 钢铁发生吸氧腐蚀时,铁作负极被氧化:Fe-3e-=Fe3+ | |
| C. | 向FeBr2溶液中通入过量Cl2的离子方程式:2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- | |
| D. | 过氧化氢能使酸性KMnO4溶液褪色:3H2O2+2MnO4-+6H+═2Mn2++4O2↑+6H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
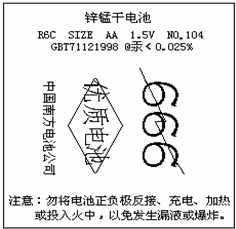 王亮在超市看到一种电池外壳的纸层包装印有如图的文字,请根据要求回答
王亮在超市看到一种电池外壳的纸层包装印有如图的文字,请根据要求回答查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 它们互为同分异构体 | B. | 丙酸分子之间存在氢键 | ||
| C. | 它们可用核磁共振氢谱法鉴别 | D. | 它们可用KMnO4(H+)溶液鉴别 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2═CH2 | B. | CH3CH═CHCH3 | C. | (CH3)2C═C(CH3)2 | D. | CH2═CHCH2CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com