
【题目】某小组为研究电化学原理,设计了如图所示装置。
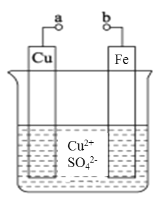
下列叙述不正确的是
A.a和b不连接时,Fe片上会有金属 Cu析出
B.a和b用导线连接时,Cu 片上发生的反应为Cu2++2e- =Cu
C.a和b导线连接时,电子从Fe 电极经溶液流向Cu电极
D.a和b用导线连接后.电流由Fe电极经导线流向Cu 电极
科目:高中化学 来源: 题型:
【题目】研究表明不含结晶水的X(由4种短周期元素组成),可作为氧化剂和漂白剂,被广泛应用于蓄电池工业等。为探究X的组成和性质,设计并完成了下列实验:
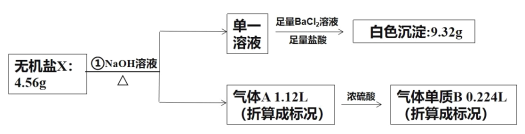
已知:气体单质B可使带火星的木条复燃。
(1)X中含有的元素为:____;图中被浓硫酸吸收的气体的电子式为:_____。
(2)请写出①的化学方程式:_____。
(3)已知X常用于检验Mn2+,它可将Mn2+氧化成MnO4-。请写出X溶液和少量MnCl2溶液反应的离子方程式:_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚合物H(![]() )是一种聚酰胺纤维,广泛用于各种刹车片,其合成路线如图:
)是一种聚酰胺纤维,广泛用于各种刹车片,其合成路线如图:
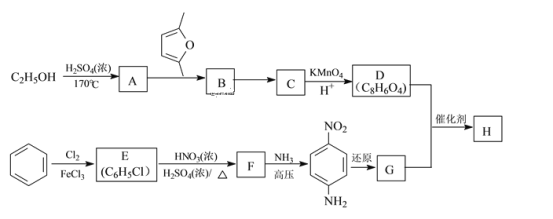
已知:①C、D、G均为芳香族化合物,分子中均只含两种不同化学环境的氢原子
②Diels-Alder反应:![]() +
+![]()
![]()
![]()
③RCOOH+H2N-R'→RCOONHR'+H2O
(1)生成D的名称是_______。
(2)B的结构简式是_______;“B→C”的反应中,除C外,另外一种产物是_______。
(3)D+G→H的化学方程式是______。
(4)Q是D的同系物,相对分子质量比D大14,则Q可能的结构有______种,其中核磁共振氢谱有4组峰,且峰面积比为1:2:2:3的结构简式为______。(任写一种)。
(5)已知:乙炔与1,3-丁二烯也能发生Diels-Alder反应。请以1,3-丁二烯和乙炔为原料,选用必要的无机试剂合成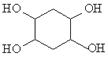 ,写出合成路线______。(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
,写出合成路线______。(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于放热反应Zn+H2SO4=ZnSO4+H2↑,下列叙述正确的是
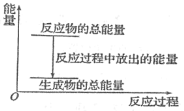
A.反应过程中的能量关系可用上图表示
B.1 mol Zn的能量大于1 mol H2的能量
C.若将其设计为原电池,则其能量转化形式为电能转化为化学能
D.若将其设计为原电池,当有32.5 g Zn溶解时,正极放出的气体一定为11.2 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W为短周期主族元素,原子序数依次增大,X原子的最外层电子数是第一层电子数的2倍,Y的气态氢化物与最高价氧化物的水化物可形成盐,Z的最外层电子数与其电子总数比为3:8,下列说法正确的是![]()
A.X、Y、W的最高价含氧酸酸性顺序:![]()
B.Z、W可形成![]() 的化合物,属于离子化合物
的化合物,属于离子化合物
C.离子半径:![]()
D.气态氢化物的稳定性:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五种短周期元素A、B、C、D、E的原子序数依次增大,A和C同族,B和D同族,C离子和B离子具有相同的电子层结构.A和B、D、E均能形成共价型化合物.A和B形成的化合物在水中呈碱性,C和E形成的化合物在水中呈中性.下列说法正确的是![]()
A.五种元素中原子半径最大的是E,最小的是A
B.A和B、D、E均能形成共价型化合物中,稳定性最差的是A、D形成的化合物
C.E最高价氧化物对应水化物化学式为![]()
D.C的单质在空气中燃烧产物的化学式为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:甲、乙、丙、丁为常见化合物,A、B为单质,相互转化关系如图。其中甲是天然气的主要成分。回答下列问题:
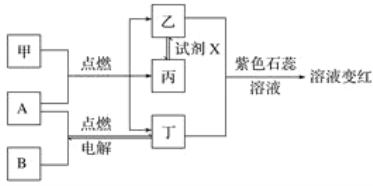
(1)丁物质的名称:______,丙物质的化学式:_________________________________________。
(2)检验化合物乙的化学方程式:___________________________________________________。
(3)试剂X可能的化学式:________、________(要求:所选物质类别不同)。
(4)通过分析表明:燃料充分燃烧的条件之一是______________________________。
(5)取变红溶液于试管中加热,观察到的现象有_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物YX2、ZX2中,X、Y、Z的核电荷数小于18;X原子最外能层的p能级中有一个轨道充填了2个电子,Y原子的最外层中p能级的电子数等于前一能层电子总数,且X和Y具有相同的电子层;Z与X在周期表中位于同一主族。回答下列问题:
(1)X的价电子排布式为____________,Y的电子排布图为___________;
(2)ZX2的分子式是________________,VSEPR模型名称为________________。YX2的电子式是______________,中心原子发生了________杂化。
(3)Y与Z形成的化合物的分子式是_______________。Y的氢化物中分子构型为正四面体的是_________(填名称),键角为______________,中心原子的杂化形式为_________。
(4)X的氢化物的沸点比同主族其他元素形成的氢化物沸点高,原因是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列框图涉及的物质所含元素中,除一种元素外,其余均为1~18号元素。
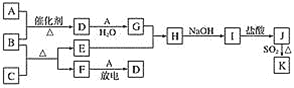
已知:A、F为无色气体单质,B为具有刺激性气味的气体,化学家哈伯因合成B获得1918年的诺贝尔化学奖。C为黑色氧化物,E为紫红色金属单质,I为蓝色沉淀(部分反应的产物未列出)。请回答下列问题:
(1)常温下铝遇到G的浓溶液后表面形成一层致密的保护膜,该现象称为___________。
(2)E与G的稀溶液反应的离子方程式为_________。
(3)在25 ℃和101 kPa的条件下,将VL的B气体溶于100 mL水中,得到密度为ρg·mL-1的溶液M,则M溶液的物质的量浓度为________ mol·L-1。(已知25 ℃、101 kPa条件下气体摩尔体积为24.5 L·mol-1,不必化简)
(4)分别蘸取B的浓溶液和G的浓溶液的玻璃棒,接近后的现象是_________。
(5)B和C反应的化学方程式为__________。
(6)J、K是同种金属的不同氯化物,K为白色沉淀。写出SO2还原J生成K的离子方程式:______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com