
”¾ĢāÄæ”æŅ»ÖÖµŚ¶ž“śæ¹×é°·Ņ©ĪļµÄÖŠ¼äĢåGµÄŗĻ³ÉĀ·ĻßČēĻĀ£ŗ

ŅŃÖŖ£ŗAµÄ·Ö×Ó½į¹¹ÖŠŗ¬ÓŠ2øö¼×»ł”£
»Ų“šĻĀĮŠĪŹĢā:
£Ø1£©AµÄĆū³ĘĪŖ__________£¬ÓÉAÉś³ÉBµÄ·“Ó¦ĄąŠĶĪŖ_______”£
£Ø2£©GÖŠŗ¬Ńõ¹ŁÄÜĶÅĆū³ĘĪŖ_______”£
£Ø3£©FµÄ·Ö×ÓŹ½ĪŖ_______”£
£Ø4£©ÓÉCÉś³ÉDµÄ»Æѧ·½³ĢŹ½ĪŖ______________”£
£Ø5£©¶Ō¶žČ”“ś·¼Ļć»ÆŗĻĪļWŹĒEµÄĶ¬·ÖŅģ¹¹Ģ壬WÄÜ·¢ÉśŅų¾µ·“Ó¦ŗĶĖ®½ā·“Ó¦£¬Ė®½ā²śĪļÖ®Ņ»ÄÜÓėFeCl3ČÜŅŗ·¢ÉśĻŌÉ«·“Ó¦£¬ŌņWÓŠ________ÖÖ½į¹¹£¬ĘäÖŠŗĖ“Ź²ÕńĒāĘ×ĪŖĪå×é·å£¬ĒŅ·åĆ껿֮±ČĪŖ1£ŗ2 : 2 : 2£ŗ9µÄ½į¹¹¼ņŹ½ĪŖ_____________”£
£Ø6£©²ĪÕÕÉĻŹöŗĻ³ÉĀ·Ļß,ŅŌŅŅČ©ĪŖŌĮĻ(ĪŽ»śŹŌ¼ĮČĪŃ”)£¬Éč¼ĘÕż¶”“¼µÄŗĻ³ÉĀ·Ļß:_______________________________”£
”¾“š°ø”æ ±ūĶŖ ¼Ó³É·“Ó¦ õ„»ł”¢ōŹ»ł C4H6Cl2O  8
8 ![]() CH3CHO
CH3CHO![]()
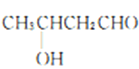
![]() CH3CH=CHCHO
CH3CH=CHCHO![]() CH3CH2CH2CH2OH
CH3CH2CH2CH2OH
”¾½āĪö”æ(1)øł¾ŻAµÄ·Ö×ÓŹ½½įŗĻAµÄ·Ö×Ó½į¹¹ÖŠŗ¬ÓŠ2øö¼×»łÖŖAĪŖ±ūĶŖ(CH3COCH3)£¬AŌŚĒāŃõ»Æ±µ“ęŌŚĢõ¼žĻĀ·“Ӧɜ³ÉB(C6H12O2)£¬ĪŖ2·Ö×ÓA·¢ÉśµÄ¼Ó³É·“Ó¦£¬¹Ź“š°øĪŖ£ŗ±ūĶŖ£»¼Ó³É·“Ó¦£»
(2)G(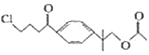 )ÖŠµÄŗ¬Ńõ¹ŁÄÜĶÅÓŠõ„»ł”¢ōŹ»ł£¬¹Ź“š°øĪŖ£ŗõ„»ł”¢ōŹ»ł£»
)ÖŠµÄŗ¬Ńõ¹ŁÄÜĶÅÓŠõ„»ł”¢ōŹ»ł£¬¹Ź“š°øĪŖ£ŗõ„»ł”¢ōŹ»ł£»
(3)F(![]() )µÄ·Ö×ÓŹ½ĪŖC4H6Cl2O£¬¹Ź“š°øĪŖ£ŗC4H6Cl2O£»
)µÄ·Ö×ÓŹ½ĪŖC4H6Cl2O£¬¹Ź“š°øĪŖ£ŗC4H6Cl2O£»
(4)øł¾Ż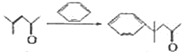 ½įŗĻCDµÄ·Ö×ÓŹ½æÉÖŖ£¬CŗĶ±½·¢Éś¼Ó³É·“Ӧɜ³ÉD£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ
½įŗĻCDµÄ·Ö×ÓŹ½æÉÖŖ£¬CŗĶ±½·¢Éś¼Ó³É·“Ӧɜ³ÉD£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ £¬¹Ź“š°øĪŖ£ŗ
£¬¹Ź“š°øĪŖ£ŗ £»
£»
(5)¶Ō¶žČ”“ś·¼Ļć»ÆŗĻĪļWŹĒE(![]() )µÄĶ¬·ÖŅģ¹¹Ģ壬WÄÜ·¢ÉśŅų¾µ·“Ó¦ŗĶĖ®½ā·“Ó¦£¬ĖµĆ÷WŹōÓŚ¼×Ėįõ„£¬Ė®½ā²śĪļÖ®Ņ»ÄÜÓėFeCl3ČÜŅŗ·¢ÉśĻŌÉ«·“Ó¦£¬ĖµĆ÷õ„»łÓė±½»·Į¬½Ó£¬ŌņWÖŠŗ¬ÓŠ
)µÄĶ¬·ÖŅģ¹¹Ģ壬WÄÜ·¢ÉśŅų¾µ·“Ó¦ŗĶĖ®½ā·“Ó¦£¬ĖµĆ÷WŹōÓŚ¼×Ėįõ„£¬Ė®½ā²śĪļÖ®Ņ»ÄÜÓėFeCl3ČÜŅŗ·¢ÉśĻŌÉ«·“Ó¦£¬ĖµĆ÷õ„»łÓė±½»·Į¬½Ó£¬ŌņWÖŠŗ¬ÓŠ![]() ½į¹¹£¬¶ŌĪ»»łĶŵĻÆѧŹ½ĪŖ”ŖC5H11£¬ŅņĪŖÓŠ”ŖC5H118ÖÖ½į¹¹£¬Ņņ“ĖWÓŠ8ÖÖ½į¹¹£¬ĘäÖŠŗĖ“Ź²ÕńĒāĘ×ĪŖĪå×é·å£¬ĒŅ·åĆ껿֮±ČĪŖ1£ŗ2:2:2£ŗ9µÄ½į¹¹¼ņŹ½ĪŖ
½į¹¹£¬¶ŌĪ»»łĶŵĻÆѧŹ½ĪŖ”ŖC5H11£¬ŅņĪŖÓŠ”ŖC5H118ÖÖ½į¹¹£¬Ņņ“ĖWÓŠ8ÖÖ½į¹¹£¬ĘäÖŠŗĖ“Ź²ÕńĒāĘ×ĪŖĪå×é·å£¬ĒŅ·åĆ껿֮±ČĪŖ1£ŗ2:2:2£ŗ9µÄ½į¹¹¼ņŹ½ĪŖ![]() £¬¹Ź“š°øĪŖ£ŗ8£»
£¬¹Ź“š°øĪŖ£ŗ8£»![]() £»
£»
(6)ŅŌŅŅČ©ĪŖŌĮĻŗĻ³ÉÕż¶”“¼£¬øł¾ŻA”śB”śCµÄ·“Ó¦ŌĄķæÉŅŌŹ¹Ģ¼Į“Ōö³¤£¬2·Ö×ÓŅŅČ©æÉŅŌŗĻ³É³öCH3CH=CHCHO£¬ŌŁÓėĒāĘų¼Ó³É¼“æÉ£¬Ņņ“ĖŗĻ³ÉĀ·ĻßĪŖCH3CHO![]()
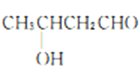
![]() CH3CH=CHCHO
CH3CH=CHCHO![]() CH3CH2CH2CH2OH£¬¹Ź“š°øĪŖ£ŗCH3CHO
CH3CH2CH2CH2OH£¬¹Ź“š°øĪŖ£ŗCH3CHO![]()
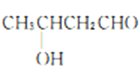
![]() CH3CH=CHCHO
CH3CH=CHCHO![]() CH3CH2CH2CH2OHӣ
CH3CH2CH2CH2OHӣ


 Ņ»ĻßĆūŹ¦ČØĶž×÷Ņµ±¾ĻµĮŠ“š°ø
Ņ»ĻßĆūŹ¦ČØĶž×÷Ņµ±¾ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĶŠæŌµē³Ų×°ÖĆČēĶ¼ĖłŹ¾£¬ĘäÖŠŃōĄė×Ó½»»»Ä¤Ö»ŌŹŠķŃōĄė×ÓŗĶĖ®·Ö×ÓĶعż£¬ĻĀĮŠÓŠ¹ŲŠšŹöÕżČ·µÄŹĒ( )

A. Šæµē¼«ÉĻ·¢ÉśµÄ·“Ó¦£ŗZn2£«£«2e£===Zn
B. µē³Ų¹¤×÷Ņ»¶ĪŹ±¼äŗ󣬼׳ŲµÄc(SO![]() )¼õŠ”
)¼õŠ”
C. µēĮ÷ÓÉŠæµē¼«¾µēĮ÷±ķĮ÷ĻņĶµē¼«
D. µē³Ų¹¤×÷Ņ»¶ĪŹ±¼äŗó£¬ŅŅ³ŲČÜŅŗµÄ×ÜÖŹĮæŌö¼Ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ°“ĻĀĮŠŹµŃé·½·Ø²Ł×÷£¬ÄÜ“ļµ½ŅŖĒóµÄŹĒ£Ø £©
A.ÓĆĶŠÅĢĢģĘ½³ĘĮæ25.20gĀČ»ÆÄĘ¹ĢĢå
B.ŹµŃéŹŅÖĘČ”ÕōĮóĖ®Ź±£¬Ō²µ×ÉÕĘæÖŠ¼ÓŠ©Ėé“ÉʬæÉ·ĄÖ¹±©·Š
C.¼ÓČȱ„ŗĶFeCl3ČÜŅŗÖʱøFe£ØOH£©3½ŗĢå
D.½«ĒāŃõ»ÆÄĘ¹ĢĢåŌŚČŻĮæĘæÖŠČܽā£¬ÅäÖĘŅ»¶ØĪļÖŹµÄĮæÅØ¶ČµÄNaOHČÜŅŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”ær”ŖFe2O3ŹĒŅ»ÖÖ¾ßÓŠ“ÅŠŌ”¢“߻Ɣ¢ĘųĆōµÄÄÉĆײÄĮĻ”£Ņ»ÖÖŅŌĮņĢśæóÉÕŌüµČĪŖŌĮĻÖʱør”ŖFe2O3µÄĮ÷³ĢČēĻĀ£ŗ

(1)ĻĀĮŠÓŠ¹Ų”°»¹Ō±ŗÉÕ”±¹¤ŠņµÄĖµ·ØÕżČ·µÄŹĒ_____(Ģī×ÖÄø)”£
a.½¹ĢæӦɣĮ棬æÕĘųÓ¦¹żĮæ
b. ±ŗÉÕ¹ż³Ģ¾łĪŖĪüČČ·“Ó¦£¬ŠčÓƵēĀƳ֊ų¼ÓČČ·“Ó¦Ę÷
c.”°»¹Ō±ŗÉÕ”±µÄÖ÷ŅŖ·“Ó¦ĪŖ 3C+2O2![]() 2CO+CO2”¢Fe2O3+CO
2CO+CO2ӢFe2O3+CO![]() 2FeO+CO2
2FeO+CO2
(2)”°½žČ””±Ē°Šč½«±ŗÉÕÉś³ÉµÄČŪĢå·ŪĖ飬ĘäÄæµÄŹĒ_____________________”£
(3)ŅŃÖŖČżÖÖ½šŹōĄė×ÓæŖŹ¼³ĮµķŗĶĶźČ«³ĮµķµÄpHČēĻĀ±ķ£ŗ
Fe3+ | Fe2+ | Al3+ | |
æŖŹ¼³ĮµķµÄpH | 2.2 | 7.5 | 4.1 |
ĶźČ«³ĮµķµÄpH | 3.5 | 9.5 | 5.4 |
Ōņ”°µ÷pH”±Ź±£¬ČÜŅŗµÄpH·¶Ī§ĪŖ_______________”£
(4)ĀĖŌü1µÄÖ÷ŅŖ³É·ÖĪŖ_________(Ģī»ÆѧŹ½)£»”°³ĮĢś”±Ź±·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ___________”£
(5)”°¹żĀĖ2”±Ź±ŠčÓĆÕōĮóĖ®Ļ“µÓ£¬ÄÜÖ¤Ć÷³ĮµķŅŃĻ“µÓøɾ»µÄ·½·ØŹĒ_________£»³Įµķ»ŗĀżŃõ»ÆĪŖĢś»ĘµÄ»Æѧ·½³ĢŹ½ĪŖ________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijĪ»Ķ¬Ń§ĪŖŃéÖ¤SO2µÄ»ÆѧŠŌÖŹ£¬×öĮĖŅ»ĻµĮŠŹµŃ飬øł¾ŻŹµŃéĶź³ÉĻĀĮŠŹµŃéŅŖĒó£ŗ
ÓĆĶÓėÅØĮņĖį·“Ó¦ÖʵĆSO2£¬»Æѧ·½³ĢŹ½ĪŖ_____________________________”£
(1)½«SO2ĶØČėĒāĮņĖįÖŠ£¬ĻÖĻóŹĒ__________£¬»Æѧ·“Ó¦·½³ĢŹ½ĪŖ________________£¬ÕāĖµĆ÷SO2¾ßÓŠ________ŠŌ”£
(2)½«SO2ĶØČėäåĖ®ÖŠ£¬ĻÖĻóŹĒ_________________£¬»Æѧ·“Ó¦·½³ĢŹ½ĪŖ___________£¬ĖµĆ÷SO2¾ßÓŠ________ŠŌ”£
(3)½«SO2ĶØČėĘ·ŗģČÜŅŗ£¬ĻÖĻóŹĒ_______________£¬½«Éś³ÉµÄČÜŅŗ¼ÓČČÖó·Š£¬ĻÖĻóŹĒ________________£¬ŌŅņŹĒ____________________”£
(4)½«SO2ĶØČėNaOHČÜŅŗ(ŗ¬ÓŠ·ÓĢŖÖøŹ¾¼Į)ÖŠ£¬ĻÖĻóŹĒ________£¬»Æѧ·½³ĢŹ½ĪŖ________________£¬ÕāĖµĆ÷SO2¾ßÓŠ________ŠŌŃõ»ÆĪļµÄŠŌÖŹ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓĆŅŅĻ©ŗĶŅŅ“¼ĪŖŌĮĻÖĘČ”²ŻĖį¶žŅŅõ„µÄ¹ż³ĢÖŠ·¢ÉśµÄ·“Ó¦ĄąŠĶ¼°Ė³ŠņÕżČ·µÄŹĒ
¢Łõ„»Æ·“Ó¦ ¢ŚŃõ»Æ·“Ó¦ ¢ŪĖ®½ā·“Ó¦ ¢Ü¼Ó³É·“Ó¦
A. ¢Ś¢Ü¢Ū¢Ł B. ¢Ü¢Ł¢Ś¢Ū C. ¢Ü¢Ū¢Ś¢Ł D. ¢Ś¢Ū¢Ł¢Ü
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ³£ĪĀĻĀ£¬¹ŲÓŚĻĀĮŠĮ½øö·“Ó¦£ŗ
a”¢0.1 mol£ÆL “×ĖįČÜŅŗ£ŗCH3COOH![]() CH3COO-+H+
CH3COO-+H+
b”¢0.1 mol£ÆL “×ĖįÄĘČÜŅŗ£ŗCH3COO-+H2O![]() CH3COOH+OH-
CH3COOH+OH-
£Ø1£©Į½Ź½µ½“ļĘ½ŗāŗ󣬼ÓČėŅ»¶ØĮæµÄĖ®ŗó£¬Ę½ŗāĻņÓŅŅĘ¶ÆµÄŹĒ________£¬ČÜŅŗµÄpHŌö“óµÄŹĒ________________”£
£Ø2£©Ļņb·“Ó¦ÖŠ¼ÓČėÉŁĮæµÄ“×ĖįÄĘ¹ĢĢ壬ČÜŅŗµÄpH½«________£¬Čō¼ÓČėĶ¬ÅØ¶ČµÄ“×ĖįÄĘČÜŅŗ£¬ČÜŅŗµÄpH½«________£ØĢī”°Ōö“ó”±”¢”°¼õŠ””±”¢”°²»±ä”±£©”£
£Ø3£©ČōĻņa·“Ó¦ÖŠ¼ÓČėÉŁĮæµÄ“×ĖįÄĘ¹ĢĢ壬ČÜŅŗµÄpH½«________£¬µēĄė³Ģ¶Č½«________£¬ČÜŅŗµÄµ¼µēŠŌ½«________£ØĢī”°Ōö“ó”±”¢”°¼õŠ””±”¢”°²»±ä”±£©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ·¢Õ¹½ą¾»Ćŗ¼¼Źõ”¢ĄūÓĆCO2ÖʱøĒå½ąÄÜŌ“µČ¶¼ŹĒŹµĻÖ¼õĢ¼ÅŷŵÄÖŲŅŖĶ¾¾¶”£
£Ø1£©½«Ćŗ×Ŗ»Æ³ÉĖ®ĆŗĘųµÄ·“Ó¦£ŗC£Øs£©+H2O£Øg£©![]() CO£Øg£©+H2£Øg£©æÉÓŠŠ§ĢįøßÄÜŌ“ĄūÓĆĀŹ£¬ČōŌŚÉĻŹö·“Ó¦ĢåĻµÖŠŌö“óH2µÄÅØ¶Č£ØĘäĖūĢõ¼ž±£³Ö²»±ä£©£¬“Ė·“Ó¦µÄ”÷H_____£ØĢī”°Ōö“ó”±”¢”°¼õŠ””±»ņ”°²»±ä”±£©”£
CO£Øg£©+H2£Øg£©æÉÓŠŠ§ĢįøßÄÜŌ“ĄūÓĆĀŹ£¬ČōŌŚÉĻŹö·“Ó¦ĢåĻµÖŠŌö“óH2µÄÅØ¶Č£ØĘäĖūĢõ¼ž±£³Ö²»±ä£©£¬“Ė·“Ó¦µÄ”÷H_____£ØĢī”°Ōö“ó”±”¢”°¼õŠ””±»ņ”°²»±ä”±£©”£
£Ø2£©CO2Öʱø¼×“¼£ŗCO2£Øg£©+3H2£Øg£©![]() CH3OH£Øg£©+H2O£Øg£©”÷H=-49.0 kJ”¤mol-1£¬ŌŚĢå»żĪŖ1 LµÄĆܱÕČŻĘ÷ÖŠ£¬³äČė1 mol CO2ŗĶ3 mol H2£¬²āµĆCO2£Øg£©ŗĶCH3OH£Øg£©ÅضČĖꏱ¼ä±ä»ÆČēĶ¼ĖłŹ¾”£
CH3OH£Øg£©+H2O£Øg£©”÷H=-49.0 kJ”¤mol-1£¬ŌŚĢå»żĪŖ1 LµÄĆܱÕČŻĘ÷ÖŠ£¬³äČė1 mol CO2ŗĶ3 mol H2£¬²āµĆCO2£Øg£©ŗĶCH3OH£Øg£©ÅضČĖꏱ¼ä±ä»ÆČēĶ¼ĖłŹ¾”£

¢ŁøĆ·“Ó¦»ÆŃ§Ę½ŗā³£ŹżKµÄ±ķ“ļŹ½ŹĒ_________”£
¢Ś0~9 minŹ±¼äÄŚ£¬øĆ·“Ó¦µÄĘ½¾ł·“Ó¦ĖŁĀŹv£ØH2£©=_________”£
¢ŪŌŚĻąĶ¬Ģõ¼žĻĀ£¬ĆܱÕČŻĘ÷µÄĢå»żĖõŠ”ÖĮ0.5 LŹ±£¬“Ė·“Ó¦“ļĘ½ŗāŹ±·Å³öµÄČČĮæ£ØQ£©æÉÄÜŹĒ_________£ØĢī×ÖÄøŠņŗÅ£©kJ”£
a. 0<Q<29.5 b. 29.5<Q<36.75
c. 36.75<Q<49 d. 49<Q<98
¢ÜŌŚŅ»¶ØĢõ¼žĻĀ£¬ĢåĻµÖŠCO2µÄĘ½ŗā×Ŗ»ÆĀŹ£Ø![]() £©ÓėLŗĶXµÄ¹ŲĻµČēĶ¼ĖłŹ¾£¬LŗĶX·Ö±š±ķŹ¾ĪĀ¶Č»ņŃ¹Ē攣
£©ÓėLŗĶXµÄ¹ŲĻµČēĶ¼ĖłŹ¾£¬LŗĶX·Ö±š±ķŹ¾ĪĀ¶Č»ņŃ¹Ē攣

i. X±ķŹ¾µÄĪļĄķĮæŹĒ_________”£
ii. ÅŠ¶ĻL1ÓėL2µÄ“󊔹ŲĻµ£ŗL1________L2£ØĢī”°<”±£¬”°=”±»ņ”°>”±£©£¬²¢¼ņŹöĄķÓÉ£ŗ_________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ°“ŅŖĒóĶź³ÉĻĀĮŠø÷Š”Ģā
£Ø1£©Š“³öNaHSO4ŌŚĖ®ČÜŅŗÖŠµÄµēĄė·½³ĢŹ½______________________________________”£
£Ø2£©ĀČ»ÆĀĮµÄĖ®ČÜŅŗ³£ĪĀŹ±³Ź_____(Ģī”°Ėį”±”¢”°ÖŠ”±”¢”°¼ī”±)ŠŌ£¬°ŃĀČ»ÆĀĮČÜŅŗÕōøÉ£¬×ĘÉÕ£¬×īŗóµĆµ½µÄ¹ĢĢå²śĪļŹĒ__________”£
£Ø3£©ŹµŃéŹŅÅäÖĘFeSO4ČÜŅŗ£¬ČܽāŹ±ĻČŅŖ¼ÓČėÉŁĮæµÄĻ”ĮņĖį£¬ĘäŌŅņŹĒ___________________(ÓĆĄė×Ó·½³ĢŹ½ŗĶŹŹµ±ĪÄ×ÖĖµĆ÷)£»ÅäÖĘĶź±ĻŗóŅŖ¼ÓČėÉŁĮæĢśŠ¼£¬ĘäÄæµÄŹĒ____________________________”£
£Ø4£©t”ꏱ£¬Ä³NaOHĻ”ČÜŅŗÖŠc(H+)=10£a mol”¤L£1£¬c(OH£)=10£b mol”¤L£1£¬ŅŃÖŖa+b=12£¬Ōņ£ŗ
¢ŁøĆĪĀ¶ČĻĀĖ®µÄĄė×Ó»ż³£ŹżKw=________________£»
¢ŚŌŚøĆĪĀ¶ČĻĀ£¬½«100mL 0.1 mol”¤L£1µÄĻ”H2SO4Óė100mL 0.4 mol”¤L£1µÄNaOHČÜŅŗ»ģŗĻŗó£¬ČÜŅŗµÄpH= _____________”£
”¾“š°ø”æ NaHSO4=Na++H++SO42- Ėį Al2O3 Fe2++2H2OFe(OH)2+2H+ ŅÖÖĘFe2+Ė®½ā ·ĄÖ¹Fe2+Ńõ»Æ 1.0”Į10-12 11
”¾½āĪö”æ£Ø1£©. NaHSO4ŹĒĒæĖįµÄĖįŹ½ŃĪ£¬ŌŚĖ®ČÜŅŗÖŠĶźČ«µēĄė£¬µēĄė·½³ĢŹ½ĪŖ£ŗNaHSO4=Na++H++SO42-£¬¹Ź“š°øĪŖ£ŗNaHSO4=Na++H++SO42-£»
£Ø2£©.AlCl3ŹĒĒæĖįČõ¼īŃĪ£¬Ė®½āŹ¹ČÜŅŗ³ŹĖįŠŌ£»Al3£«£«3H2O![]() Al(OH)3£«3H£«£¬¼ÓČČÕōøÉĀČ»ÆĀĮČÜŅŗ£¬“Ł½ųĀĮĄė×ÓµÄĖ®½ā£¬Ź¹Ę½ŗāÕżĻņŅĘ¶Æ£¬ŅņHClŅ×»Ó·¢£¬ŌņÕōøÉŗóµĆµ½Al(OH)3¹ĢĢ壬×ĘÉÕŹ±Al(OH)3·¢Éś·Ö½ā£ŗ2Al(OH)3
Al(OH)3£«3H£«£¬¼ÓČČÕōøÉĀČ»ÆĀĮČÜŅŗ£¬“Ł½ųĀĮĄė×ÓµÄĖ®½ā£¬Ź¹Ę½ŗāÕżĻņŅĘ¶Æ£¬ŅņHClŅ×»Ó·¢£¬ŌņÕōøÉŗóµĆµ½Al(OH)3¹ĢĢ壬×ĘÉÕŹ±Al(OH)3·¢Éś·Ö½ā£ŗ2Al(OH)3 ![]() Al2O3£«3H2O£¬ĖłŅŌ×ĘÉÕŗóµĆµ½Ńõ»ÆĀĮ¹ĢĢ壬¹Ź“š°øĪŖ£ŗĖį£»Al2O3£»
Al2O3£«3H2O£¬ĖłŅŌ×ĘÉÕŗóµĆµ½Ńõ»ÆĀĮ¹ĢĢ壬¹Ź“š°øĪŖ£ŗĖį£»Al2O3£»
£Ø3£©.ŹµŃéŹŅÅäÖĘFeSO4ČÜŅŗ£¬ŅņŃĒĢśĄė×Ó·¢ÉśĖ®½ā£ŗFe2++2H2O![]() Fe(OH)2+2H+£¬ŌņČܽāŹ±ĻČ¼ÓČėÉŁĮæµÄĻ”ĮņĖį£¬Ōö“óĒāĄė×ÓÅØ¶Č£¬ŅÖÖĘFe2+Ė®½ā£»ŅņFe2+ČŻŅ×±»æÕĘųÖŠµÄŃõĘųŃõ»ÆĪŖFe3£«£¬ÅäÖĘĶź±Ļŗó¼ÓČėÉŁĮæĢśŠ¼£¬æÉŅŌ·¢Éś£ŗFe£«2Fe3£«=3Fe2£«£¬“Ó¶ų“ļµ½·ĄÖ¹Fe2+±»Ńõ»ÆµÄ×÷ÓĆ£¬¹Ź“š°øĪŖ£ŗFe2++2H2O
Fe(OH)2+2H+£¬ŌņČܽāŹ±ĻČ¼ÓČėÉŁĮæµÄĻ”ĮņĖį£¬Ōö“óĒāĄė×ÓÅØ¶Č£¬ŅÖÖĘFe2+Ė®½ā£»ŅņFe2+ČŻŅ×±»æÕĘųÖŠµÄŃõĘųŃõ»ÆĪŖFe3£«£¬ÅäÖĘĶź±Ļŗó¼ÓČėÉŁĮæĢśŠ¼£¬æÉŅŌ·¢Éś£ŗFe£«2Fe3£«=3Fe2£«£¬“Ó¶ų“ļµ½·ĄÖ¹Fe2+±»Ńõ»ÆµÄ×÷ÓĆ£¬¹Ź“š°øĪŖ£ŗFe2++2H2O![]() Fe(OH)2+2H+£¬ŅÖÖĘFe2+Ė®½ā£»·ĄÖ¹Fe2+Ńõ»Æ£»
Fe(OH)2+2H+£¬ŅÖÖĘFe2+Ė®½ā£»·ĄÖ¹Fe2+Ńõ»Æ£»
£Ø4£©.¢Ł . t”ꏱ£¬Ä³NaOHĻ”ČÜŅŗÖŠc(H+)=10£a mol”¤L£1£¬c(OH£)=10£b mol”¤L£1£¬ŌņKw= c(H+)”Įc(OH£)= 10£a mol”¤L£1”Į10£b mol”¤L£1=1.0”Į10£(a+b)£¬ŅŃÖŖa+b=12£¬ŌņKw=1.0”Į10£12£¬¹Ź“š°øĪŖ£ŗ1.0”Į10£12£»
¢ŚŌŚøĆĪĀ¶ČĻĀ£¬100mL 0.1 mol”¤L£1µÄĻ”H2SO4ČÜŅŗÖŠn£ØH+£©=0.1L”Į0.1 mol”¤L£1”Į2=0.02mol£¬100mL 0.4 mol”¤L£1µÄNaOHČÜŅŗÖŠn£ØOH££©=0.1L”Į0.4 mol”¤L£1=0.04mol£¬Į½ČÜŅŗ»ģŗĻŗóĒāŃõøłĄė×Ó¹żĮ棬ĖłµĆČÜŅŗÖŠc£ØOH££©=![]() = 0.1mol/L£¬Ōņc£ØH+£©=
= 0.1mol/L£¬Ōņc£ØH+£©=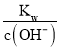 =10£11mol/L£¬ŌņpH= £lgc£ØH+£©=11£¬¹Ź“š°øĪŖ£ŗ11”£
=10£11mol/L£¬ŌņpH= £lgc£ØH+£©=11£¬¹Ź“š°øĪŖ£ŗ11”£
”¾ĢāŠĶ”æ×ŪŗĻĢā
”¾½įŹų”æ
24
”¾ĢāÄæ”æŅŃÖŖ25 ”ꏱ,²æ·ÖČõµē½āÖŹµÄµēĄėĘ½ŗā³£ŹżŹż¾ŻČēĻĀ±ķ£ŗ
ČõĖį»ÆѧŹ½ | CH3COOH | HCN | H2CO3 |
µēĄėĘ½ŗā³£Źż | 1.7”Į10£5 | 6.2”Į10£10 | K1£½4.3”Į10£7 K2£½5.6”Į10£11 |
£Ø1£©ÓĆĄė×Ó·½³ĢŹ½±ķŹ¾Na2CO3ČÜŅŗ³Ź¼īŠŌµÄŌŅņ£ŗ____________________”£
£Ø2£©µČĪļÖŹµÄĮæÅØ¶ČµÄA£®CH3COONa B£®NaCN C£®Na2CO3 D£®NaHCO3ČÜŅŗµÄpHÓɓ󵽊”µÄĖ³ŠņĪŖ____________________________________(Ģī×ÖÄø)”£
£Ø3£©ŅŃÖŖŌŚ25”ꏱ, ½«HCNČÜŅŗÓėNaOHČÜŅŗµČĢå»żµČÅØ¶Č»ģŗĻŗó,“ĖČÜŅŗÖŠĄė×ÓÅضČÓɓ󵽊”µÄĖ³ŠņŹĒ____________________________________”£
£Ø4£©³£ĪĀĻĀ£¬0.1mol”¤L£1µÄCH3COOHČÜŅŗ¼ÓĖ®Ļ”ŹĶ£¬ĻĀĮŠ±ķ“ļŹ½µÄŹż¾Ż±ä“óµÄŹĒ______”£
A£®c(H£«) B£®c(H£«)/c(CH3COOH) C£®c(H£«)”¤c(OH£)
£Ø5£©Ģå»ż¾łĪŖ10 mL ,pH¾łĪŖ2µÄ“×ĖįČÜŅŗÓėŃĪĖį·Ö±šÓė×ćĮæZn·“Ó¦£¬·“Ó¦øÕæŖŹ¼Ź±²śÉśH2µÄĖŁĀŹ£ŗv(HCl)______v(CH3COOH)£ØĢī”°£½”±”¢”°£¾”±»ņ”°£¼”±ĻĀĶ¬£©£¬·“Ó¦ĶźČ«ŗó£¬ĖłµĆĒāĘųµÄÖŹĮæ£ŗm(H2)ŃĪĖį_______m(H2)“×Ėį”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com