
| A. | 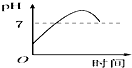 | B. | 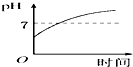 | C. |  | D. | 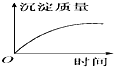 |
分析 Al2(SO4)3水解呈酸性,离子放电顺序为H+>Al3+>Na+,Cl->OH->SO42-,阳极依次发生:2Cl--2e-═Cl2↑,4OH--4e-═O2↑+2H2O;阴极发生2H++2e-=H2↑,结合相关离子的物质的量解答该题.
解答 解:混合溶液的体积为1L,
则n(Cl-)=3mol,n(Al3+)=1mol,
离子放电顺序为H+>Al3+>Na+,Cl->OH->SO42-,
阳极发生:2Cl--2e-═Cl2↑,Cl-离子全部放电,失去3mol电子,
阴极反应为2H++2e-═H2↑,得到3mol电子,生成3molOH-,
而1molAl3+与3molOH-发生Al3++3OH-═Al(OH)3↓,
剩余溶液为K2SO4,溶液呈中性,pH=7,
继续电解,为电解水,溶液pH不变,沉淀不溶解.
故选:D.
点评 本题考查电解原理,为高考常见题型,侧重于学生分析能力和计算能力的考查,注意把握离子的放电顺序,难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题

| 序号 | 试剂1 | 试剂2 | 混合前温度 | 混合后的最高温度 |
| ① | 50mL水 | 2.5g NaHCO3固体 | 20℃ | 18.5℃ |
| ② | 50mL水 | 3.2g Na2CO3固体 | 20℃ | 24.3℃ |
| ③ | 50mL稀盐酸 | 2.5g NaHCO3固体 | 20℃ | 16.2℃ |
| ④ | 50mL稀盐酸 | 3.2g Na2CO3固体 | 20℃ | 25.1℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 相同温度下,0.02 mol•L-1的醋酸溶液与0.01 mol•L-1的醋酸溶液中的c(H+)之比小于2:1 | |
| B. | 相同温度下,0.1 mol•L-1 (NH4)2SO4溶液与0.1 mol•L-1NH4NO3溶液中c(NH4+)之比大于2:1 | |
| C. | 在0.1 mol•L-1NaOH溶液中逐滴加入0.1 mol•L-1CH3COOH溶液,当溶液pH=7时,加入CH3COOH溶液的体积与NaOH溶液的体积比小于2:1 | |
| D. | 40℃时,pH=7的(NH4)2SO4与NH3•H2O的混合溶液中c(NH4+)与c(SO42-)之比小于2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 原硅酸的结构如图,若去掉氢原子后的剩余部分即SiO44-为原硅酸,其构型为正四面体,四面体顶角上的氧原子叫“角氧”.有关叙述正确的是( )
原硅酸的结构如图,若去掉氢原子后的剩余部分即SiO44-为原硅酸,其构型为正四面体,四面体顶角上的氧原子叫“角氧”.有关叙述正确的是( )| A. | 两分子原硅酸脱去一分子水得到的H6Si2O7分子中有6个Si-O键 | |
| B. | 两个硅氧四面体,彼此用一个角氧相连后,形成的Si2O76-离子中各键角均为109°28′ | |
| C. | 3个硅氧四面体彼此用3个角氧相连后,形成的Si3O96-离子呈链状 | |
| D. | n个硅氧四面体彼此用四个角氧连接后的晶体是二氧化硅 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 汽车尾气中的主要污染物是NO和CO2.为了减轻大气污染,人们提出通过以下反应来处理汽车尾气.
汽车尾气中的主要污染物是NO和CO2.为了减轻大气污染,人们提出通过以下反应来处理汽车尾气.| 时间/s | 0 | 2 | 3 | 4 | 5 |
| c(NO)/10-4mol•L-1 | 10.0 | c1 | 1.50 | 1.00 | 1.00 |
| c(CO)10-3mol•L-1 | 3.60 | c2 | 2.75 | 2.70 | 2.70 |
| 实验 序号 | T/℃ | NO初始浓 度/10-3mol•L-1 | CO初始浓 度/10-3mol•L-1 | 催化剂的比表面积/㎡•g-1 |
| ① | 350 | 1.20 | 5.80 | 124 |
| ② | 280 | 1.20 | 5.80 | 124 |
| ③ | 280 | 1.20 | 5.80 | 82 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X为负极,Y为正极 | |
| B. | 该电池工作时,X极附近溶液的碱性增强 | |
| C. | 在标准状况下,通入5.6LO2完全反应后,有1mol电子发生转移 | |
| D. | 工作一段时间后,KOH的物质的量减少 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 鉴别集气瓶中的甲烷和乙烯:移去玻璃片,分别点燃,观察火焰的颜色及是否有黑烟 | |
| B. | 检验酒精中的少量水:向酒精中加入足量生石灰 | |
| C. | 制备氯乙烷(C2H5Cl):将乙烷和氯气的混合气放在光照条件下反应 | |
| D. |  证明溴乙烷与NaOH醇溶液共热生成乙烯:用如右图所示的实验装置 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
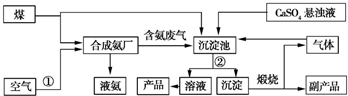
 2NH3.
2NH3. CaCO3↓+(NH4)2SO4.
CaCO3↓+(NH4)2SO4.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com