
【题目】短周期元素X、Y、Z、W、Q在元素周期表中的位置如表所示。下列说法不正确的是( )
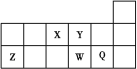
A.元素X与元素Z的最高正化合价之和的数值等于8
B.Y2-和Z3+具有相同的电子层结构
C.原子半径的大小顺序为rQ>rW>rZ>rY>rX
D.元素W的最高价氧化物对应水化物的酸性比Q的弱
【答案】C
【解析】
由元素周期表分布和题目表达可知,X为N,Y为O,Z为Al,W为S,Q为Cl。据此解答。
A. 元素X的最外层电子数为5,元素Z的最外层电子数为3,最高正化合价之和的数值等于8,A正确;
B. 氧离子最外层8个电子,铝离子最外层8个电子,电子层数均为2层,具有相同的电子层结构,B正确;
C. 同周期,原子半径随着核电荷数的增大而减小,同主族,原子半径随着核电荷数增大而增大,则原子半径的大小顺序为rZ>rW>rQ>rX>rY,C错误;
D. 同周期,随着核电荷数增大,非金属性增强,元素Q的最高价氧化物对应水化物HClO4比元素W的最高价氧化物对应水化物H2SO4的酸性强,D正确。
答案为C。


科目:高中化学 来源: 题型:
【题目】一定温度下,密闭容器中进行反应:2SO2(g)+O2(g)![]() 2SO3(g) ΔH<0。测得v正(SO2)随反应时间(t)的变化如图所示。下列有关说法正确的是( )
2SO3(g) ΔH<0。测得v正(SO2)随反应时间(t)的变化如图所示。下列有关说法正确的是( )
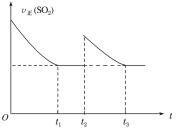
A.t2时改变的条件是:只加入一定量的SO2
B.t1时平衡常数K1大于t3时平衡常数K2
C.t1时平衡混合气体的平均相对分子质量大于t3时平衡混合气体的平均相对分子质量
D.t1时平衡混合气体中SO3的体积分数等于t3时平衡混合气体中SO3的体积分数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用粗盐(含Ca2+、Mg2+、![]() 等杂质)为主要原料采用“侯氏制碱法”生产纯碱和化肥NH4Cl,工艺流程如下图所示,下列有关说法正确的是( )
等杂质)为主要原料采用“侯氏制碱法”生产纯碱和化肥NH4Cl,工艺流程如下图所示,下列有关说法正确的是( )
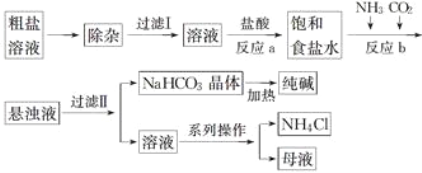
A. 在“侯氏制碱法”中涉及到了氧化还原反应
B. 饱和食盐水中先通入的气体为CO2
C. 流程图中的系列操作中一定需要玻璃棒
D. 工艺中只有碳酸氢钠加热分解产生的CO2可回收循环利用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在苯酚钠溶液中通入少量的CO2,写出反应的化学方程式:_______________;
(2)丙酸与乙醇发生酯化反应的的化学方程式:_______________;
(3)1,2—二溴丙烷发生消去反应:_______________;
(4)甲醛和新制的银氨溶液反应:_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.按系统命名法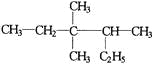 的名称为3,3—二甲基—2—乙基戊烷
的名称为3,3—二甲基—2—乙基戊烷
B.乙烯、乙炔是较活泼的有机物,能发生氧化反应,甲烷和苯性质较稳定,不能发生氧化反应
C.分子式为C5H12O的醇共有8种,其中能催化氧化成醛的同分异构体有4种
D.A、B两种有机化合物,无论以何种比例混合,只要混合物的总质量不变,完全燃烧后,产生水的质量也不变,则A、B满足的条件必须是最简式相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气是一种重要的化工原料,大量用于制造盐酸、有机溶剂、农药、染料和药品,为研究氯气,某研究性学习小组利用下列装置制取并验证氯气部分化学性质,请回答下列问题:
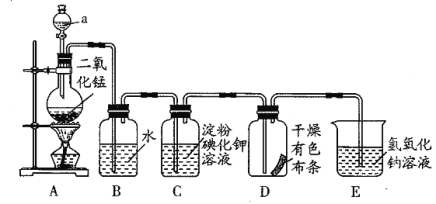
(1)装置A中,仪器a的名称为___,该装置中发生反应的化学方程式:___;34.8gMnO2完全反应生成Cl2体积为___(标准状况下)。
(2)当Cl2气流通过一段时间后,装置B中溶液的pH___(填“>”“<”或“=”)7,写出Cl2与水反应的离子方程式:___。
(3)当有少量Cl2气流通过后,观察到装置C中的溶液变为___色,反应的离子方程式为___。
(4)当Cl2气流持续通过时,装置D中干燥的有色布条能否褪色?为什么?___。
(5)装置E的作用是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】PTT是一种高分子材料,能作为纺织纤维和地毯等材料而得到广泛应用。其合成路线可设计为:
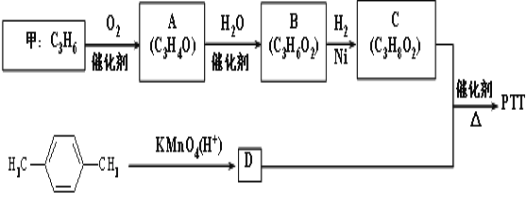
其中A、B、C均为链状化合物,A能发生银镜反应,C不含甲基,1molC可与足量钠反应生成22.4LH2(标准状况)。请回答下列问题:
(1)A的结构简式为___,C的名称___(系统命名)。
(2)1molD与足量的烧碱溶液反应最多消耗NaOH___mol。
(3)指出反应类型A→B___;C和D生成PTT___。
(4)由物质B生成C的化学方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着汽车数量的逐年增多,汽车尾气污染已成为突出的环境问题之一。反应:2NO(g)+2CO(g) ![]() 2CO2(g)+N2(g)可用于净化汽车尾气,已知该反应速率极慢,570 K时平衡常数为1×1059。下列说法正确的是 ( )
2CO2(g)+N2(g)可用于净化汽车尾气,已知该反应速率极慢,570 K时平衡常数为1×1059。下列说法正确的是 ( )
A.提高尾气净化速率的常用方法是降低温度
B.提高尾气净化速率的最佳途径是研制高效催化剂
C.装有尾气净化装置的汽车排出的气体中不再含有NO或CO
D.570 K时及时抽走CO2、N2,平衡常数将会增大,尾气净化效率更佳
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知有机物A与NaOH的醇溶液混合加热得产物C和溶液D。C与乙烯混合在催化剂作用下可反应生成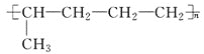 的高聚物。而在溶液D中先加入硝酸酸化,后加AgNO3溶液有白色沉淀生成,则A的结构简式可能为( )
的高聚物。而在溶液D中先加入硝酸酸化,后加AgNO3溶液有白色沉淀生成,则A的结构简式可能为( )
A. 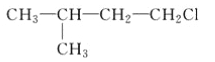 B.
B. 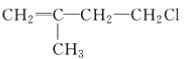 C. CH3CH2CH2ClD.
C. CH3CH2CH2ClD. 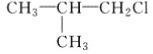
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com