
| A、6mol A+3mol B |
| B、3mol A+1mol B+4mol C |
| C、2mol C+1mol B |
| D、1mol B+3C |


科目:高中化学 来源: 题型:
| A、在氧化还原反应中,金属单质只体现还原性,金属阳离子只体现氧化性 |
| B、按金属活动性顺序,排在前面的金属一定可以把排在后面的金属从它们的盐溶液中置换出来 |
| C、考虑到成本问题,工业上将氯气通入澄清石灰水中制取漂白粉 |
| D、液态(熔融)HCl不导电,但是HCl的水溶液可以导电,所以HCl是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、液态HBr不导电,因此HBr是非电解质 |
| B、强电解质溶液的导电性不一定很强 |
| C、NH3的水溶液能导电,因此NH3是电解质 |
| D、强电解质在液态时一定能导电 |
| E、强电解质在液态时一定能导电 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、二氧化碳与苯酚钠溶液 |
| B、乙酸钠溶液与硫酸氢钠溶液 |
| C、苯酚溶液与氯化铁溶液 |
| D、氢氧化铜悬浊液与甲酸溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、F2、Cl2、Br2、I2的熔、沸点逐渐升高 |
| B、NH3易液化 |
| C、HF、HCl、HBr、HI的热稳定性依次减弱 |
| D、H2S的熔沸点低于H2O的熔、沸点 |
查看答案和解析>>
科目:高中化学 来源: 题型:
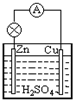 如图,在锌、铜和稀硫酸组成的原电池中,下列说法中正确的是( )
如图,在锌、铜和稀硫酸组成的原电池中,下列说法中正确的是( )| A、铜是正极 |
| B、铜电极的质量减轻 |
| C、锌电极的反应为:2H++2e-=H2↑ |
| D、锌片上发生还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 放电 |
| 充电 |
| A、电池放电时,镍元素被氧化 |
| B、电池充电时,氢元素被还原 |
| C、电池放电时,镍元素被还原 |
| D、电池充电时,H2在阴极生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、X、Y、Z的稳定性逐渐增强 |
| B、A、B、C、D只能形成四种单质 |
| C、X、Y、Z三种化合物的熔沸点逐渐升高 |
| D、只含有A、B、C、D 四种元素的化合物有两种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com