
【题目】L-多巴是一种有机物,分子式为C9H11O4N,它可用于帕金森病的治疗,其结构简式为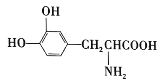 。下列关于L-多巴的叙述不正确的是( )
。下列关于L-多巴的叙述不正确的是( )
A.它属于α-氨基酸,既具有酸性,又具有碱性
B.它能与FeCl3溶液发生显色反应
C.它可以通过两分子间缩合形成分子式为C18H18O6N2的化合物,该化合物中有3个六元环
D.它既与酸反应又与碱反应,等物质的量的L-多巴最多消耗的NaOH与HC1的物质的量之比为1:1
科目:高中化学 来源: 题型:
【题目】汽车的启动电源常用铅蓄电池。其结构如图所示,放电时的电池反应为PbO2+Pb+2H2SO4=2PbSO4+2H2O。根据此反应判断下列说法正确的是( )
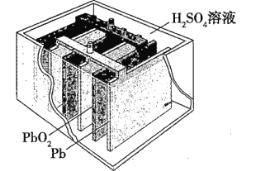
A.PbO2是电池的负极
B.Pb是电池的负极
C.PbO2得电子,被氧化
D.电池放电时,溶液的酸性增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环己烯是重要的化工原料。其实验室制备流程如下:
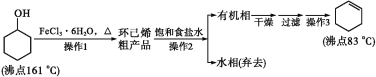
回答下列问题:
Ⅰ.环己烯的制备与提纯
(1)原料环己醇中若含苯酚杂质,检验试剂为__________,现象为____________。
(2)操作1的装置如图所示(加热和夹持装置已略去)。
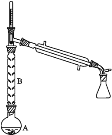
①烧瓶A中进行的可逆反应化学方程式为__________________________________,浓硫酸也可作该反应的催化剂,选择FeCl3·6H2O而不用浓硫酸的原因为___________(填序号)。
a.浓硫酸易使原料炭化并产生SO2
b.FeCl3·6H2O污染小、可循环使用,符合绿色化学理念
c.同等条件下,用FeCl3·6H2O比浓硫酸的平衡转化率高
②仪器B的作用为____________________________。
(3)操作2用到的玻璃仪器是__________________________。
Ⅱ.环己烯含量的测定
在一定条件下,向a g环己烯样品中加入定量制得的b mol Br2,与环己烯充分反应后,剩余的Br2与足量KI作用生成I2,用c mol·L-1的Na2S2O3标准溶液滴定,终点时消耗Na2S2O3标准溶液V mL(以上数据均已扣除干扰因素)。
测定过程中,发生的反应如下:
①Br2+![]() →
→![]()
②Br2+2KI=I2+2KBr
③I2+2Na2S2O3=2NaI+Na2S4O6
(4)滴定所用指示剂为__________________________。样品中环己烯的质量分数为______________________(用字母表示)。
(5)下列情况会导致测定结果偏低的是__________________(填序号)。
a.样品中含有苯酚杂质
b.在测定过程中部分环己烯挥发
c.Na2S2O3标准溶液部分被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯仿(CHCl3)常因保存不慎而被氧化,产生剧毒物光气(COCl2):2CHCl3+O2―→2HCl +2COCl2。下列说法不正确的有

A. CHCl3分子的空间构型为正四面体
B. COCl2分子中中心C原子采用sp2杂化
C. COCl2分子中所有原子的最外层电子都满足8电子稳定结构
D. 使用前可用硝酸银稀溶液检验氯仿是否变质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图中A、B、C、D、E、F、G均为有机化合物。根据如图所示转化关系回答下列问题:

(1)D的化学名称是___________________。
(2)反应③的化学方程式是______________________________________________________。
(3)B的分子式是_________,A的结构简式是_________。反应①的反应类型是_________。
(4)符合下列两个条件的B的同分异构体(不包括B)有_________种。
①与B有相同官能团且苯环上只有两个取代基 ②不与![]() 溶液发生显色反应
溶液发生显色反应
写出其中任意一种同分异构体的结构简式:_______________。
(5)反应④的化学方程式是_________________________________________________________________。G是重要的工业原料,用化学方程式表示G形成高聚物的反应:__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.在纯水中加入盐一定促进水的电离
B.同温时,等浓度的NaHCO3和Na2CO3溶液,NaHCO3溶液的pH大
C.加热CH3COONa溶液,溶液中![]() 的值将变大
的值将变大
D.0.1mol·L-1HA弱酸溶液与0.05mol·L-1NaOH溶液等体积混合,所得溶液中:2c(H+)+c(HA)=c(A-)+2c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电化学技术在工业生产中有着重要的作用。请回答:
(1)氢氧燃料电池是符合绿色化学理念的新型发电装置。如图为电池示意图,该电池电极表面镀一层细小的铂粉。铂吸附气体的能力强,性质稳定。
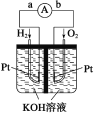
①氢氧燃料电池能量转化的主要形式是__。
②负极反应式为__。
③电极表面镀铂粉的原因是__。
(2)工业级氢氧化钾的溶液中含有某些含氧酸根杂质,可用离子交换膜法电解提纯。电解槽内装有阳离子交换膜(只允许阳离子通过),其工作原理如图所示。
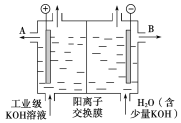
①该电解槽的阳极反应式是___。
②通电开始后,阴极附近溶液pH会增大,请简述原因___。
③除去杂质后的氢氧化钾溶液从液体出口___(填写“A”或“B”)导出。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.常温下反应C(s)+CO2 (g)2CO(g)不能自发进行,则该反应△H>0
B.自发反应的熵一定增大,非自发反应的熵一定减小
C.凡是放热反应都是自发的,凡是吸热反应都是非自发的
D.反应2Mg(s)+CO2 (g)C(s)+2MgO(s)能自发进行,则该反应△H>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某含C、H、O三种元素的有机物M的相对分子质量小于100,经燃烧分析实验测定该有机物中碳的质量分数为40%,氢的质量分数为6.7%。由此所得结论正确的是( )
A.M的分子式为CH2OB.M的实验式为CH3O
C.M不可能是2-羟基丙酸D.M可能是饱和一元羧酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com