
【题目】以下说法正确的是( )
A.干冰升华克服了分子间作用力,没有破坏共价键
B.HCl气体溶于水,形成稀盐酸,仅克服分子间作用力
C.C60与金刚石互为同素异形体,它们都属于原子晶体
D.乙醇和二甲醚分子都是C2H6O,它们是同位素
 互动英语系列答案
互动英语系列答案 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案科目:高中化学 来源: 题型:
【题目】酯化反应是有机化学中的一类重要反应,下列对酯化反应理解不正确的是 ( )。
A.酯化反应是有限度的B.酯化反应可看成取代反应的一种
C.酯化反应的产物只有酯D.浓硫酸可做酯化反应的催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2-甲基-2-己醇常用于合成洗涤剂、乳化剂等。实验室制备2-甲基-2-己醇的流程如下:
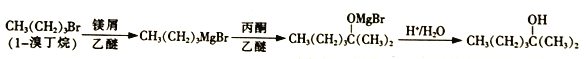
已知:RMgBr化学性质活泼,易与H2O、R'X等发生反应生成RH、R-R'。
(1)仪器A的名称是___________。
(2)引发CH3(CH2)3Br与镁屑反应可微热或加入米粒大小的碘单质,其中碘的作用可能是_____,若镁屑不足,则反应时生成的有机副产物为________(填结构简式)。

(3)干燥管中无水氯化钙的作用为__________。
(4)加入丙酮及稀硫酸时均需用冰水冷却,这是因为_________。
(5)起始加入三颈烧瓶的1-溴丁烷的体积为5mL,密度为1.28g/mL,最终所得产品的质量为2.71g,则2-甲基-2-己醇的产率为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋酸亚铬水合物[Cr(CH3COO)2]2·2H2O是一种氧气吸收剂,为红棕色晶体,易被氧化,微溶于乙醇,不溶于水和乙醚(易挥发的有机溶剂)。其制备装置及步骤如下:

①检查装置气密性,往三颈烧瓶中依次加入过量锌粉、适量CrCl3溶液。
②关闭k2打开k1,旋开分液漏斗的旋塞并控制好滴速。
③待三颈烧瓶内的溶液由深绿色(Cr3+)变为亮蓝色(Cr2+)时,把溶液转移到装置乙中,当出现大量红棕色晶体时,关闭分液漏斗的旋塞。
④将装置乙中混合物快速过滤、洗涤和干燥,称量得到2.76 g[Cr(CH3COO)2]2·2H2O。
(1)装置甲中连通管a的作用是______________________。
(2)三颈烧瓶中的Zn除了与盐酸生成H2外,发生的另一个反应的离子方程式为______________________。
(3)实验步骤③中溶液自动转移至装置乙中的实验操作为______________________。
(4)装置丙中导管口水封的目的是______________________。
(5)洗涤产品时,为了去除可溶性杂质和水分,下列试剂的正确使用顺序是________(填字母)。
a.乙醚 b.去氧冷的蒸馏水 c.无水乙醇
(6)若实验所取用的CrCl3溶液中含溶质3.17 g,则[Cr(CH3COO)2]2·2H2O(相对分子质量为376)的产率是______________________。
(7)一定条件下,[Cr(CH3COO)2]2·2H2O受热得到CO和CO2的混合气体,请设计实验检验这两种气体的存在________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示中,A为一种常见的单质,B、C、D、E是含A元素的常见化合物,它们的焰色反应均为黄色.
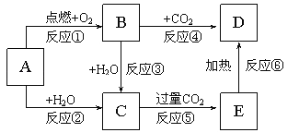
填写下列空白:
(1)写出化学式:A__________,B______________.
(2)写出反应⑤的化学反应方程式:_______________________________﹣ .
(3)写出反应⑥的化学反应方程式:_________________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列实验装置进行相应实验,能达到实验目的的是
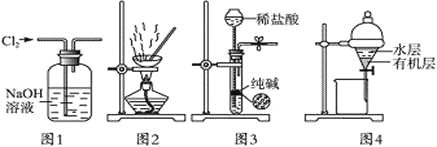
A. 用图1所示装置除去Cl2中含有的少量HCl
B. 用图2所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体
C. 用图3所示装置制取少量纯净的CO2气体
D. 用图4所示装置分离CCl4萃取碘水后已分层的有机层和水层
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学是一门以实验为基础的自然科学,化学实验在化学学习中具有重要作用。
( I )下列关于实验的叙述中正确的有______________(填字母)。
A.酒精灯使用结束后,应立即吹灭
B.不慎将酸沾到皮肤或衣物上,应立即用浓NaOH溶液清洗
C.分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出
D.取用Na2SO4溶液时,发现取量过多,为了不浪费,应把多余的试剂倒入原试剂瓶中
E.称量氢氧化钠固体时,应先在天平两个托盘上各放一张相同质量的纸,再把氢氧化钠固体放在纸上称
F.使用分液漏斗前要检查其是否漏水
G.测量溶液pH时,应先将pH试纸润湿
( II )化学家研究物质的组成和性质时,首先需要将被研究的物质从混合物中分离出来并加以提纯,以下是常见的可用于分离或提纯物质的部分仪器和方法:
仪器:

方法:① 过滤;② 结晶;③ 蒸馏;④ 萃取分液。
请将相应的字母填入空白处:
实验 | 所需仪器 | 方法 |
除去水中混有的泥沙 | _______ | _______ |
从海水中获取淡水 | _______ | _______ |
分离碘和水的混合物 | _______ | _______ |
从海水中获取粗盐 | _______ | _______ |
( III ) 实验室用63%的浓HNO3 (其密度为1.4 g·mL-1)配制480 mL 0.25 mol·L-1稀HNO3;可供选用的仪器有:
a.胶头滴管 b.烧瓶 c.烧杯 d.药匙 e.托盘天平 f.10 mL量筒 g.50 mL量筒
回答下列问题:
(1)此浓硝酸的物质的量浓度为________mol·L-1。
(2)量取63%的浓硝酸时应选用________(填仪器的字母编号)量取________mL。
(3)实验时,上述仪器中还需要选用的有_________(填字母),还缺少的仪器有_______、_____ (写仪器名称)。
(4)配制过程中,下列操作会使配制的稀硝酸溶液浓度偏低的是________________ (填序号)。
①用量筒量取浓硝酸时,眼睛俯视刻度线
②容量瓶使用时底部残留有水
③定容时眼睛俯视刻度线
④移液时不小心有少量液体洒到瓶外
⑤定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在“冰→液体水→氢气和氧气”的变化过程中,微粒间被破坏的作用力依次是( )
A.范德华力、范德华力
B.范德华力、共价键
C.共价键、范德华力
D.共价键、共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】双一(对烷氧基苯甲酸)-2,3一二氯—1,4—苯二酚酯(G)是一种新的液晶化合物,在液晶显示领域里有广泛的应用,其合成路线如下:

已知:R为烷烃基,D的核磁共振氢谱为四组峰,且峰面积之比为9:2:2:1。
回答下列问题:
(1)A的结构简式为______________________________。
(2)B的化学名称为_________________________。
(3)A与B生成C的化学方程式为_____________________________。
(4)由E生成G的反应类型为______________________。
(5)G的分子式为______________________。
(6)H是D的同分异构体,H的苯环上只有两个对位的取代基,H可与FeCl3溶液发生显色反应,且能发生水解反应和银镜反应,则H共有______种;其中核磁共振氢谱为六组峰,且峰面积之比为1:2:6:2:2:1的结构简式为_______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com