
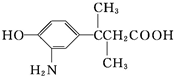
 ),下列关于A的叙述中错误的是( )
),下列关于A的叙述中错误的是( )| A. | 该物质在一定条件下能发生缩聚反应 | |
| B. | 该物质的核磁共振氢谱(1H-NMR)上共有7个峰 | |
| C. | 1 mol该物质最多能与含1 mol Br2的溴水发生取代反应 | |
| D. | 该物质能与Na、NaOH、NaHCO3、盐酸等物质反应 |
分析 由结构可知,分子中含酚-OH、氨基、-COOH,结合酚、羧酸的性质来解答.
解答 解:A.含-OH、-COOH可发生缩聚反应,氨基、-COOH可发生缩聚反应,故A正确;
B.分子中含有9种类型的H原子,共有9个峰,故B错误;
C.只有酚-OH的一个邻位可与溴水发生取代反应,1 mol该物质最多能与含1 mol Br2的溴水发生取代反应,故C正确;
D.含-COOH,能与Na、NaOH、NaHCO3反应,含氨基与盐酸反应,故D正确;
故选B.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重分析与应用能力的考查,注意酚与氨基酸的性质,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | CCl4 | B. | C2H5OH | C. | CS2 | D. | C6H6 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 质子数与中子数相等的氢原子符号${:}_{1}^{1}$H | |
| B. | 乙烯的比例模型: | |
| C. | 双氧水的电子式:${H}_{•}^{•}{\stackrel{••}{\underset{••}{O}}}_{•}^{•}{\stackrel{••}{\underset{••}{O}}}_{•}^{•}$H | |
| D. | 次氯酸的结构式:H-O-Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Ca(HCO3)2溶液中滴入过量NaOH溶液:HCO3-+Ca2++OH-═CaCO3↓+H2O | |
| B. | 向NaAlO2溶液中通入过量的CO2:CO2+2H2O+AlO2-═Al(OH)3↓+HCO3- | |
| C. | 0.01 mol•L-1 的NH4Al(SO4)2溶液与0.02 mol•L-1的Ba(OH)2溶液等体积混合:Al3++2SO42-+NH4++2Ba2++4OH-═2BaSO4↓+Al(OH)3↓+NH3•H2O | |
| D. | 向Ca(ClO)2溶液中通入过量的SO2:ClO-+SO2+H2O═HClO+HSO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 随着原子序数的递增,原子最外层电子数总是从1到8重复出现 | |
| B. | 元素的性质随着原子序数的递增而呈周期性变化 | |
| C. | 随着原子序数的递增,仅有元素的化合价出现周期性的变化 | |
| D. | 元素性质的周期性变化是仅指原子半径的周期性变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 DIDP常温下为液体,工业上常用作树脂或塑料增塑剂,密度约为0.966g•cm-3,不溶于水,易溶于有机溶剂,制备邻苯二甲酸二异癸酯(DIDP)的主要操作步骤如下(夹持和加热装置已略去):
DIDP常温下为液体,工业上常用作树脂或塑料增塑剂,密度约为0.966g•cm-3,不溶于水,易溶于有机溶剂,制备邻苯二甲酸二异癸酯(DIDP)的主要操作步骤如下(夹持和加热装置已略去): )、95.7g异癸醇及邻苯二甲酸酐;
)、95.7g异癸醇及邻苯二甲酸酐;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com