
| A. | CH3CH2CH2Br在碱性溶液中水解 | |
| B. | 甲苯在催化剂(FeBr3)作用下与Br2发生苯环上的取代反应 | |
| C. |  与NaOH的醇溶液共热反应 与NaOH的醇溶液共热反应 | |
| D. |  在催化剂存在下与H2完全加成 在催化剂存在下与H2完全加成 |
分析 A、卤代烃在碱性条件下发生的是水解反应,其实质是卤素原子被羟基取代;
B、甲苯在FeBr3存在下与液溴发生取代反应,取代的是苯环上的氢原子;
C、根据氯代烃的消去反应实质来判断;
D、苯环和碳碳双键均可以被氢气加成,完全加成即均变为单键.
解答 解:A、CH3CH2CH2Br在碱性溶液中水解得到CH3CH2CH2OH,无同分异构体,故A错误;
B、甲苯在铁粉存在下与液溴发生取代反应,可以取代苯环上的氢原子,苯环上含有三种氢原子,所得产物存在同分异构体,故B正确;
C、 与NaOH的醇溶液共热,发生消去反应生成丙烯,无同分异构体,故C错误;
与NaOH的醇溶液共热,发生消去反应生成丙烯,无同分异构体,故C错误;
D、 在催化剂存在下与H2完全加成只能得到乙苯一种产物,无同分异构体,故D错误;
在催化剂存在下与H2完全加成只能得到乙苯一种产物,无同分异构体,故D错误;
故选B.
点评 本题以加成反应与消去反应为载体,考查同分异构体、常见有机物的性质等,注意理解加成反应与消去反应的反应原理.


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:解答题
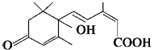 分子式为C15H20O4;
分子式为C15H20O4; 分子式C11H16
分子式C11H16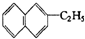 属于萘的同系物,则萘和萘的同系物分子组成通式CnH2n-12(n≥10)
属于萘的同系物,则萘和萘的同系物分子组成通式CnH2n-12(n≥10)
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
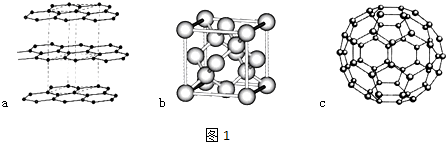
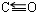 ;写出另一与CO互为等电子体的化学式CN-.
;写出另一与CO互为等电子体的化学式CN-.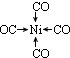 ;写出基态Ni原子的电子排布式1s22s22p63s23p63d84s2.
;写出基态Ni原子的电子排布式1s22s22p63s23p63d84s2.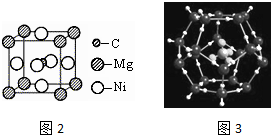
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
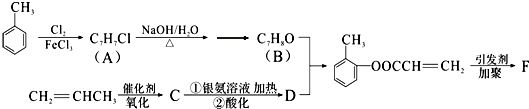
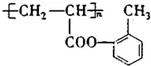
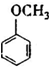 (填结构简式).
(填结构简式).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (已知乙醇的键线式为
(已知乙醇的键线式为 )
)
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
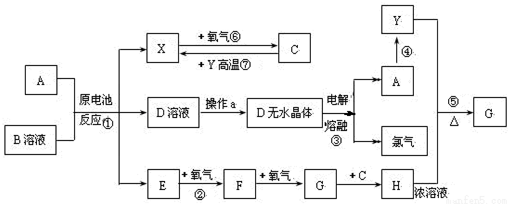

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 序号 | 滴定前读数(mL) | 滴定后读数(mL) |
| 1 | 0.00 | 20.10 |
| 2 | 1.00 | 20.90 |
| 3 | 0.00 | 22.10 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ca2+、Na+、NO3-、Fe2+ | B. | Ca2+、Na+、Fe3+、NO3- | ||
| C. | K+、Cl-、HCO3-、NO3- | D. | Mg2+、Cl-、NH4+、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
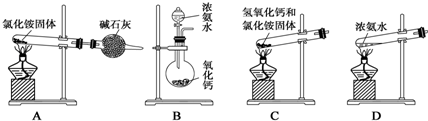
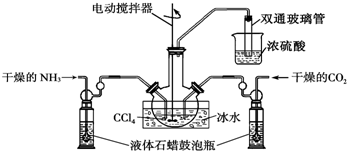
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com