
| A. | 若温度不变,容器体积缩小到原来的一半,此时A的浓度是原来的1.75倍,则a+b<c+d | |
| B. | 若温度不变,容器体积缩小到原来的一半,A的转化率可能不增大 | |
| C. | 若a+b=c+d,则对于体积不变的容器,升高温度平衡向左移动,容器中气体的压强不变 | |
| D. | 混合气体的平均相对分子质量不再变化是该反应达到平衡的标志之一 |
分析 A.容器体积缩小到原来的一半,此时A的浓度是原来的1.75倍,可知压强增大,平衡逆向移动;
B.容器体积缩小到原来的一半,平衡可能不移动或逆向移动;
C.由pV=nRT可知,温度与压强成正比;
D.均为气体,混合气体的质量不变,且气体的物质的量也可能不变.
解答 解:A.温度不变,容器体积缩小到原来的一半,相当于压强变大,平衡应向气体体积减小的方向移动,此时A的浓度变为原来的1.75倍,说明平衡向右移动了,则a+b>c+d,故A错误;
B.温度不变,容器体积缩小到原来的一半,若a+b=c+d,平衡不移动,A的转化率不改变,若a+b≠c+d,平衡移动,A的转化率一定改变,故B正确;
C.若a+b=c+d,则对于体积不变的容器,升高温度平衡向左移动,根据pV=nRT,在体积和物质的量都不改变的情况下,容器中气体的压强与温度成正比,升高温度压强变大,故C错误;
D.若a+b=c+d,混合气体的平均相对分子质量恒定不变,不能作为判断该反应达到平衡的标志,故D错误;
故选B.
点评 本题考查化学平衡移动,为高频考点,把握压强、温度对平衡移动的影响为解答的关键,侧重分析与应用能力的考查,注意平衡判定的方法,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 苹果放在空气中久置变黄和纸张久置变黄原理相似 | |
| B. | 合成洗涤剂和纯碱溶液都可洗去油污的原理相同 | |
| C. | 纤维素食用在人体内水解为葡萄糖为人体提供能量 | |
| D. | SO2具有还原性,可用已知浓度的KMnO4溶液测定食品中SO2残留量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯酚沾到手上,应立即用浓NaOH溶液清洗 | |
| B. | 酒精灯在桌上倾倒失火时,立即用湿布盖灭 | |
| C. | 点燃CO、CH4等可燃性气体前,必须检验气体的纯度 | |
| D. | 给试管里的液体加热时,液体体积一般不超过试管容积的$\frac{1}{3}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用碳酸钠溶液吸收少量二氧化硫:2CO32-+SO2+H2O=2HCO3-+HSO3- | |
| B. | 硅酸钠溶液中通人足量二氧化碳:SiO32-+2CO2+3H2O═H4SiO4↓+2HCO3- | |
| C. | 向硫酸氢钾溶液中加入Ba(OH)2溶液至刚好沉淀完全:2H++SO42-+Ba2++2OH-=2H2O+BaSO4↓ | |
| D. | 小苏打溶液中加入过量的澄清石灰水:2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 g碳燃烧生成一氧化碳时放出126.4 kJ的热量 | |
| B. | 1 mol固体碳在氧气中燃烧生成一氧化碳气体时放出126.4 kJ的热量 | |
| C. | 1 g碳燃烧生成一氧化碳时吸收126.4 kJ的热量 | |
| D. | 12 g碳和氧气反应生成一氧化碳时放出126.4 kJ的热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(Fe3+)=0.1mol/L的溶液中:K+、Mg2+、SCN-、SO42- | |
| B. | c(H+)=1mol/L的溶液中:Cu2+、Na+、ClO-、S2- | |
| C. | 能使酚酞变红的溶液中:Na+、Ba2+、NO3-、Cl- | |
| D. | pH=2的溶液中:Na+、Ag+、I-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,2.24LO2、O3的混合气体含有NA个分子 | |
| B. | 28 g CO和N2混合气体含有NA个分子 | |
| C. | 标准状况下,4.48 L水含有的分子数等于0.2NA | |
| D. | 标准状况下,CO2与Na2O2反应生成2.24 L O2转移的电子数为0.4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
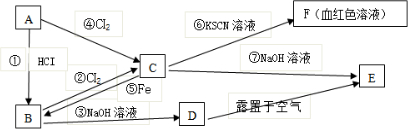
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃时,1LpH=11的氨水中OH-为0.001NA | |
| B. | 标准状况下,2.24LSO3的氧原子数为0.3NA | |
| C. | 4.6g乙醇中含有的共价键数为0.7NA | |
| D. | 3.6gD2O所含质子数为2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com