
【题目】雷雨天闪电时空气中有臭氧(O3)生成.下列说法正确的是( )
A.O2和O3互为同位素
B.O2和O3的相互转化是物理变化
C.在相同的温度与压强下,等体积的O2和O3含有相同的分子数
D.等物质的量的O2和O3含有相同的质量
 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:
【题目】锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过,下列有关叙述不正确的是( ) 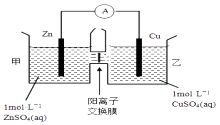
A.铜电极上发生还原反应
B.电池工作一段时间后,甲池的c(SO42﹣)不变
C.电池工作一段时间后,乙池溶液的总质量增加
D.阴阳离子离子分别通过交换膜向负极和正极移动,保持溶液中电荷平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室可用氯气和金属铁反应制备无水三氧化铁,该化合物呈棕红色、易潮解,100℃左右时升华。装置如下:
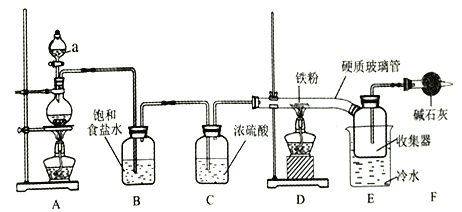
(1)仪器a的名称是________。
(2)A中反应的化学方程式是________。
(3)碱石灰的作用是________。
(4)反应开始时,先点燃_______处的酒精灯(填“A”或“D”)。
(5)D中反应开始后,收集器中有大量棕红色烟生成,反应结束后,将收集器及硬质玻璃管中的物质快速转移至锥形瓶中,加水溶解,充分反应后,加入KSCN溶液未变红色,其原因是__________。(用离子方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼酸(H3BO3)为一元弱酸,已知H3BO3与足量NaOH溶液反应的离子方程式为H3BO3+OH-=B(OH)4-,H3BO3可以通过电解的方法制备。其工作原理如下图所示(阳膜和阴膜分别只允许阳离子、阴离子通过)。下列说法错误的是( )
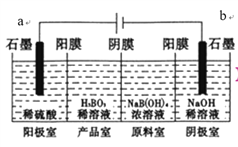
A. a与电源的正极相连接
B. 阳极的电极反应式为:2H2O-4e-=O2↑+4H+
C. 当电路中通过3mol电子时,可得到1molH3BO3
D. B(OH)4-穿过阴膜进入产品室,Na+穿过阳膜进入阴极室
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在强酸性溶液中能大量共存并且溶液为无色透明的离子组是 ( )
A.Ba2+、Na+、NO3-、SO42-B.Mg2+、Cl-、Al3+、SO42-
C.K+、Cl-、HCO3-、NO3-D.Ca2+、Na+、Fe3+、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.催化剂是化工技术的核心,绝大多数的化工生产需采用催化工艺。
(1)新的研究表明,可以将CO2转化为炭黑进行回收利用,反应原理如图所示。
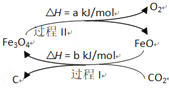
整个过程中Fe3O4的作用是________________________________。
(2)已知反应N2(g)+3H2(g)![]() 2NH3(g) ΔH<0。按n(N2)∶n(H2) = 1∶3向反应容器中投料,在不同温度下分别达平衡时,混合气中NH3的质量分数随压强变化的曲线如图所示:
2NH3(g) ΔH<0。按n(N2)∶n(H2) = 1∶3向反应容器中投料,在不同温度下分别达平衡时,混合气中NH3的质量分数随压强变化的曲线如图所示:
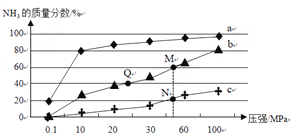
①下列说法正确的是__________。(填字母)
a.曲线a、b、c对应的温度是由低到高
b.加入催化剂能加快化学反应速率和提高H2的转化率
c.图中Q、M、N点的平衡常数:K(N)>K(Q)=K(M)
②M点对应H2的转化率是__________。
③2007年化学家格哈德·埃特尔在哈伯研究所证实了氢气与氮气在固体催化剂表面合成氨的反应过程,示意图如下:
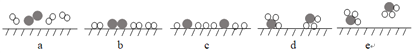
![]() 、
、![]() 和
和![]() 分别表示N2、H2和NH3。e表示生成的NH3离开催化剂表面,b和c的含义分别是____________和______________。
分别表示N2、H2和NH3。e表示生成的NH3离开催化剂表面,b和c的含义分别是____________和______________。
(3)有机反应中也常用到催化剂。某反应原理可以用下图表示,写出此反应的化学方程式_____________________________。
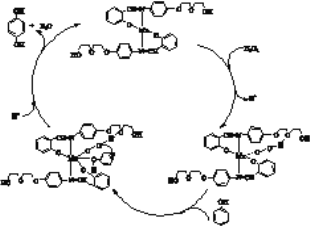
Ⅱ.过二硫酸钾(K2S2O8)在科研与工业上有重要用途。
(4)某厂采用湿法K2S2O8氧化脱硝和氨法脱硫工艺综合处理燃煤锅炉烟气,提高了烟气处理效率,处理液还可以用作城市植被绿化的肥料。一定条件下,NO去除率随温度变化的关系如图所示。80℃时,若NO初始浓度为450 mg·m-3,t min达到最大去除率,NO去除的平均反应速率:v(NO)=__________mol·L-1·Min-1(列代数式,不必计算结果)
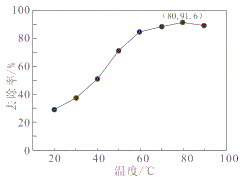
(5)过二硫酸钾可通过“电解→转化→提纯”方法制得,电解装置示意图如图所示。
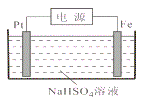
常温下,电解液中含硫微粒的主要存在形式与pH的关系如下图所示。
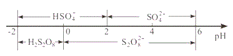
在阳极放电的离子主要是HSO4,阳极区电解质溶液的pH范围为___________,阳极的电极反应式为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.“一酸两浸,两碱联合”法是实现粉煤灰(含SiO2、Al2O3、Fe2O3、CaO、MgO等)综合利用的新工艺。聚合氯化铝铁(PAFC)化学式为:[Al2(OH)nCl6-n]m·[Fe2(OH)xCl6-x]y,是一种新型高效的净水剂。工业流程如下:

回答下列问题:
(1)实际工业中“酸浸”、“碱浸”均不能充分反应,滤渣A中主要含有SiO2、Al2O3。“纯碱混合焙烧”中,它们分别发生反应的化学方程式为_________________、_________________。
(2)滤液混合后“蒸发”的作用是________________________________。
(3)“电解”时阳极的电极反应式为________________。
(4)PAFC、无水AlCl3、FeCl3·6H2O用量均为25 mg·L-1时,处理不同pH污水的浊度去除率如图所示,PAFC的优点是___________________________。
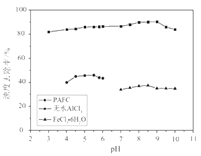
Ⅱ.(5)25℃时,用0.1mol/L的CH3COOH溶液滴定20mL0.1mol/L的NaOH溶液,当滴加VmLCH3COOH溶液时,混合溶液的pH=7。已知CH3COOH的电离平衡常数为Ka,忽略混合时溶液体积的变化,Ka的表达式为___________。
(6)常温下,测得某纯CaSO3与水形成的浊液pH为9,已知Ka1(H2SO3)=1.8×10-2,Ka2(H2SO3)=6.0×10-9,忽略SO32-的第二步水解,则Ksp(CaSO3)=_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】朱自清在《荷塘月色》中写道:“薄薄的青雾浮起在荷塘里……月光是隔了树照过来的,高处丛生的灌木,落下参差的斑驳的黑影……”月光穿过薄雾形成的种种美景本质原因是
A.雾是一种胶体B.空气中的小水滴颗粒的布朗运动
C.发生丁达尔现象D.空气中的小水滴颗粒直径大小约为1~100 nm
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】光刻胶的一种合成路线如下:
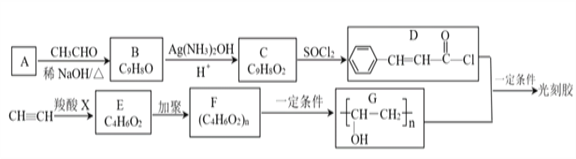
已知:
I.![]()
II.![]()
III.RCOOH+CH![]() CH
CH![]() RCOOCH=CH2
RCOOCH=CH2
回答下列问题
(1)A的名称是______。C中含氧官能团的结构简式是______。C→D的反应类型是_______。
(2)B和银氨溶液反应的离子方程式为__________________________。
(3)D+G→光刻胶的化学方程式为_______________________________________。
(4)T是C的同分异构体,T具有下列性质或特征:①能发生水解反应和银镜反应;②能使溴的四氯化碳溶液褪色;③属于芳香族化合物。则T的结构有____种。其中核磁共振氢谱为5组峰,且峰面积比为1∶1∶2∶2∶2的结构简式为_______(任写一种)。
(5)根据已有知识并结合相关信息,写出以CH3CH2OH为原料制备CH3CH2CH2COOH的合成路线流程图(无机试剂任用)。(合成路线流程图示例如下:CH2=CH2![]() CH3CH2Br
CH3CH2Br![]() CH3CH2OH)___________
CH3CH2OH)___________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com