
(10分)实验室需要标准状况下11.2L的CO2,现用CaCO3与250ml足量稀盐酸反应,问:
(1)至少需要CaCO3多少克?
(2)生成CaCl2的物质的量浓度是多少?(假设反应前后溶液体积保持不变)
 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2012届安徽省马鞍山市高三第一次教学质量检测理科综合试卷化学部分(解析版) 题型:填空题
(14分)KCIO3在农业上用作除草剂,超细CaCO3广泛用于生产牙膏、无炭复写纸等。某同学在实验室模拟工业生产,利用制乙炔产生的残渣制备上述两种物质,过程如下:
I.残渣中主要成分是Ca(OH)2和 。
II.将I中的部分灰浆配成浊液,通入Cl2在一定的温度下只得到Ca(ClO3)2与CaCl2两种溶质,该反应的化学方程式是 。
Ⅲ、向II所得溶液中加入KCl,发生复分解反应,经蒸发浓缩,冷却结晶,过滤得49.0克KClO3晶体,则理论上至少需要标准状况下Cl2 升。
Ⅳ、将I中的残渣溶于NH4Cl溶液,加热,收集挥发出的气体再利用。向所得CaCl2溶液中依次通入NH3、CO2,便可获得超细CaCO3,过程如下: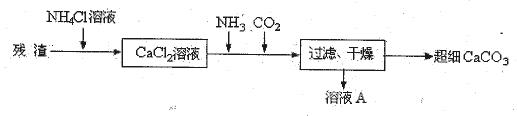
①根据沉淀溶解平衡原理,解释残渣中难溶盐的溶解原因 。
②CaCl2溶液中通入两种气体后,生成超细CaCO3的化学方程式是 。
③图示的溶液A可循环使用,其主要成分的化学式是 。
查看答案和解析>>
科目:高中化学 来源:2014届福建省高一上学期期中考试化学试卷 题型:计算题
(10分)实验室需要标准状况下11.2L的CO2,现用CaCO3与250ml足量稀盐酸反应,问:
(1)至少需要CaCO3多少克?
(2)生成CaCl2的物质的量浓度是多少?(假设反应前后溶液体积保持不变)
查看答案和解析>>
科目:高中化学 来源: 题型:
(10分)实验室需要标准状况下11.2L的CO2,现用CaCO3与250ml足量稀盐酸反应,问:
(1)至少需要CaCO3多少克?
(2)生成CaCl2的物质的量浓度是多少?(假设反应前后溶液体积保持不变)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com