
【题目】下面是几种有机化合物的转换关系:

请回答下列问题:
(1)根据系统命名法,化合物A的名称是__________。
(2)上述框图中,①是__________反应,③是__________反应(填反应类型)。
(3)化合物E是重要的工业原料,写出由D生成E的化学方程式:______________________。
(4)C2的结构简式是_________________________________,F1的结构简式是__________________________________________,F1和F2互为______________。
【答案】2,3-二甲基丁烷 取代 加成 

 同分异构体
同分异构体
【解析】
烷烃A与氯气发生取代反应生成卤代烃B,B发生消去反应生成C1、C2,C2与溴发生加成反应生成二溴代物D,D再发生消去反应生成E,E与溴可以发生1,2-加成或1,4-加成,故C2为![]() ,C1为
,C1为![]() ,则D为
,则D为 ,E为
,E为![]() ,F1为
,F1为 ,F2为
,F2为 ;
;
(1)根据系统命名法,化合物A的名称是:2,3-二甲基丁烷;
(2)上述反应中,反应①中A中H原子被Cl原子取代生成B,属于取代反应,反应③是碳碳双键与溴发生加成反应;故答案为:取代,加成;
(3)由D生成E是卤代烃发生消去反应,该反应的化学方程式为: ;
;
(4)由上述分析可知,C2的结构简式是![]() ,F1的结构简式是
,F1的结构简式是 ,F1和F2分子式相同,碳碳双键物质不同,属于同分异构体。
,F1和F2分子式相同,碳碳双键物质不同,属于同分异构体。


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
【题目】按要求填空![]() 均用序号表示
均用序号表示![]() :
:
①O2和O3②一氯甲烷和二氯甲烷 ③正丁烷和异丁烷④CH4和![]() ⑤CH3CH2CH(CH3)2和
⑤CH3CH2CH(CH3)2和 ⑥氕、氘和氚⑦C2H5C
⑥氕、氘和氚⑦C2H5C![]() CCH3和
CCH3和![]() ⑧CH2=CH2和
⑧CH2=CH2和![]() ,⑨红磷和白磷。
,⑨红磷和白磷。
(1)互为同分异构体的是 ______ ;
(2)互为同系物的是 ______ ;
(3)实际上是同种物质的是 ______ ;
(4)互为同素异形体的是 ______
(5)互为同位素的是 ______ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.2H和3H互为同位素B.O2和O3互为同素异形体
C.CH3CH2OH 和CH3OCH3互为同分异构体D.C2H2和C6H6互为同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通常人们把拆开1 mol某化学键所吸收的能量看成该化学键的键能。现给出化学键的键能(见下表):

计算H2(g)+ Br2(g)===2HBr(g)的反应热 ( )
A. +103 kJ·mol-1 B. +679 kJ·mol-1
C. -103 kJ·mol-1 D. +183 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaOH和盐酸都是中学化学常见的试剂。
Ⅰ.某同学用0.200 0 mol·L-1标准盐酸滴定待测烧碱溶液浓度
(1)将5.0 g烧碱样品(杂质不与酸反应)配成250 mL待测液,取10.00 mL待测液,如图是某次滴定时的滴定管中的液面,其读数为________ mL。

(2)由下表数据得出NaOH的百分含量是________。
滴定次数 | 待测NaOH溶液体积(mL) | 标准盐酸体积 | |
滴定前的刻度(mL) | 滴定后的刻度(mL) | ||
第一次 | 10.00 | 0.40 | 20.50 |
第二次 | 10.00 | 4.10 | 24.00 |
Ⅱ.氧化还原滴定实验与酸碱中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。测血钙的含量时,进行如下实验:
①可将2 mL血液用蒸馏水稀释后,向其中加入足量草酸铵(NH4)2C2O4晶体,反应生成 CaC2O4沉淀,将沉淀用稀硫酸处理得H2C2O4溶液。
②将①得到的H2C2O4溶液,再用酸性KMnO4溶液滴定,氧化产物为CO2,还原产物为Mn2+。
③终点时用去20 mL l.0×l0﹣4 mol/L的KMnO4溶液。
(1)写出用KMnO4滴定H2C2O4的离子方程式_____________________。
(2)滴定时,将KMnO4溶液装在________(填“酸式”或“碱式”)滴定管中。
(3)判断滴定终点的方法是________________________。
(4)误差(填“偏高”、“偏低”或“无影响”)
①如果滴定管用蒸馏水洗后未用酸性KMnO4标准液润洗,则测量结果________。
②滴定前后读数都正确,但滴定前有气泡,而滴定后气泡消失,则测量结果________。
(5)计算:血液中含钙离子的浓度为________mol/L。
Ⅲ.50 mL 0.50 mol·L-1盐酸与50 mL 0.55 mol·L-1NaOH溶液测定计算中和反应的反应热。回答下列问题:

(1)从实验装置上看,图中缺少的一种玻璃用品是__________。如改用0.0275 mol NaOH固体与该盐酸进行实验,则实验中测得的“中和热”数值将________(填“偏大”、“偏小”或“无影响”)。
(2)已知盐酸和NaOH稀溶液发生中和反应生成0.1 mol H2O时,放出5.73 kJ的热量,则表示该反应中和热的热化学方程式为:___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中华民族历史悠久,在浩瀚的历史文明中有许多关于化学的记载,下列说法不合理的是( )
选项 | 古代文献 | 记载内容 | 涉及原理 |
A | 《淮南万毕术》 | “曾青得铁则化为铜” | 活泼金属置换不活泼金属 |
B | 《鹤林玉露·一钱斩吏》 | “一日一钱,千日千钱,绳锯木断,水滴石穿” | 不涉及化学变化 |
C | 《天工开物》 | “凡火药,硫为纯阳,硝为纯阴” | 纯阴指化合价降低,利用硝酸钾的氧化性 |
D | 《肘后备急方》 | “青蒿一握,以水二升渍,绞取汁” | 利用物理方法提取青蒿素 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】国际计量大会第26次会议新修订了阿伏加德罗常数(NA=6.02214076×1023mol-1),并于2019年5月20日正式生效。下列说法正确的是( )
A. 56g聚乙烯分子中含碳碳双键的数目为2 NA
B. 核聚变如21H+31H―→42He+10n,由于有新微粒生成,该变化是化学变化
C. 铅蓄电池放电时负极净增质量比正极净增质量多16g时转移电子数为NA
D. 1L0.5mlol·L-1Al2Fe(SO4)4溶液中阳离子数目小于1.5 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化材料具有高硬度、高强度、高韧性、极高的耐磨性及耐化学腐蚀性等优良的物化性能。以锆英石(主要成分为 ZrSiO4,含有少量Al2O3、SiO2、Fe2O3等杂质)为原料通过碱熔法制备氧化锆(ZrO2)的流程如下:
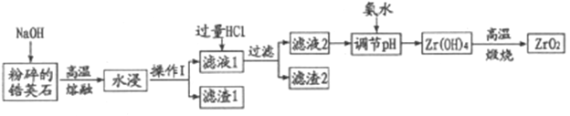
25℃时,有关离子在水溶液中沉淀时的pH数据:
Fe(OH)3 | Zr(OH)4 | Al(OH)3 | |
开始沉淀时pH | 1.9 | 2.2 | 3.4 |
沉淀完全时pH | 3.2 | 3.2 | 4.7 |
请回答下列问题:
(1)流程中旨在提高化学反应速率的措施有___________。
(2)操作I的名称是___________滤渣2的成分为___________。
(3)锆英石经“高温熔融”转化为Na2ZrO3,写出该反应的化学方程式:___________。
(4)“调节pH”时,合适的pH范围是___________。为了得到纯的ZrO2,Zr(OH)4需要洗涤,检验Zr(OH)4是否洗涤干净的方法是___________。
(5)写出“高温煅烧”过程的化学方程式___________。根据ZrO2的性质,推测其两种用途___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对阿伏加德罗定律及推论的理解不正确的是( )
A.同温同压下,气体的体积之比等于它们的物质的量之比
B.同温同压下,气体的体积之比等于它们的质量之比
C.同温同压下,相同体积的气体质量比等于它们的相对分子质量之比
D.同温同压下,气体的密度之比等于它们的相对分子质量之比
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com