
| 选项 | A | B | C | D |
| 晶体名称 | 碘化钾 | 干冰 | 硫 | 碘 |
| 晶体中的微粒名称 | 阴、阳离子 | 分子 | 原子 | 分子 |
| 晶体内存在的结合力 | 离子键 | 范德华力 | 共价键 | 范德华力 |
| A. | A | B. | B | C. | C | D. | D |
科目:高中化学 来源: 题型:选择题
| A. | ①>②>③>⑤>④ | B. | ②>③>⑤>④>① | C. | ③>①>②>⑤>④ | D. | ④>⑤>②>①>③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 一定温度下,在2L的密闭容器中,A、B、D三种气体的物质的量随时间变化的曲线如图所示.下列表述正确的是( )
一定温度下,在2L的密闭容器中,A、B、D三种气体的物质的量随时间变化的曲线如图所示.下列表述正确的是( )| A. | 反应的化学方程式为A(g)+B(g)?D(g) | |
| B. | 反应开始到10s,用B表示的反应速率为0.079mol/(L•s) | |
| C. | 在10s时,D的体积分数为71.8% | |
| D. | 反应开始到10s时,A的转化率为79% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含C=C的物质一定是烯烃 | B. | 最简式为C3H6的物质一定是丙烯 | ||
| C. | CH≡CCH2Cl属于不饱和烃 | D. | 烯烃中一定含C=C |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 烯类化合物 | 相对速率 |
| (CH3)2C=CHCH3 | 10.4 |
| CH3CH=CH2 | 2.03 |
| CH2=CH2 | 1.00 |
| CH2=CHBr | 0.04 |
 与HBr反应的主要产物的结构简式
与HBr反应的主要产物的结构简式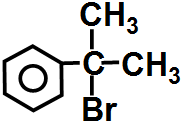 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(H+)=1×10-7mol•L-1的溶液 | |
| B. | pH=pOH 的溶液 | |
| C. | pH=14-pOH 的溶液 | |
| D. | 浓度均为0.1 mol•L-1的一元酸与氢氧化钠溶液等体积混合 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蒸馏常用于分离提纯液态有机混合物 | |
| B. | 燃烧法是研究确定有机物成分的有效方法 | |
| C. | 1H核磁共振谱通常用于分析有机物的相对分子质量 | |
| D. | 对有机物分子红外光谱图的研究有助于确定有机物分子中的官能团 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com