
 ��ͼ�ס����ǵ绯ѧʵ��װ�ã�
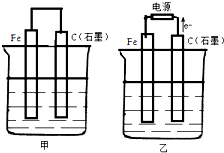
��ͼ�ס����ǵ绯ѧʵ��װ�ã����� ��1����Ϊԭ��أ���̼FeCl3ԭ����У�FeΪ������Fe�������ӷ�Ӧ�����������ӣ���̼CuSO4��Һԭ����У�FeΪ������Feʧ���������������ӣ�
��2����Ϊ���أ��ݵ��������֪��CΪ������FeΪ�������ݵ����غ���д������KI��Ӧ�����ӷ���ʽ��
��3���������ͭ��Һʱ��������ӦΪ4OH--4e-=O2��+4H2O��������ӦΪCu2++2e-=Cu���ܷ���ʽΪ2CuSO4+2H2O$\frac{\underline{\;ͨ��\;}}{\;}$2Cu+O2��+2H2SO4���Դ˽����⣮
��� �⣺��1����Ϊԭ��أ���̼FeCl3ԭ����У�FeΪ������Fe�������ӷ�Ӧ�����������ӣ����ӷ���ʽΪFe+2Fe3+=3Fe2+����̼CuSO4��Һԭ����У�FeΪ������Feʧ���������������ӣ������ϵĵ缫��ӦʽΪFe-2e-=Fe2+���ʴ�Ϊ��Fe+2Fe3+=3Fe2+��Fe-2e-=Fe2+��
��2����Ϊ���أ��ݵ��������֪��CΪ������FeΪ�������μӷ�Ӧ��Cl2��KI�����ʵ���֮��Ϊ3��1����������ԭ��Ӧ�е�ʧ�����غ㣬��Ӧ�����ӷ���ʽΪI-+3Cl2+3H2O=IO3-+6H++6Cl-���ʴ�Ϊ��������I-+3Cl2+3H2O=IO3-+6H++6Cl-��
��3�����ҳ��еĵ缫������0.640gCuʱ��n��Cu��=$\frac{0.64g}{64g/mol}$=0.01mol�����ܷ���ʽ2CuSO4+2H2O$\frac{\underline{\;ͨ��\;}}{\;}$2Cu+O2��+2H2SO4��֪����0.01molH2SO4��
��c��H+��=$\frac{0.02mol}{0.2L}$=0.1mol/L��pH=1����Ҫʹ��Һ�ָ������ǰ��״̬������������Һ�м���0.01molCuO��������Ϊ0.01mol��80g/mol=0.8g��
�ʴ�Ϊ��1��0.8��CuO��
���� ���⿼��ԭ��غ͵���֪ʶ��������ѧ���ķ������������������͵绯ѧ֪ʶ���ۺϿ��飬Ϊ�߿��������ͺ�Ƶ���㣬ע����յ缫����ʽ����д���ѶȲ���


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
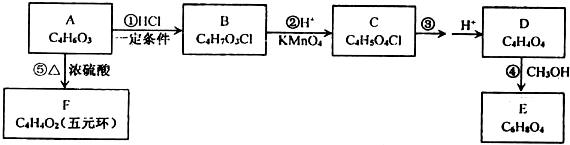
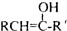 ��R�� R�䣬��������� H�����ȶ�����������ʾ������Ǵ���ṹ��
��R�� R�䣬��������� H�����ȶ�����������ʾ������Ǵ���ṹ�� 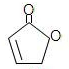 E����ʽ����
E����ʽ����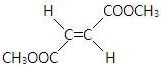
 ��
��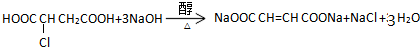 ��
�� ��
��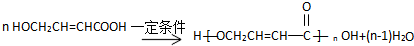 ��
��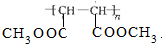 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
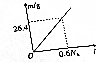 ij�����������������Ӹ�����N���Ĺ�ϵ��ͼ��ʾ����NAΪ�����ӵ�������ֵ��������������Ϊ��������
ij�����������������Ӹ�����N���Ĺ�ϵ��ͼ��ʾ����NAΪ�����ӵ�������ֵ��������������Ϊ��������| A�� | CO | B�� | CO2 | C�� | CH4 | D�� | SO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
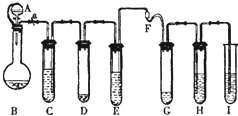 ����ѧ����ŵʵ�顱�����÷�Ӧ�����������ѹ���ͺ�������ԭ����ʹ���ɻ�ѧʵ�����η�������������ֻ����Ƶ�һ����Ӧ���ͺ������ŵ������Ϸһ������ͼ��һ������ѧ����ŵʵ�顱����װ�����Լ������ʣ�
����ѧ����ŵʵ�顱�����÷�Ӧ�����������ѹ���ͺ�������ԭ����ʹ���ɻ�ѧʵ�����η�������������ֻ����Ƶ�һ����Ӧ���ͺ������ŵ������Ϸһ������ͼ��һ������ѧ����ŵʵ�顱����װ�����Լ������ʣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
 ��
�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | HClO��HCl | B�� | NH4Cl��HCl | C�� | NH4Cl��HClO | D�� | NH4Cl��HClO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.01mol | B�� | 1g | C�� | 4 | D�� | 0.02mol |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com