
下列说法不正确的是
A.1 mol 氧气中含有12.04×1023个氧原子,在标准状况下占有体积22.4 L
B.1 mol臭氧和1.5 mol氧气含有相同的氧原子数
C.等体积、浓度均为1 mol·L-1的磷酸和盐酸,含有的氢元素质量之比为3∶1
D.等物质的量的干冰和葡萄糖(C6H12O6)中所含碳原子数之比为1∶6,氧原子数之比为1∶3
科目:高中化学 来源:2016届江西省新余、 万载、宜春三校高三上学期10月联考化学试卷(解析版) 题型:选择题
设NA表示阿伏加德罗常数的数值,下列说法正确的是
A.0.1 mol Na2O2中含有的阴离子数为0.2NA
B.标准状况下,由H2O2制得2.24LO2转移的电子数目为0.4NA
C.常温下,1 L pH=2的H2SO4溶液中含有的H+数目为0.02NA
D.常温常压下,8gO3含有4 NA个电子
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高一上第一次月考化学试卷(解析版) 题型:选择题
把VL含有MgSO4和K2SO4的混合溶液分成两等份,一份加入含a mol NaOH的溶液,恰好使Mg2+完全沉淀为氢氧化镁;另一份加入含b mol BaCl2的溶液,恰好使SO42-完全沉淀为硫酸钡,则原混合溶液中K+的浓度为mol﹒L-1。
A.(b-a)/V B.(2b-a)/V C.2(b-a)/V D.2(2b-a)/V
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江嘉兴一中高一上10月阶段测化学卷 (解析版) 题型:选择题
据《科学》杂志报道:科学家们已大量制造出反物质中的反氢原子,认为反物质研究领域的前景“正前所未有的光明”。反原子原子核和核外电子电性与原子的电性刚好相反……假若发现反氯离子,请运用核外电子排布规律大胆设想反氯离子的结构示意图
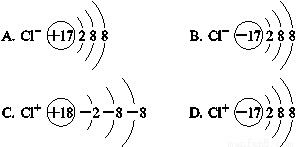
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江嘉兴一中高一上10月阶段测化学卷 (解析版) 题型:选择题
氯化铁溶液与氢氧化铁胶体具有的共同性质是
A.两者的本质区别是氢氧化铁胶体能产生丁达尔现象。
B.都能透过半透膜
C.都是透明的澄清液体
D.都呈红褐色
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江嘉兴一中高一上10月阶段测化学卷 (解析版) 题型:选择题
2.16g X2O5中含有0.1mol氧原子,则X的相对原子质量为
A.21.6 B.28 C.14 D.31
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江省龙东南四校高一下学期期末联考化学试卷(解析版) 题型:填空题
(13分)现有部分短周期元素的性质或原子结构如下表:
元素编号 | 元素性质或原子结构 |
T | M层的电子数为K层电子数的3倍 |
X | 其氢化物的空间构型为正四面体 |
Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
Z | 元素最高正价是+7价 |
(1)元素T的阴离子的结构示意图 ;元素X的最高价氧化物的电子式 ;
(2)元素Y 在周期表中位于 周期, 族。该元素的最高价氧化物对应水化物与其氢化物能生成盐M,M中含有的化学键类型有 ;
(3)四种元素最高价氧化物对应的水化物中酸性最强的是 (填物质化学式)
(4)元素Z与元素T相比,非金属性较强的是 (用元素符号表示),下列表述中能证明这一事实的是
a. 常温下Z的单质和T的单质状态不同
b. Z的氢化物比T的氢化物稳定
c. Z的最高价氧化物所对应的水化物比T的最高价氧化物所对应的水化物的酸性强
d. Z的氢化物比T的氢化物溶解度大
e. Z的单质与H2化合比 T的单质与H2化合更容易
(5)含有34个电子的元素X的氢化物的分子式
(6)写出实验室制备Z单质的化学方程式:
(7)比较T和Z的简单离子的半径大小: (用元素离子符号表示)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江省龙东南四校高一下学期期末联考化学试卷(解析版) 题型:选择题
已知短周期元素的离子,aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述正确的是

A.原子半径A >B>C> D B.原子序数 A >B>C> D
C.离子半径C>D>B>A D.单质的还原性A>B>D>C
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南湘潭、岳阳一中高一上联考化学试卷(解析版) 题型:实验题
掌握仪器名称、组装及使用方法是中学化学实验的基础,下图为两套实验装置。
(1)写出下列仪器的名称: b.
(2)利用装置I分离四氯化碳和酒精的混合物时,冷凝水由 (填f或g)口通入。
(3)现需配制0.1mol/LNaOH溶液500mL,装置II是某同学转移溶液的示意图。
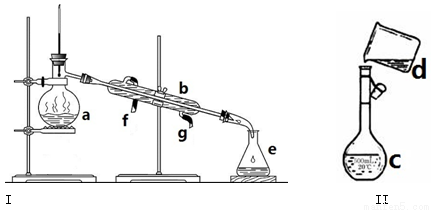
①图中的错误是 。
②配制溶液时,其正确的操作顺序是(用字母表示,每个字母只能用一次) ________。
A.将容量瓶盖紧,振荡,摇匀
B.改用胶头滴管加水,使溶液凹面恰好与刻度相切
C.继续往容量瓶内小心加水,直到液面接近刻度2~3cm处
D.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶
E.将溶解的氢氧化钠溶液沿玻璃棒注入500mL的容量瓶中
F.准确称取计算量的氢氧化钠固体于烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解
③配制溶液时下列操作会造成所配溶液浓度偏小的是( )
A.称量后转移固体时不小心把少量固体洒到烧杯外
B.干净的容量瓶又用蒸馏水洗涤了一遍
C.转移过程中不小心把几滴溶液滴在外面
D.加水定容时,俯视容量瓶刻度线读数
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com