
下列有机物中,只含有一种官能团的是
A.氯乙烯 B.苯 C.甲苯 D.乙炔
科目:高中化学 来源:2014-2015山东省菏泽市高一上学期期末考试化学A试卷(解析版) 题型:选择题
对下列实验现象的解释正确的是
现 象 | 解 释 | |
A | Na2O2 投入到 FeCl2 溶液中得到大量红褐色沉淀 | Na2O2 具有还原性 |
B | 浓硝酸在光照条件下变黄 | 浓硝酸不稳定,生成的有色产物能溶于浓硝酸 |
C | 向某溶液中加入硝酸酸化的氯化钡溶液,有白色沉淀生成 | 说明该溶液中含有SO42- |
D | 向盐酸中加入浓硫酸时产生白雾 | 说明浓硫酸具有脱水性 |
查看答案和解析>>
科目:高中化学 来源:2014-2015江西省高一上学期期末化学试卷(解析版) 题型:选择题
在下列溶液中,各组离子一定能够大量共存的是
A.使酚酞变红的溶液:Na+ Cl- SO42- AlO2-
B.某无色溶液:CO32- NO3- Al3+ Ba2+
C.加入Al能放出H2的溶液中 NH4+、Cl-、Na+、SO42-
D.酸性溶液中: NO3-、SO32-、Na+、Fe3+
查看答案和解析>>
科目:高中化学 来源:2014-2015江西省高二上学期期末化学试卷(解析版) 题型:选择题
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.pH=1的溶液中:Fe2+、NO3-、SO42-、Na+
B.无色溶液中:K+、Fe3+、SO42-、H+
C.c (H+)/c (OH-) = 1012 的溶液中:NH4+、Al3+、NO3-、Cl-
D.由水电离的c (H+)=1×10-14 mol/L的溶液中:Ca2+、K+、Cl-、HCO3-
查看答案和解析>>
科目:高中化学 来源:2014-2015江西省高二上学期期末化学试卷(解析版) 题型:选择题
已知Zn(OH)2的溶度积常数为1.2×10-17,则Zn(OH)2在水中物质的量浓度为
A.1.4×10-6mol·L-1 B.3.0×10-6mol·L-1
C.1.4×10-9mol·L-1 D.3.0×10-9mol·L-1
查看答案和解析>>
科目:高中化学 来源:2014-2015江苏省高二上学期期末考试化学试卷(解析版) 题型:填空题
(15分)通常人们把拆开1mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可以估算化学反应的反应热(△H)化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。
Si—O | Si—Cl | H—H | H—Cl | Si—Si | Si—C | |
键能/kJ·mol-1 | 460 | 360 | 436 | 431 | 176 | 347 |
请回答下列问题:
(1)比较下列两组物质的熔点高低(填“>”或“<”)
SiCl4 SiO2;Si SiC
(2)下图每个“●”表示硅晶体中的一个硅原子,每个硅原子与Si—Si键数之比为_____________,属于_________晶体。
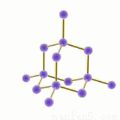
(3)工业上所用的高纯硅可以通过下列反应制备得到:SiCl4(g)+2H2(g) =Si(s)+4HCl(g);
根据此方程式并结合上述表格中数据可计算出此反应的△H=+236KJ.mol-1,请判断该反应是 反应(填“吸热”或“放热”)。
查看答案和解析>>
科目:高中化学 来源:2014-2015江苏省高二上学期期末考试化学试卷(解析版) 题型:选择题
下列说法正确的是
A.分子晶体的熔点比金属晶体的低
B.在晶体中只要有阳离子,一定有阴离子
C.在SiO2晶体中,Si原子与Si—O键数目比为1:2
D.离子化合物中可能含有非极性共价键
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高三3月阶段测试理综化学试卷(解析版) 题型:选择题
下列说法正确的是
A.淀粉、纤维素和油脂都属于天然高分子化合物
B.蛋白质溶液中加入硫酸铜溶液,有白色沉淀产生,加水,白色沉淀重新溶解
C.等质量的CH4、C2H4、C2H2分别在氧气中完全燃烧,消耗氧气的量依次减少
D.分子式为C2H4O2与C4H8O2的两种物质一定属于同系物
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省兰州市高三下学期诊断考试理综化学试卷(解析版) 题型:填空题
[化学—选修3:物质结构与性质](15分)
在周期表中1~36号之间的A、B、C、D、E、F六种元素,它们的原子序数依次增大,已知A与其余五种元素既不同周期也不同主族,B的一种核素在考古时常用来鉴定一些文物的年代,C元素原子的最外层有3个自旋方向相同的未成对电子,D原子核外电子有8种不同的运动状态,E元素在第四周期,E的基态原子中未成对电子数是核外电子总数的1/4,F元素位于周期表的ds区,其基态原子最外能层只有一个电子。
(1)写出基态E原子的价电子排布式 。
(2)B、C、D三种元素第一电离能由小到大的顺序为 (用元素符号表示)。
(3)A与C形成CA3型分子,分子中C原子的杂化类型为 ,分子的立体结构为 ;C的单质与化合物BD是等电子体,根据等电子体原理,写出化合物BD的电子式 。
(4)A2D的沸点在同族元素中最高,其原因是 。A2D由液态形成晶体时密度 (填“增大”、“不变”或“减小”),其主要原因 (用文字叙述)。
(5)已知D、F能形成一种化合物,其晶胞的结构如图所示,则该化合物的化学式为 (用元素符号表示);若相邻D原子和F原子间的距离为a cm,阿伏伽德罗常数为NA,则该晶体的密度为 g·cm-3(用含a、NA的符号表示)。
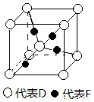
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com