
”¾ĢāÄæ”æ·ÖĪöŹµŃéÖŠ³öĻÖĻĀĮŠĻÖĻó¶ŌĖłÅäČÜŅŗµÄÅضČÓŠŗĪÓ°Ļģ£ŗ
£Ø1£©¢ŁÅØĮņĖįČܽāŗóĪ“ĄäČ“ÖĮŹŅĪĀ¼“×ŖŅĘÖĮČŻĮæĘæÖŠ½ųŠŠ¶ØČŻ£¬£ØĢī”°Ę«øß”±”¢”°Ę«µĶ”±»ņ”°ĪŽÓ°Ļģ”±£©£»
¢Ś¶ØČŻŹ±ŃöŹÓæĢ¶ČĻߣ¬£»Ģī”°Ę«øß”±”¢”°Ę«µĶ”±»ņ”°ĪŽÓ°Ļģ”±£©£»
¢ŪĮæČ”ŗĆÅØĮņĖįµ¹ČėÉÕ±Čܽāŗó£¬ÓĆĖ®Ļ“µÓĮæĶ²2”«3“Ī£¬½«Ļ“µÓŅŗµ¹ČėÉÕ±ÖŠ£¬ £® £ØĢī”°Ę«øß”±”¢”°Ę«µĶ”±»ņ”°ĪŽÓ°Ļģ”±£©£»
£Ø2£©7.8gĆ¾ĀĮŗĻ½šÓė×ćĮæµÄĻ”ŃĪĖį·“Ó¦£¬Éś³ÉĒāĘųµÄĢå»żĪŖ8.96L£Ø±ź×¼×“æö£©£¬Ōņ“Ė·“Ó¦ÖŠ×ŖŅʵē×ӵďżÄæĪŖ £¬ Ć¾ŗĶĀĮ·Ö±š²śÉśĒāĘųµÄĢå»żÖ®±ČĪŖ £®
”¾“š°ø”æ
£Ø1£©Ę«øߣ»Ę«µĶ£»Ę«øß
£Ø2£©0.8NA£»2£ŗ3
”¾½āĪö”æ½ā£ŗ£Ø1£©¢ŁÅØĮņĖįČܽāŗóĪ“ĄäČ“ÖĮŹŅĪĀ¼“×ŖŅĘÖĮČŻĮæĘæÖŠ½ųŠŠ¶ØČŻ£¬ĄäČ“ŗóČÜŅŗĢå»żĘ«Š”£¬ČÜŅŗÅضČĘ«øߣ»ĖłŅŌ“š°øŹĒ£ŗĘ«øߣ»¢Ś¶ØČŻŹ±ŃöŹÓæĢ¶ČĻߣ¬µ¼ÖĀČÜŅŗĢå»żĘ«“ó£¬ČÜŅŗÅضČĘ«µĶ£»
ĖłŅŌ“š°øŹĒ£ŗĘ«µĶ£»¢ŪĮæČ”ŗĆÅØĮņĖįµ¹ČėÉÕ±Čܽāŗó£¬ÓĆĖ®Ļ“µÓĮæĶ²2”«3“Ī£¬½«Ļ“µÓŅŗµ¹ČėÉÕ±ÖŠ£¬µ¼ÖĀĮæČ”µÄÅØĮņĖįĢå»żĘ«“ó£¬ČÜÖŹµÄĪļÖŹµÄĮæĘ«“ó£¬ČÜŅŗÅضČĘ«øߣ»
ĖłŅŌ“š°øŹĒ£ŗĘ«øߣ»£Ø2£©Įī7.8gĆ¾ĀĮŗĻ½šÖŠMgµÄĪļÖŹµÄĮæĪŖxmol£¬AlµÄĪļÖŹµÄĮæĪŖymol£¬Ōņ£ŗ24x+27y=7.8£¬
Éś³ÉĒāĘųµÄĪļÖŹµÄĮæĪŖ ![]() =0.4mol£¬øł¾Żµē×Ó×ŖŅĘŹŲŗćÓŠ£ŗ2x+3y=0.4”Į2£¬
=0.4mol£¬øł¾Żµē×Ó×ŖŅĘŹŲŗćÓŠ£ŗ2x+3y=0.4”Į2£¬
ĮŖĮ¢·½³Ģ£¬½āµĆ£ŗx=0.1£¬y=0.2£»
Éč×ŖŅʵē×ÓŹżĪŖnŌņ£ŗ
2H+”«H2”ü”«2e©
1 2
0.4mol n
½āµĆn=0.8mol£»
ĖłŅŌ×ŖŅʵē×ÓŹżĪŖ0.8NA£»
ŅĄ¾ŻĆ¾”¢ĀĮÓėŃĪĖį·“Ӧɜ³ÉĘųĢå¹ŲĻµµĆ£»
Mg”«”«”«H2”ü Al”«”«”«1.5H2”ü
1 2 1 1.5
0.1mol 0.2mol 0.2mol 0.3mol
ĖłŅŌĆ¾ÓėĀĮÓėŃĪĖį·“Ӧɜ³ÉĒāĘųµÄĢå»żÖ®±ČµČÓŚĪļÖŹµÄĮæÖ®±ČµČÓŚ£ŗ0.2£ŗ0.3=2£ŗ3£»
ĖłŅŌ“š°øŹĒ£ŗ0.8NA£»2£ŗ3£»


 ĆūŠ£æĪĢĆĻµĮŠ“š°ø
ĆūŠ£æĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æij»ÆѧŠ”×éŅŌ±½¼×ĖįĪŖŌĮĻ£¬ÖĘČ”±½¼×Ėį¼×õ„£¬ŅŃÖŖÓŠ¹ŲĪļÖŹµÄ·ŠµćČē±ķ£ŗ
ĪļÖŹ | ¼×“¼ | ±½¼×Ėį | ±½¼×Ėį¼×õ„ |
·Šµć/”ę | 64.7 | 249 | 199.6 |
£Ø1£©ŗĻ³É±½¼×Ėį¼×õ„“Ö²śĘ· £Øi£©¼×ŗĶŅŅĮ½Ī»Ķ¬Ń§·Ö±šÉč¼ĘĮĖČēĶ¼ĖłŹ¾µÄĮ½Ģ׏µŃéŹŅŗĻ³É±½¼×Ėį¼×õ„µÄ×°ÖĆ£Ø¼Š³ÖŅĒĘ÷ŗĶ¼ÓČČŅĒĘ÷¾łŅŃĀŌČ„£©£®øł¾ŻÓŠ»śĪļµÄ·Šµć£¬×īŗĆ²ÉÓĆ£ØĢī”°¼×”±»ņ”°ŅŅ”±£©×°ÖĆ£®ĄķÓÉŹĒ £® 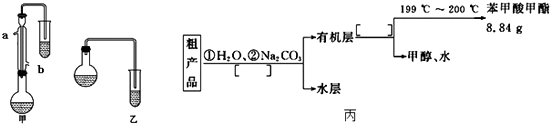
£Øii£©ŹµŃéÖŠÅØĮņĖįµÄ×÷ÓĆŹĒĄäÄżĖ®Ó¦“Ó£ØĢī”°a”±»ņ”°b”±£¬ĻĀĶ¬£©æŚ½ų£¬æŚ³ö£®
£Øiii£©·“Ó¦ĪļCH3OHÓ¦¹żĮ棬ĄķÓÉŹĒ£»Į½Ģ××°ÖĆÖŠµ¼¹ÜÄ©¶Ė¾łĆ»ÓŠÉģČėµ½ŹŌ¹ÜŅŗĆęŅŌĻĀµÄŌŅņ £®
£Ø2£©“Ö²śĘ·µÄ¾«ÖĘ ±½¼×Ėį¼×õ„“Ö²śĘ·ÖŠĶłĶłŗ¬ÓŠÉŁĮæ¼×“¼”¢±½¼×ĖįŗĶĖ®µČ£¬ĻÖÄāÓĆĻĀĮŠĮ÷³ĢĶ¼½ųŠŠ¾«ÖĘ£¬ĒėŌŚĮ÷³ĢĶ¼±ūÖŠ·½ĄØŗÅÄŚĢīČė²Ł×÷·½·ØµÄĆū³Ę£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ½«Ć¾”¢ĀĮµÄ»ģŗĻĪļ¹²0.2mol£¬ČÜÓŚ200mL 4molL©1µÄŃĪĖįČÜŅŗÖŠ£¬Č»ŗóŌŁµĪ¼Ó2molL©1µÄNaOHČÜŅŗ£®Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ČōŌŚµĪ¼ÓNaOHČÜŅŗµÄ¹ż³ĢÖŠ£¬³ĮµķÖŹĮæm Ėę¼ÓČėNaOHČÜŅŗµÄĢå»żV±ä»ÆĒéæöČēĶ¼ĖłŹ¾£®µ±V1=160mLŹ±£¬Ōņ½šŹō·ŪÄ©ÖŠn £ØAl£©=mol
£Ø2£©0”«V1¶Ī·¢ÉśµÄ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£»
£Ø3£©ČōŌŚµĪ¼ÓNaOHČÜŅŗµÄ¹ż³ĢÖŠ£¬ÓūŹ¹Mg2+”¢Al3+øÕŗĆ³ĮµķĶźČ«£¬ŌņµĪČėNaOHČÜŅŗµÄĢå»żV£ØNaOH£©=mL£»
£Ø4£©ČōĆ¾”¢ĀĮµÄ»ģŗĻĪļČŌĪŖ0.2mol£¬ĘäÖŠĆ¾·ŪµÄĪļÖŹµÄĮæ·ÖŹżĪŖa£¬øÄÓĆ200mL 4molL©1µÄĮņĖįČܽā“Ė»ģŗĻĪļŗó£¬ŌŁ¼ÓČė840mL 2molL©1µÄNaOHČÜŅŗ£¬ĖłµĆ³ĮµķÖŠĪŽAl£ØOH£©3 £¬ ŌņaµÄȔֵ·¶Ī§ĪŖ £®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÉč°¢·üŁ¤µĀĀŽ³£ŹżĪŖ NA £¬ ŌņĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
A.³£ĪĀ³£Ń¹ĻĀ£¬1mol C nH 2n+2ÖŠĖłŗ¬ÓŠµÄ¹²¼Ū¼üŹżÄæĪŖ£Ø3n+1£©N A
B.14g ŅŅĻ©ŗĶ±ūĻ©µÄ»ģŗĻĪļÖŠŗ¬ÓŠŌ×ӵďżÄæĪŖN A
C.±ź×¼×“æöĻĀ£¬1 LĪģĶé³ä·ÖČ¼ÉÕŗóÉś³ÉµÄĘųĢ¬²śĪļµÄ·Ö×ÓŹżĪŖ ![]() NA
NA
D.1.5g ¼×»ł£Ø©CH 3£©Ėłŗ¬ÓŠµÄµē×ÓŹżŹĒ N A
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓĆ98%µÄÅØĮņĖį£Ø¦Ń=1.84g/cm3£©ÅäÖĘ250mL 1mol/LµÄĻ”ĮņĖį£¬ĖłŠčÅØĮņĖįµÄĢå»żĪŖmL£ØŠ”Źżµćŗó±£ĮōŅ»Ī»ÓŠŠ§Źż×Ö£©£®Čē¹ūŹµŃéŹŅÓŠ10mL”¢20mL”¢50mLĮæĶ²£¬Ó¦Ń”ÓĆmLĮæĶ²£¬ŹµŃéÖŠ»¹ŠčŅŖÓƵ½µÄŅĒĘ÷ÓŠÉÕ±”¢½ŗĶ·µĪ¹Ü”¢²£Į§°ōŗĶ £®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠŌŖĖŲ“¦ÓŚµŚ¶žÖÜĘŚ¢÷A×åµÄŹĒ£Ø £©
A. Cl B. O C. F D. S
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠø÷×éÓŠ»śĪļÖŠ£¬Ö»Šč¼ÓČėäåĖ®¾ĶÄÜŅ»Ņ»¼ų±šµÄŹĒ£Ø £©
A.±½”¢¼ŗĶé
B.¼ŗČ²”¢¼ŗĻ©
C.±½”¢¼×±½
D.¼ŗĻ©”¢±½
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĪļÖŹÖŠ£¬²»ÄÜ×÷ĪŖŹ³Ę·Ģķ¼Ó¼ĮµÄŹĒ
A.Ź³ŃĪB.ŃĒĻõĖįÄĘC.±½¼×ĖįÄĘD.¼×“¼
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŅĖį±½¼×õ„£Ø ![]() £©¹ć·ŗ“ęŌŚÓŚæÉæÉ”¢æ§·Č”¢²ŻŻ®µČĪļÖŹÖŠ£¬æÉÓĆ×÷Ź³ĪļŗĶČÕ»ÆÓĆĘ·µÄĻć¾«£® ŅŃÖŖ£ŗXµÄ²śĮææÉŅŌÓĆĄ“ŗāĮæŅ»øö¹ś¼ŅµÄŹÆÓĶ»Æ¹¤·¢Õ¹Ė®Ę½£¬¹¤ŅµÉĻæÉÓĆXŗĶ¼×±½ČĖ¹¤ŗĻ³ÉŅŅĖį±½¼×õ„£®ĘäŗĻ³ÉĀ·ĻßČēĻĀ£ŗ
£©¹ć·ŗ“ęŌŚÓŚæÉæÉ”¢æ§·Č”¢²ŻŻ®µČĪļÖŹÖŠ£¬æÉÓĆ×÷Ź³ĪļŗĶČÕ»ÆÓĆĘ·µÄĻć¾«£® ŅŃÖŖ£ŗXµÄ²śĮææÉŅŌÓĆĄ“ŗāĮæŅ»øö¹ś¼ŅµÄŹÆÓĶ»Æ¹¤·¢Õ¹Ė®Ę½£¬¹¤ŅµÉĻæÉÓĆXŗĶ¼×±½ČĖ¹¤ŗĻ³ÉŅŅĖį±½¼×õ„£®ĘäŗĻ³ÉĀ·ĻßČēĻĀ£ŗ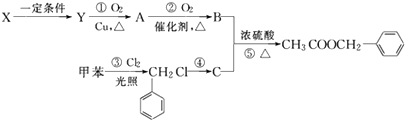
¾Ż“Ė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©XÉś³ÉYµÄ»Æѧ·½³ĢŹ½ĪŖ £¬ Éś³ÉĪļYÖŠŗ¬ÓŠ¹ŁÄÜĶŵÄĆū³ĘĪŖ £®
£Ø2£©![]() ·¢Éś·“Ó¦¢ÜĖłŠčµÄĢõ¼žŹĒ £¬ øĆ·“Ó¦µÄ·“Ó¦ĄąŠĶĪŖ £®
·¢Éś·“Ó¦¢ÜĖłŠčµÄĢõ¼žŹĒ £¬ øĆ·“Ó¦µÄ·“Ó¦ĄąŠĶĪŖ £®
£Ø3£©ŹµŃéŹŅĪŖ¼ų±šAŗĶBĮ½ÕßµÄĖ®ČÜŅŗ£¬æÉŅŌŃ”ÓƵĻÆѧŹŌ¼ĮŹĒ £® A£®“æ¼īČÜŅŗ””B£®NaOHČÜŅŗ””C£®½šŹōÄĘ””D£®Ņų°±ČÜŅŗ
£Ø4£©ÉĻŹö·“Ó¦¢Ł”«¢ŻÖŠŌ×ӵĥķĀŪĄūÓĆĀŹĪŖ100%”¢·ūŗĻĀĢÉ«»ÆѧŅŖĒóµÄ·“Ó¦ŹĒ£ØĢīŠņŗÅ£©£®
£Ø5£©ĒėŠ“³ö·“Ó¦¢ŻµÄ»Æѧ·½³ĢŹ½ £®
£Ø6£©Š“³ö·ūŗĻĻĀĮŠĢõ¼žµÄŅŅĖį±½¼×õ„µÄŅ»ÖÖĶ¬·ÖŅģ¹¹Ģå£ŗ¢Łŗ¬±½»·½į¹¹£»¢Ś¾ßÓŠõ„µÄ½į¹¹£® £®
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com