
天然气化工是指通过甲烷的化学反应来生产一系列化工产品的工艺过程。以天然气为原料经下列反应路线可得工程塑料PBT。
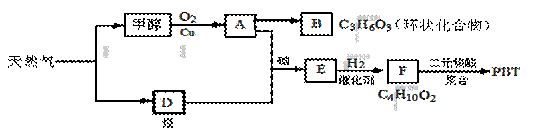
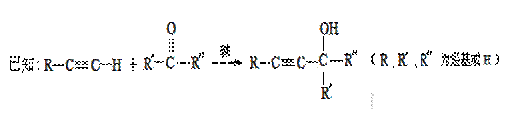
(1)B分子结构中只有一种氢、一种氧、一种碳,则B的结构简式是 ;B的同分异构体中与葡萄糖具有类似结构的是 。(写结构简式)
(2)F的结构简式是 ;PBT属于 类有机高分子化合物。
(3)由A、D生成E的反应方程式为 ,其反应类型为 。
(4)E的同分异构体G不能发生银镜反应,能使溴水褪色,能水解且产物的碳原子数不等,则G在NaOH溶液中发生水解反应的化学方程式是 。
【知识点】有机物的推断M3
【答案解析】
(1)
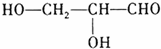
(2)HO—CH2—CH2—CH2—CH2—OH ; 酯(或聚酯)
(3)HC≡CH+2HCHO HOCH2C≡CCH2OH;加成反应
HOCH2C≡CCH2OH;加成反应
(4)CH2=CH—COOCH3+NaOH CH2=CH—COONa+CH3OH
CH2=CH—COONa+CH3OH
解析:(1)甲醇氧化生成甲醛(HCHO),结合A、B的分子式可知,B为3分子甲醛形成,B分子结构中只有一种氢、一种氧、一种碳,是3分子甲醛之间的加成反应生成B,故B的结构简式为: ,B的同分异构体与葡萄糖结构类似,该异构体中含有1个-CHO,2个羟基-OH,为链状结构,该同分异构体的结构简式为
,B的同分异构体与葡萄糖结构类似,该异构体中含有1个-CHO,2个羟基-OH,为链状结构,该同分异构体的结构简式为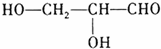 ,
,
(2)由E→F的转化及F分子式可知,E中含有4个C原子,由HCHO+D→E,再根据已知反应信息可知,该反应为2分子甲醛与乙炔发生加成反应,D为HC≡CH,E为HOCH2-C≡C-CH2OH,E与氢气发生加成反应生成F,故F结构简式为HO-CH2-CH2-CH2-CH2-OH,F与二元羧酸通过酯化反应形成高聚物PBT,PBT属于酯类;
(3)由(2)中分析可知,该反应为该反应为2分子甲醛与乙炔发生加成反应生成HOCH2-C≡C-CH2OH,由A、D生成E的反应方程式为:HC≡CH+2HCHO HOCH2C≡CCH2OH;
HOCH2C≡CCH2OH;
(4)HOCH2-C≡C-CH2OH的同分异构体G不能发生银镜反应,分子中不含醛基-CHO或-OOCH,能使溴水褪色,含有不饱和键,能水解且产物的碳原子数不等,含有酯基,故含有1个C=C双键、1个酯基,且形成该酯的羧酸含有3个碳原子,醇为甲醇,故G的结构简式为:CH2=CH-COOCH3,CH2=CH-COOCH3在氢氧化钠溶液中发生水解方程式为:
CH2=CH-COOCH3+NaOH→CH2=CH-COONa+CH3OH;
【思路点拨】本题考查有机物的推断与合成,充分利用有机物的分子式与反应信息进行判断,难度中等,能较好的考查考生的阅读、自学能力和思维能力,是热点题型。


科目:高中化学 来源: 题型:
据报道,有一种叫Thibacillus Ferroxidans 的细菌在氧气存在下的酸性溶液中,能将黄铜矿(CuFeS2)氧化成硫酸盐,发生的反应为:
4CuFeS2+2H2SO4+17O2=4CuSO4+2Fe2(SO4)3+2H2O
(1)CuFeS2中的Fe的化合价为+2,则被氧化的元素为 (填元素名称)
(2)工业生产中利用上述反应后的溶液,按如下流程可制备胆矾(CuSO4·5H2O):

①分析下列表格(其中Ksp是相应金属氢氧化物的沉淀溶解平衡常数):
| Ksp | 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe3+ | 2.6×10-39 | 1.9 | 3.2 |
| Cu2+ | 2.2×10-20 | 4.7 | 6.7 |
步骤一应调节溶液的pH范围是 ,请运用沉淀溶解平衡的有关理论解释加入CuO能除去CuSO4溶液中Fe3+的原因
②步骤三中的具体操作方法是
(3)工业上冶炼铜的方法之一为:
Cu2S(s)+2Cu2O(s)=6Cu(s)+SO2(g) ΔH
已知:①2Cu(s)+1/2O2(g)=Cu2O(s) ΔH=-12kJ/mol
②2Cu(s)+S(s)=Cu2S(s) ΔH=-79.5kJ/mol
③S(s)+O2(g)=SO2(g) ΔH=-296.8kJ/mol
则该法冶炼铜的反应中ΔH= 。
查看答案和解析>>
科目:高中化学 来源: 题型:
有机物X的结构如下,下列说法正确的是
A. X能发生氧化、取代、酯化、加聚、缩聚反应
B. X与FeCl3溶液不能发生显色反应
C. 1mol X与足量NaOH溶液反应,最多消耗2mol NaOH
D. X的分子式为C23H26 N2O7
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子在给定条件下能大量共存的是 ( )
A.在c(HCO3-)=0.1 mol·L-1的溶液中:NH4+、Al3+、Cl-、NO3-
B.有大量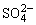 存在的溶液中:Na+、Mg2+、Ca2+、I-
存在的溶液中:Na+、Mg2+、Ca2+、I-
C.有大量 存在的强酸性溶液中:NH4+、Ba2+、Fe2+、Br-
存在的强酸性溶液中:NH4+、Ba2+、Fe2+、Br-
D.能使红色石蕊试纸变蓝的溶液中:SO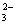 、S2-、Na+、K+
、S2-、Na+、K+
查看答案和解析>>
科目:高中化学 来源: 题型:
某二价金属的碳酸盐和酸式碳酸盐的混合物,跟足量的稀盐酸反应,消耗H+和生成CO2物质的量之比为6:5,则该混合物中碳酸盐和酸式碳酸盐的物质的量之比是 ( )
A.1:1 B.1:2 C.1: 3 D.1:4
查看答案和解析>>
科目:高中化学 来源: 题型:
为了使宇航员在飞船中得到一个稳定的、良好的生存环境,一般在飞船内安装盛有Na2O2或K2O2颗粒的装置,它的用途是产生氧气。下列关于Na2O2的叙述正确的是
①Na2O2中阴、阳离子的个数比是1:1
②Na2O2分别与水及CO2反应产生等量氧气时,需水和CO2的质量相等
③Na2O2分别与水及CO2反应产等量氧气时,转移电子的物质的量相等
④Na2O2的漂白原理与SO2的漂白原理相同
⑤Na2O2与SO2反应生成Na2SO3与H2O
⑥Na2O2能与酸反应生成盐和水,所以Na2O2是碱性氧化物
⑦Na2O2与水反应,Na2O2既是氧化剂,又是还原剂
⑧Na2O2投入到紫色石蕊试液中,溶液先变蓝,后褪色
A.①③⑥⑧ B.③⑦⑧ C②⑤⑥⑦ D.①④⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
汽车剧烈碰撞时,安全气囊中发生反应:10NaN3+2KNO3= K2O+5Na2O+16N2↑。若氧化产物比还原产物多1. 75 mol,则下列判断正确的是
A.生成40.0 L N2(标准状况) B.有0. 250 mol KNO3被氧化
C.转移电子的物质的量为1. 75mol D.被氧化的N原子的物质的量为3.75mol
查看答案和解析>>
科目:高中化学 来源: 题型:
从海带中制取单质碘需要经过灼烧、溶解、过滤、氧化、萃取、分液、蒸馏等操作。下列图示 对应的装置合理、操作规范的是
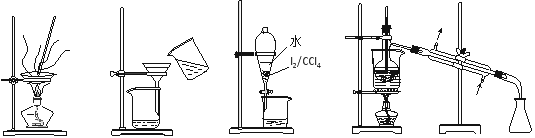
A.灼烧 B.过滤 C.分液 D.蒸馏
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:①N2(g)+O2(g)═2NO(g)△H1=+180kJ•mol﹣1
②N2(g)+3H2(g)⇌2NH3(g)△H2=﹣92.4kJ•mol﹣1
③2H2(g)+O2(g)═2H2O(g)△H3=﹣483.6kJ•mol﹣1
下列说法正确的是( )
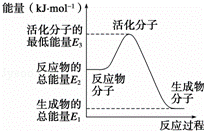
|
| A. | 反应②中的能量变化如图所示,则△H2=E1﹣E3 |
|
| B. | H2的燃烧热为241.8 kJ•mol﹣1 |
|
| C. | 由反应②知在温度一定的条件下,在一恒容密闭容器中通入1 mol N2和3 mol H2,反应后放出的热量为Q1 kJ,若通入2 mol N2和6 mol H2充分反应后放出的热量为Q2 kJ,则184.8>Q2>2Q1 |
|
| D. | 氨的催化氧化反应为4NH3(g)+5O2(g)═4NO(g)+6H2O(g)△H=+906 kJ•mol﹣1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com