
CuSO4是一种重要的化工原料,其有关制备途径及性质如图所示。下列说法不正确的是

A.相对于途径①,途径②更好地体现了绿色化学思想
B.Y可以是葡萄糖溶液
C.CuSO4在1100℃分解所得气体X可能是SO2和SO3的混合气体
D.将CuSO4溶液蒸发浓缩,冷却结晶可制得胆矾晶体
科目:高中化学 来源:2016-2017学年安徽省高一上期中化学试卷(解析版) 题型:选择题
在150℃时,(NH4)2CO3分解的方程式为:(NH4)2CO3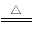 2NH3↑+H2O↑+CO2↑
2NH3↑+H2O↑+CO2↑
若完全分解,产生的气态混合物的密度是相同条件下氢气密度的( )
A.12倍 B.24倍 C.48倍 D.96倍
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省高二上期中化学试卷(解析版) 题型:推断题
已知:①醛在一定条件下可以两分子加成:
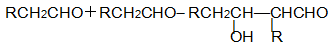
产物不稳定,受热即脱水而生成不饱和醛。
②B是一种芳香族化合物。根据下图所示转化关系填空(所有无机物均已略去)
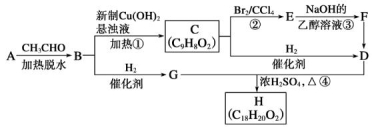
③在醇溶液中不考虑羧酸与氢氧化钠的中和反应
(1)写出 B、F的结构简式:
B____________________;F____________________。
(2)写出②和③反应的反应类型:
②____________;③_____________。
(3)写出下列化学方程式:
A→B_______________________________
E→F_______________________________
(4) D满足下列条件的同分异构体有 种
①是芳香族化合物,②能发生银镜反应和水解反应
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省高二上期中化学试卷(解析版) 题型:选择题
下列实验能成功的是
A. 用 1体积的乙醇与3体积的浓H2SO4混合加热到140℃制乙烯
B. 加入适量浓溴水除去苯中混有的少量苯酚
C. 用饱和食盐水和电石(CaC2)制乙炔
D. 以盐酸、石灰石、苯酚钠溶液为试剂,验证酸性强弱关系:盐酸>石炭酸>碳酸
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省瓦房店市高三上10月月考化学试卷(解析版) 题型:实验题
亚硝酸钠常用作食品防腐剂。现用下图所示仪器(夹持装置已省略)及药品,探究亚硝酸钠与硫酸的反应及生成气体产物的成分。
已知:①NO+NO2+2OH-===2NO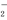 +H2O
+H2O
②气体液化的温度:NO2:21℃、NO:-152℃
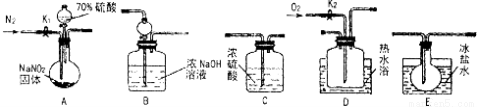
(1)为了检验装置A中生成的气体产物,仪器的连接顺序为(按左→右连接):
(2)组装好仪器后,接下来进行的操作是 .
(3)关闭弹簧夹K1,打开分液漏斗活塞,滴入70%硫酸后,A中产生红棕色气体。
①确认A中产生的气体中含有NO,依据的现象是___________________。
②装置B的作用是___________________,装置E的作用是____________。
(4)如果向D中通入过量O2,则装置B中发生反应的化学方程式为 。如果没有装置C,对实验结论造成的影响是__________________。
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省瓦房店市高三上10月月考化学试卷(解析版) 题型:选择题
某稀硫酸和稀硝酸的混合溶液中c(SO42-)+c(NO3-)=2.5 mol•L-1.取200mL该混合酸,则能溶解铜的最大质量为
A.12.8g B.19.2g C.32.0g D.38.4g
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省瓦房店市高三上10月月考化学试卷(解析版) 题型:选择题
分类法是一种行之有效、简单易行的科学方法。某同学用下表所示形式对所学知识进行分类,其中甲与乙、丙、丁是包含关系。下列各组中,不正确的组合是
选项 | 甲 | 乙、丙、丁 |
A | 纯 | 液氯、FeO·Fe2O3、明矾 |
B | 非电解质 | CO2、SO2、乙醇 |
C | 弱电解质 | CH3COOH 、氨水、H2O |
D | 强电解质 | HCl、NaOH、BaSO4 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年青海省高二上月考一化学卷(解析版) 题型:选择题
对于反应mA+nB===pC,下列说法正确的是( )
A.某温度时,化学反应速率无论用A、B、C何种物质表示,其数值是相同的
B.其他条件不变,增大压强,反应速率加快
C.若增加或减小B的物质的量,则反应速率一定会发生明显的变化
D.其他条件不变,升高温度,反应速率加快
查看答案和解析>>
科目:高中化学 来源:2016-2017学年贵州省高二上半期考试化学卷(解析版) 题型:填空题
(1)反应A(g)+B(g)  C(g) +D(g)过程中的能量变化如图所示(E1>0,E2>0),回答下列问题。
C(g) +D(g)过程中的能量变化如图所示(E1>0,E2>0),回答下列问题。
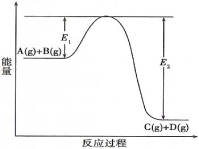
①图中该反应是_________反应(填“吸热”、“放热”)。反应热△H的表达式为__________。
②在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1_________,E2_________(填“增大”、“减小”或“不变”)
(2)丙烷是一种价格低廉的常用燃料,其主要成分是碳和氢两种元素,燃烧后只有二氧化碳和气态水,不会对环境造成污染。已知1 g丙烷完全燃烧放出50.45 kJ的热量。试回答下列问题。丙烷在室温下燃烧的热化学方程式为_______________。
(3)C3H8(g)→CH4(g)+HC≡CH(g)+H2(g)△H1=+156.6kJ·mol-1;
CH3CH=CH2(g)→CH4(g)+HC≡CH(g)△H2=+32.4kJ·mol-1。
则相同条件下,反应:C3H8(g)→CH3CH=CH2(g)+H2(g)的△H= kJ·mol-1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com